前四周期元素结构信息见表,回答下列问题。
(1)A、B、C、E四种元素,第一电离能由大到小的顺序为___________ (用元素符号表示)。
(2)基态D元素的核外电子排布式为___________ 。
(3)写出B基态原子价电子的轨道式___________ 。
(4)E基态原子填有电子的轨道数为___________ 。
| 元素 | 结构信息 |
| A | 基态原子有6个原子轨道填充满电子,有3个未成对电子· |
| B | M层电子数比L层电子数少两个 |
| C | 基态原子有17个不同运动状态的电子 |
| D | 基态原子的价电子排布为3dx4s2,在常见化合物中其最高正价为+7 |
| E | 基态原子的M层全充满,N层没有成对电子,只有1个未成对电子 |
(2)基态D元素的核外电子排布式为
(3)写出B基态原子价电子的轨道式
(4)E基态原子填有电子的轨道数为
更新时间:2023-06-30 14:28:37
|
相似题推荐
【推荐1】法国一家公司研发出一种比锂电池成本更低、寿命更长、充电速度更快的钠离子电池,该电池的负极材料为Na2Co2TeO6(制备原料为Na2CO3、Co3O4和TeO2),电解液为NaClO4的碳酸丙烯酯溶液。回答下列问题:
(1)C、O、Cl三种元素电负性由大到小的顺序为_______ 。
(2)基态Na原子中,核外不同电子运动状态的数目为_______ ,Co属于元素周期表中_______ 区元素,其基态原子的价电子排布式为_______ 。
(3)碳酸丙烯酯的结构简式如图所示,其中碳原子的杂化轨道类型为_______ ,1mol碳酸丙烯酯中σ键的数目为_______ 。

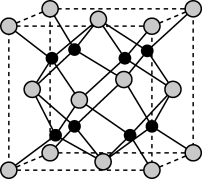
(4)Na和O形成的离子化合物的晶胞结构如图所示,已知该晶胞的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则Na与O之间的最短距离为_______ cm(用含有ρ、NA的代数式表示)。
(1)C、O、Cl三种元素电负性由大到小的顺序为
(2)基态Na原子中,核外不同电子运动状态的数目为
(3)碳酸丙烯酯的结构简式如图所示,其中碳原子的杂化轨道类型为

(4)Na和O形成的离子化合物的晶胞结构如图所示,已知该晶胞的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则Na与O之间的最短距离为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】点击化学(click chemistry)是一种能够让分子的构建模块快速、高效地结合在一起的化学反应。科学工作者可以利用基础模块搭建出变化无穷的造型,就如同玩乐高玩具一般。叠氨化物和块经合成抗真菌药物三唑是点击化学的重要应用,反应示例如下:
(1) 的核外电子排布式为
的核外电子排布式为_______ 。
(2)C、N、Cu的电负性由大到小的顺序为_______ 。
(3)分子乙中存在5中心6电子的大 键,其中,提供两个电子形成大
键,其中,提供两个电子形成大 键(
键( )的原子是
)的原子是_______ (填对应原子的序号)。
(4)分子中碳碳三键的活泼性:甲_______ 丙(填“>”“=”“<”),理由是_______ (从分子的结构角度分析)。
(5)丁形成的晶体中不存在的微粒间作用力有_______ 。
A.离子键 B.极性键 C.非极性键 D.氢键 E.范德华力
(6)CuCl的晶胞中, 的位置如图所示,
的位置如图所示, 填充于
填充于 构成的四面体空隙中。
构成的四面体空隙中。 的配位数为
的配位数为_______ 。
②由 构成的八面体空隙与有
构成的八面体空隙与有 填充的
填充的 构成的四面体空隙的数目之比为
构成的四面体空隙的数目之比为_______ 。
 +CH3CH2N3
+CH3CH2N3

 +CH3CH2N3→
+CH3CH2N3→
(1)
 的核外电子排布式为
的核外电子排布式为(2)C、N、Cu的电负性由大到小的顺序为
(3)分子乙中存在5中心6电子的大
 键,其中,提供两个电子形成大
键,其中,提供两个电子形成大 键(
键( )的原子是
)的原子是(4)分子中碳碳三键的活泼性:甲
(5)丁形成的晶体中不存在的微粒间作用力有
A.离子键 B.极性键 C.非极性键 D.氢键 E.范德华力
(6)CuCl的晶胞中,
 的位置如图所示,
的位置如图所示, 填充于
填充于 构成的四面体空隙中。
构成的四面体空隙中。
 的配位数为
的配位数为②由
 构成的八面体空隙与有
构成的八面体空隙与有 填充的
填充的 构成的四面体空隙的数目之比为
构成的四面体空隙的数目之比为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】超分子化学已逐渐扩展到化学的各个分支,还扩展到生命科学和物理学等领域。由Mo将2个 分子、2个p—甲酸丁酯毗啶及2个CO分子利用配位键自组装的超分子结构如图所示:
分子、2个p—甲酸丁酯毗啶及2个CO分子利用配位键自组装的超分子结构如图所示:

(1)Mo处于第五周期第VIB族,核外电子排布与Cr相似,它的基态价电子排布式是_ ;核外未成对电子数是_______ 个。
(2)该超分子中除配位键外还存在的化学键类型有_ (填标号)。
A.σ键 B.π键 C.氢键
(3) 与金刚石互为同素异形体,从结构与性质之间的关系解释
与金刚石互为同素异形体,从结构与性质之间的关系解释 的熔点远低于金刚石的原因是
的熔点远低于金刚石的原因是_______ 。
(4)钼铝合金性能优良,其立方晶胞如图甲所示(Al未画出),其中Mo按体心立方堆积,每个Mo周围围绕的Al形成正二十面体(如图乙),即每个Mo位于正二十面体的中心。基态Al核外电子云轮廓图呈球形、哑铃形的能级上电子数之比为_______ 。已知该晶胞参数为a pm,Mo之间的最短距离为_______ pm,则该晶体的密度为_______  (设
(设 为阿伏加德罗常数的值,用含a、
为阿伏加德罗常数的值,用含a、 的代数式表示)。
的代数式表示)。

 分子、2个p—甲酸丁酯毗啶及2个CO分子利用配位键自组装的超分子结构如图所示:
分子、2个p—甲酸丁酯毗啶及2个CO分子利用配位键自组装的超分子结构如图所示:
(1)Mo处于第五周期第VIB族,核外电子排布与Cr相似,它的基态价电子排布式是
(2)该超分子中除配位键外还存在的化学键类型有
A.σ键 B.π键 C.氢键
(3)
 与金刚石互为同素异形体,从结构与性质之间的关系解释
与金刚石互为同素异形体,从结构与性质之间的关系解释 的熔点远低于金刚石的原因是
的熔点远低于金刚石的原因是(4)钼铝合金性能优良,其立方晶胞如图甲所示(Al未画出),其中Mo按体心立方堆积,每个Mo周围围绕的Al形成正二十面体(如图乙),即每个Mo位于正二十面体的中心。基态Al核外电子云轮廓图呈球形、哑铃形的能级上电子数之比为
 (设
(设 为阿伏加德罗常数的值,用含a、
为阿伏加德罗常数的值,用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题
(1)钛在元素周期表中的位置___________ ,基态钛原子的价层电子轨道表示式为___________ ,与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有___________ 种。下列状态的钛元素形成得微粒中,电离其最外层的一个电子所需能量最小的是___________ (填序号)。
A.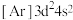 B.
B.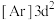 C.
C.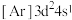 D.
D.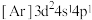
(2)第三周期元素中第一电离能介于Al和P的元素有___________ 种。与Co同周期,基态原子有1个未成对电子的元素有___________ 种。
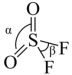
(3) 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是___________ 。
(4) 、
、 、
、 沸点由高到低的顺序为
沸点由高到低的顺序为___________ ,其主要原因是___________ 。
(5)铜离子的一种配合物化学式为 ,该配合物中铜离子的配位数为
,该配合物中铜离子的配位数为___________ 。
(6)醋酸 中C原子的杂化类型为
中C原子的杂化类型为___________ 。
(7)等物质的量的 和
和 中,σ键数目之比
中,σ键数目之比___________ 。
(1)钛在元素周期表中的位置
A.
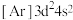 B.
B.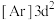 C.
C.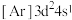 D.
D.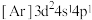
(2)第三周期元素中第一电离能介于Al和P的元素有
(3)
 分子结构如图所示,已知键角
分子结构如图所示,已知键角 为124°,
为124°, 为96°,则
为96°,则 的原因主要是
的原因主要是
(4)
 、
、 、
、 沸点由高到低的顺序为
沸点由高到低的顺序为(5)铜离子的一种配合物化学式为
 ,该配合物中铜离子的配位数为
,该配合物中铜离子的配位数为(6)醋酸
 中C原子的杂化类型为
中C原子的杂化类型为(7)等物质的量的
 和
和 中,σ键数目之比
中,σ键数目之比
您最近一年使用:0次
【推荐2】元素周期表前3周期的元素a、b、c,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍。回答下列问题:
(1)a的基态原子核外电子运动的轨道呈____ 形。
(2)b的基态原子的核外电子占据____ 个原子轨道。
(3)c的外围电子轨道表示式为____ 。
(4)b与c的第一电离能相比,较大的是____ (填元素符号),理由是____ 。
(1)a的基态原子核外电子运动的轨道呈
(2)b的基态原子的核外电子占据
(3)c的外围电子轨道表示式为
(4)b与c的第一电离能相比,较大的是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】某些元素在周期表中的位置如图
(1)A位于元素周期表第_______ 周期第_______ 族;B的基态原子核外有_______ 未成对电子;
(2)C基态原子价层电子排布式为_______ ;
(3)D基态原子,最外层电子的电子云轮廓图形状为_______ ;E基态原子中,电子占据的最高能层符号为_______ ,该能层具有的原子轨道数为_______ ;
(4)F基态原子,核外存在_______ 对自旋相反的电子
(5)G的正二价阳离子的价层电子排布图为_______ ;
(6)下列说法中正确的是 。
| A | B | C | |||||||||||||||
| D | E | F | |||||||||||||||
| G | H | I | |||||||||||||||
(1)A位于元素周期表第
(2)C基态原子价层电子排布式为
(3)D基态原子,最外层电子的电子云轮廓图形状为
(4)F基态原子,核外存在
(5)G的正二价阳离子的价层电子排布图为
(6)下列说法中正确的是 。
| A.元素H和I在元素周期表中位于同一个区 |
| B.元素A的基态原子中,能量不同的电子有6种 |
| C.与元素I具有相同最外层电子数的元素只可能处于ds区 |
| D.元素B的基态原子空间运动状态有5种 |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D都是元素周期表中的短周期元素,它们的核电荷数依次增大.A是元素周期表中原子半径最小的元素,非金属元素B原子的核外电子数是未成对电子数的3倍,C原子的最外层p轨道的电子为半充满结构,D是地壳中含量最多的元素,E位于第4周期,其基态原子的内层轨道全部排满电子,且最外层电子数与A相同。回答下列问题:
⑴E的基态原子价电子排布图______ 。
⑵B、C、D的第一电离能由小到大的顺序为______ 。 用元素符号表示
用元素符号表示
⑶CA3物质能与很多化合物通过配位键发生相互作用,CA3与第2周期中的另一种元素的氢化物相互作用得到的化合物X是科学家潜心研究的一种储氢原料,X是乙烷的等电子体;加热X会缓慢释放H2,转变为化合物Y,Y是乙烯的等电子体。
 化合物CA3的分子空间构型为
化合物CA3的分子空间构型为 ______ ,X的结构式为 ______  必须标明配位键
必须标明配位键 。
。
 形成CA3物质的中心原子在X、Y分子中的杂化方式分别是
形成CA3物质的中心原子在X、Y分子中的杂化方式分别是 ___ ,Y分子中δ键和π键数目之比为 ____ 。
⑷E能与类卤素(SCN)2反应生成E(SCN)2,类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H—S—C N)的沸点低于异硫氰酸(H—N
N)的沸点低于异硫氰酸(H—N C
C S)的沸点,其原因是
S)的沸点,其原因是 ______ 。
⑴E的基态原子价电子排布图
⑵B、C、D的第一电离能由小到大的顺序为
 用元素符号表示
用元素符号表示
⑶CA3物质能与很多化合物通过配位键发生相互作用,CA3与第2周期中的另一种元素的氢化物相互作用得到的化合物X是科学家潜心研究的一种储氢原料,X是乙烷的等电子体;加热X会缓慢释放H2,转变为化合物Y,Y是乙烯的等电子体。
 化合物CA3的分子空间构型为
化合物CA3的分子空间构型为  必须标明配位键
必须标明配位键 。
。 形成CA3物质的中心原子在X、Y分子中的杂化方式分别是
形成CA3物质的中心原子在X、Y分子中的杂化方式分别是 ⑷E能与类卤素(SCN)2反应生成E(SCN)2,类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H—S—C
 N)的沸点低于异硫氰酸(H—N
N)的沸点低于异硫氰酸(H—N C
C S)的沸点,其原因是
S)的沸点,其原因是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如表所示:
(1)W在元素周期表中的位置是___________ ,属于___________ 区。
(2)X基态原子的电子排布图为___________ 。
(3)同一周期中与X相邻的共三种元素的第一电离能由小到大的顺序为___________ (用元素符号表示)。
(4)X的一种氢化物H2X2分子中极性键和非极性键数目之比为___________ 。
(5)W2+和W3+中更稳定的是___________ (用离子符号),用一个离子方程式证明___________ 。
| 元素 | 相关信息 |
| X | X的一种核素的质量数为18,中子数为10 |
| Y | Y与X同主族,且它的一种氧化物是导致酸雨的主要物质之一 |
| Z | Z的单质常温下为黄绿色气体 |
| W | W的基态原子核外有4个未成对电子 |
(2)X基态原子的电子排布图为
(3)同一周期中与X相邻的共三种元素的第一电离能由小到大的顺序为
(4)X的一种氢化物H2X2分子中极性键和非极性键数目之比为
(5)W2+和W3+中更稳定的是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】氰化钾是一种剧毒的物质,贮存和使用时必须注意安全。已知:KCN+H2O2=KOCN+H2O,回答下列问题:
(1)OCN-中所含三种元素的第一电离能从大到小的顺序为_________ (用元素符号表示,下同),电负性从大到小的顺序为__________ ,基态氮原子价电子排布图为__________________ 。
(2)H2O2中的共价键类型为_____ (填“σ键”或“π键”),其中氧原子的杂化轨道类型为__________ ;分子中4个原子______ (填“在”或“不在”)同一条直线下。
(1)OCN-中所含三种元素的第一电离能从大到小的顺序为
(2)H2O2中的共价键类型为
您最近一年使用:0次



