辉钼矿( )是最重要钼矿,它在130℃、高压氧条件下,跟苛性碱溶液发生反应,
)是最重要钼矿,它在130℃、高压氧条件下,跟苛性碱溶液发生反应,
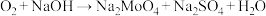 (未配平),下列说法正确的是
(未配平),下列说法正确的是
 )是最重要钼矿,它在130℃、高压氧条件下,跟苛性碱溶液发生反应,
)是最重要钼矿,它在130℃、高压氧条件下,跟苛性碱溶液发生反应,
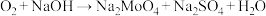 (未配平),下列说法正确的是
(未配平),下列说法正确的是A.上述反应中 是氧化剂, 是氧化剂, 是还原产物 是还原产物 |
B. 中Mo元素化合价为 中Mo元素化合价为 ;氧化性强于 ;氧化性强于 |
C.每生成  反应中转移 反应中转移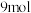  |
D.若通过原电池来实现上述反应,正极的电极反应为 |
更新时间:2023-08-21 09:07:42
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】重铬酸钾溶液中存在如下平衡: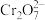 (橙色)+H2O
(橙色)+H2O 2H++2Cr
2H++2Cr (黄色)
(黄色)
①向2mL0.1mol•L-1K2Cr2O7溶液中滴入3滴6mol•L-1NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴6mol/LH2SO4,溶液由黄色变为橙色。②向2mL0.1mol•L-1酸化的K2Cr2O7溶液中滴入适量的(NH4)2Fe(SO4)2溶液,发生反应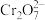 +14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O。
+14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O。
下列分析正确的是
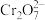 (橙色)+H2O
(橙色)+H2O 2H++2Cr
2H++2Cr (黄色)
(黄色)①向2mL0.1mol•L-1K2Cr2O7溶液中滴入3滴6mol•L-1NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴6mol/LH2SO4,溶液由黄色变为橙色。②向2mL0.1mol•L-1酸化的K2Cr2O7溶液中滴入适量的(NH4)2Fe(SO4)2溶液,发生反应
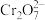 +14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O。
+14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O。下列分析正确的是
| A.实验①和②均能证明K2Cr2O7溶液中存在上述平衡 |
B.实验②能说明氧化性: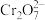 >Fe3+ >Fe3+ |
| C.实验②的反应中电子转移总数为6 |
D.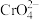 和Fe2+在酸性溶液中可以大量共存 和Fe2+在酸性溶液中可以大量共存 |
您最近一年使用:0次
多选题
|
适中
(0.64)
【推荐2】下列实验操作和对应的现象、结论都正确的是
| 选项 | 操 作 | 现 象 | 结 论 |
| A | 在滴有酚酞的Na2CO3溶液中加入BaC12溶液 | 红色褪去 | Na2CO3溶液中存在水解平衡 |
| B | 将某气体通入品红溶液中 | 品红溶液褪色 | 该气体一定是SO2 |
| C | 将铜板电路投入FeCl3溶液中 | 铜溶于FeCl3溶液 | 氧化性:Fe3+ > Cu2+ |
| D | 向NaCl溶液滴少量AgNO3溶液,再滴加少量NaI溶液 | 先有白色沉淀,后变成黄色沉淀 | Ksp(AgI) >Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐3】向200mL1.5mol∙L-lFeBr2溶液中逐渐通入Cl2,其中n(Fe2+)、n(Br-)随通入Cl2的物质的量n(Cl2)变化如图所示,下列说法错误的是
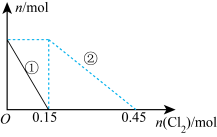

| A.①代表Fe2+,②代表Br- |
| B.还原性强弱:Br->Fe2+ |
| C.n(Cl2)=0.35mol时,溶液中c(Fe3+)=c(Br-) |
| D.n(Cl2)=0.45mol时,总的离子方程式为:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】以铁片和铜片为电极,以稀硫酸为电解质溶液组成的原电池,当导线中通过电子时,下列叙述正确的是
| A.铁片溶解1mol,铜片上析出1mol H2 |
| B.两极上溶解和析出的物质的量质量相等 |
| C.铁片溶解2g,铜片上析出1g H2 |
| D.铁片溶解1mol,硫酸消耗1mol |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】糕点包装中常用的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是( )
| A.脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| B.脱氧过程中铁做原电池正极,电极反应:Fe-3e-=Fe3+ |
| C.脱氧过程中碳做原电池正极,电极反应:2H2O+O2+4e-=4OH- |
| D.含有1.12 g铁粉的脱氧剂,理论上最多能吸收氧气336 mL(标准状况) |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】科学家近年发明了一种新型Zn-CO2水介质电池,电池示意图如图所示,电极为金属锌和选择性催化材料。放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
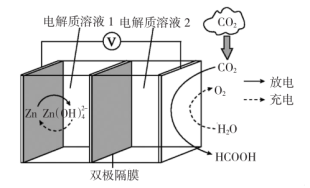
下列说法中错误的是

下列说法中错误的是
| A.放电时,负极反应为Zn+4OH--2e-=[Zn(OH)4]2- |
| B.放电时,1molCO2转化为HCOOH,转移的电子数为1mol |
| C.充电时,电池总反应为2[Zn(OH)4]2-=2Zn+O2↑+4OH-+2H2O |
| D.充电时,正极溶液中OH-浓度升高 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】最近我国科学家研制出一种可充电 双离子电池体系,其工作原理如图所示。
双离子电池体系,其工作原理如图所示。
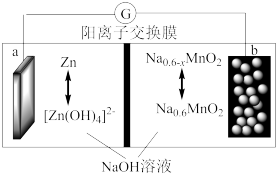
下列说法错误的是
 双离子电池体系,其工作原理如图所示。
双离子电池体系,其工作原理如图所示。
下列说法错误的是
A.充电时,阴极区溶液的 增大 增大 |
| B.因部分电能转化为热能,充电时通过的电量与锌的析出量无确定关系 |
C.放电时,每转移 电子,负极区电解质溶液质量减少4.6g 电子,负极区电解质溶液质量减少4.6g |
D.放电时,正极反应式为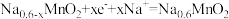 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、W为原子序数依次增大的前四周期元素,X与Z可以形成两种常见液态化合物,W与Z能形成多种化合物,其中之一为红棕色,常用来制作红色油漆或涂料,由Y、Z、W三种元素形成的化合物A的化学式为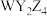 ,其结构如图所示。下列叙述错误的是
,其结构如图所示。下列叙述错误的是
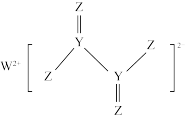
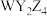 ,其结构如图所示。下列叙述错误的是
,其结构如图所示。下列叙述错误的是
| A.Y、Z的单质均存在同素异形体 |
B.W与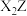 在一定条件下能发生置换反应生成红棕色化合物 在一定条件下能发生置换反应生成红棕色化合物 |
C. 化合物A与足量酸性高锰酸钾溶液完全反应转移电子数是 化合物A与足量酸性高锰酸钾溶液完全反应转移电子数是 |
| D.化合物A受热易分解,可产生两种气体,其中一种能使澄清石灰水变浑浊 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】食盐中的碘元素以碘酸钾(KIO3)形式存在,可根据反应:IO +5I-+6H+=3I2+3H2O验证食盐中存在IO
+5I-+6H+=3I2+3H2O验证食盐中存在IO ,根据上述反应,下列说法错误的是
,根据上述反应,下列说法错误的是
 +5I-+6H+=3I2+3H2O验证食盐中存在IO
+5I-+6H+=3I2+3H2O验证食盐中存在IO ,根据上述反应,下列说法错误的是
,根据上述反应,下列说法错误的是A.IO 作氧化剂,发生还原反应,1个IO 作氧化剂,发生还原反应,1个IO 得6个电子 得6个电子 |
| B.I2既是氧化产物又是还原产物 |
| C.烹饪时应该多加食醋和早加碘盐 |
| D.每生成3molI2转移电子的物质的量为5mol |
您最近一年使用:0次

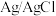 复合电极,b的电极反应式为
复合电极,b的电极反应式为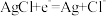 。下列说法正确的是
。下列说法正确的是

 由b极区向a极区迁移
由b极区向a极区迁移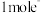 时,理论上a极区模拟海水的质量减少58.5g
时,理论上a极区模拟海水的质量减少58.5g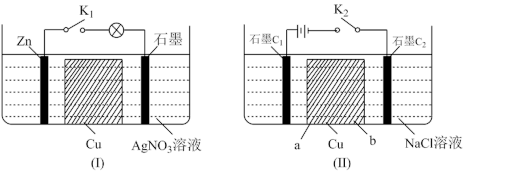
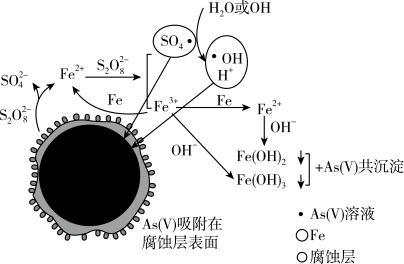
 氧化成Fe2+
氧化成Fe2+ ·+H2O = SO
·+H2O = SO +·OH+H+
+·OH+H+

