重铬酸钾溶液中存在如下平衡: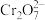 (橙色)+H2O
(橙色)+H2O 2H++2Cr
2H++2Cr (黄色)
(黄色)
①向2mL0.1mol•L-1K2Cr2O7溶液中滴入3滴6mol•L-1NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴6mol/LH2SO4,溶液由黄色变为橙色。②向2mL0.1mol•L-1酸化的K2Cr2O7溶液中滴入适量的(NH4)2Fe(SO4)2溶液,发生反应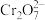 +14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O。
+14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O。
下列分析正确的是
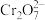 (橙色)+H2O
(橙色)+H2O 2H++2Cr
2H++2Cr (黄色)
(黄色)①向2mL0.1mol•L-1K2Cr2O7溶液中滴入3滴6mol•L-1NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴6mol/LH2SO4,溶液由黄色变为橙色。②向2mL0.1mol•L-1酸化的K2Cr2O7溶液中滴入适量的(NH4)2Fe(SO4)2溶液,发生反应
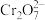 +14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O。
+14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O。下列分析正确的是
| A.实验①和②均能证明K2Cr2O7溶液中存在上述平衡 |
B.实验②能说明氧化性: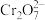 >Fe3+ >Fe3+ |
| C.实验②的反应中电子转移总数为6 |
D.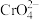 和Fe2+在酸性溶液中可以大量共存 和Fe2+在酸性溶液中可以大量共存 |
更新时间:2021-10-27 16:37:24
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】两种溶液各含有以下8种离子中的4种不同离子: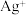 、
、 、
、 、
、 、
、 、
、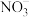 、
、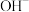 、
、 ,如将两种溶液按一定比例混合,沉淀后溶液无色且只含硝酸钠。下列选项中正确的是
,如将两种溶液按一定比例混合,沉淀后溶液无色且只含硝酸钠。下列选项中正确的是
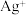 、
、 、
、 、
、 、
、 、
、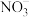 、
、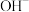 、
、 ,如将两种溶液按一定比例混合,沉淀后溶液无色且只含硝酸钠。下列选项中正确的是
,如将两种溶液按一定比例混合,沉淀后溶液无色且只含硝酸钠。下列选项中正确的是A. 和 和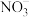 一定来自同一溶液 一定来自同一溶液 | B. 和 和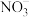 一定来自同一溶液 一定来自同一溶液 |
C. 和 和 一定来自不同溶液 一定来自不同溶液 | D. 和 和 一定来自不同溶液 一定来自不同溶液 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】在下列各溶液中,离子可能大量共存的是
| A.透明的溶液中:Cu2+、Fe3+、NO3-、、Cl- |
| B.使pH试纸变红的溶液中:NH4+、Na+、SO42-、Cl- |
| C.含有大量ClO—的溶液中:K+、H+、I-、SO32— |
| D.水电离产生的c(H+) =10—12mol·L—1的溶液中:Na+、Fe2+、SO42—、NO3- |
您最近一年使用:0次
【推荐1】已知反应:①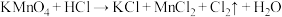
② 、
、
③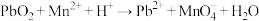 (方程式均未配平)。
(方程式均未配平)。
下列说法不正确的是
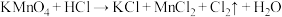
②
 、
、③
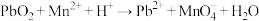 (方程式均未配平)。
(方程式均未配平)。下列说法不正确的是
A.反应③中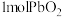 参加反应转移电子2mol 参加反应转移电子2mol |
B.反应①中氧化剂与参与反应的HCl的物质的量之比为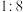 |
C.上述反应中,还原性由强到弱顺序: 、 、 、 、 |
D.反应①和②中消耗相同物质的量的 和 和 时,生成 时,生成 的物质的量之比为 的物质的量之比为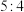 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】根据下表,下列叙述中正确的是
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | FeCl3 | ||
| ② | KMnO4 | H2O2 | H2SO4 | O2 | MnSO4 |
| ③ | KClO3 | HCl(浓) | Cl2 | Cl2 | |
| ④ | KMnO4 | HCl(浓) | Cl2 | MnCl2 |
| A.表中第①组反应的氧化产物一定有FeCl3(实为Fe3+) |
| B.氧化性比较:KMnO4>Cl2>Fe3+>Br2>Fe2+ |
| C.还原性比较:H2O2>Mn2+>Cl- |
| D.④的离子方程式配平后,H+的化学计量数为16 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向FeBr2溶液中通入适量Cl2,溶液由浅绿色变为黄色 | Cl2氧化性强于Br2 |
| B | 向H2O2溶液中滴入NaClO溶液,产生无色气体 | H2O2具有氧化性 |
| C | 向酸性含碘废水中加入淀粉溶液,然后滴入少量Na2SO3溶液,废水立刻变蓝色 | 该废水中可能含 |
| D | 向蔗糖中滴加少量浓硫酸,搅拌,蔗糖变黑,体积膨松,变成疏松多孔的海绵状 | 浓硫酸具有脱水性和强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】为防止废弃的硒单质(Se)造成环境污染,通常用浓硫酸将其转化成处理成二氧化硒(SeO2),再用KI溶液处理后回收Se。发生的反应为:①Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O、②SeO2+4KI+4HNO3=4KNO3+Se+2I2+2H2O。下列说法正确的是
| A.反应①中SO2是氧化产物,SeO2是还原产物 |
| B.反应②中KI是还原剂,HNO3是氧化剂 |
| C.反应②中,每生成0.6molI2转移1.2mole- |
| D.氧化性由强到弱的顺序是:H2SO4(浓)>SeO2>I2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】根据下列实验操作及现象所得出的结论或解释正确的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | FeCl3+3KSCN⇌Fe(SCN)3+3KCl在平衡体系中加入KCl晶体 | 溶液颜色不变 | 加入少量KCl晶体,不会影响该化学平衡 |
| B | 取相同大小、形状和质量的Cu粒分别投入稀硝酸和浓硝酸中 | Cu粒与浓硝酸反应更剧烈 | 实验目的是探究浓度对化学反应速率的影响 |
| C | 将20℃0.5mol·Lˉ1Na2CO3溶液加热到60℃,用传感器测定溶液pH | 溶液的pH逐渐减小 | Kw改变与水解平衡移动共同作用的结果 |
| D | 用pH试纸测得相同浓度的CH3COONa溶液、NaNO2溶液的pH | CH3COONa溶液pH约为9,NaNO2溶液的pH约为8 | CH3COOH的酸性比HNO2强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
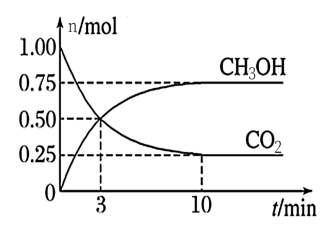
【推荐2】工业上可以用CO2来生产甲醇燃料。在体积为2 L的密闭容器中,充入l mol CO2和3 mol H2,一定条件下发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
 CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
CH3OH(g)+H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示。下列描述正确的是
| A.达到平衡时,H2的转化率为75% |
| B.3 min 时,CH3OH和CO2的浓度相等,达到了化学平衡状态 |
| C.反应进行到10 min后,向容器中再充入CO2,则CO2的转化率会增大 |
| D.反应开始到10 min,用CO2表示的反应速率为0.0375 mol·L-1·min-1 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】已知:[Co( H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2- 为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下:
 ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下: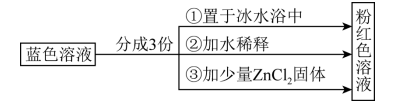
| A.由实验①可推知正反应为放热反应 |
| B.等物质的量的 [Co( H2O)6]2+和 [CoCl4]2-中σ键数之比为 9:2 |
| C.实验②是由于c(H2O)增大,导致平衡逆向移动 |
| D.由实验③可知配离子的稳定性:[ZnCl4]2->[CoCl4]2- |
您最近一年使用:0次

 、
、 、
、 、
、 、
、 、
、

 、
、 的物质的量之比为2:1
的物质的量之比为2:1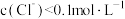
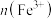 、
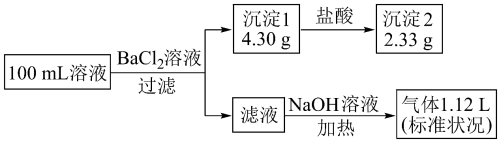
、 随通入
随通入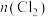 的变化如图所示,下列说法不正确的是
的变化如图所示,下列说法不正确的是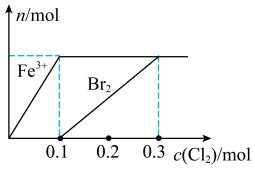
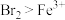
 时,溶液中的离子浓度为
时,溶液中的离子浓度为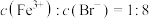
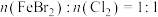 时,反应的离子方程式为:
时,反应的离子方程式为:


