H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
(1)平衡时CO2的浓度为_______ 。
(2)H2S的平衡转化率α1=_______ %,反应平衡常数K=_______ 。
 COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。(1)平衡时CO2的浓度为
(2)H2S的平衡转化率α1=
更新时间:2023-08-27 16:42:13
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】已知:A(g)+2B(g) 2C(g)ΔH<0。此反应的平衡常数表达式K=
2C(g)ΔH<0。此反应的平衡常数表达式K=__________ ,温度降低,K值会______ (增大、减小、不变),A的转化率_______ ,化学反应速率_____
 2C(g)ΔH<0。此反应的平衡常数表达式K=
2C(g)ΔH<0。此反应的平衡常数表达式K=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO 2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1) 已知该反应ΔS<0,在上述条件下反应能够自发进行,则反应的ΔH________ 0(填写“>”“<”或“=”)。
(2)前2 s内的平均反应速率v(N2)=________ 。
(3)在该温度下,反应的平衡常数表达式K=________ 。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是________ 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
 2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(10-4mol·L-1) | 10 | 4.5 | 2.5 | 1.5 | 1.0 | 1.0 |
| c(CO)/(10-3mol·L-1) | 36.0 | 30.5 | 28.5 | 27.5 | 27.0 | 27.0 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1) 已知该反应ΔS<0,在上述条件下反应能够自发进行,则反应的ΔH
(2)前2 s内的平均反应速率v(N2)=
(3)在该温度下,反应的平衡常数表达式K=
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】汽车尾气里含有的NO气体是由内燃机燃烧时产生的高温引起氮气和氧气反应所致:N2(g)+O2(g) 2NO(g) ΔH>0。已知该反应在2404℃时,平衡常数K=6.4×10−3。请回答下列问题。
2NO(g) ΔH>0。已知该反应在2404℃时,平衡常数K=6.4×10−3。请回答下列问题。
(1)该反应的平衡常数表达式为__ ,升高温度N2的转化率__ (填“变大”、“变小”或“不变”)。
(2)该温度下,向2L密闭容器中充入N2和O2各1mol,平衡时,N2的转化率是___ %(保留整数)。
(3)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10−1 mol∙L−1、4.0×10−2 mol∙L−1和3.0×10−3 mol∙L−1,此时反应___ (填“处于化学平衡状态”、“向正方向进行”或“向逆方向进行”),理由是__ 。
(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数___ (填“变大”、“变小”或“不变”)。
 2NO(g) ΔH>0。已知该反应在2404℃时,平衡常数K=6.4×10−3。请回答下列问题。
2NO(g) ΔH>0。已知该反应在2404℃时,平衡常数K=6.4×10−3。请回答下列问题。(1)该反应的平衡常数表达式为
(2)该温度下,向2L密闭容器中充入N2和O2各1mol,平衡时,N2的转化率是
(3)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10−1 mol∙L−1、4.0×10−2 mol∙L−1和3.0×10−3 mol∙L−1,此时反应
(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】完成下列问题。
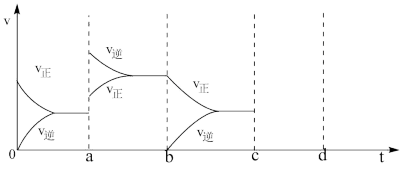
(1)如图表示在密闭容器中反应:2SO2(g)+O2(g) 2SO3(g)达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b过程中改变的条件可能是
2SO3(g)达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b过程中改变的条件可能是___________ ;bc过程中改变的条件可能是___________ ;若增大压强时,反应速度变化情况画在c~d处___________ 。
(2)在一定温度下,10L密闭容器中加入5molSO2、4.5molO2,经10min后反应达平衡时有3molSO2发生了反应。试填写下列空格:
①SO2的转化率为___________ 。
②用SO2表示该反应的平均反应速率为___________ 。
③平衡时体系中SO3的百分含量(体积分数)为___________ 。
④平衡常数K为___________ 。
(1)如图表示在密闭容器中反应:2SO2(g)+O2(g)
 2SO3(g)达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b过程中改变的条件可能是
2SO3(g)达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b过程中改变的条件可能是
(2)在一定温度下,10L密闭容器中加入5molSO2、4.5molO2,经10min后反应达平衡时有3molSO2发生了反应。试填写下列空格:
①SO2的转化率为
②用SO2表示该反应的平均反应速率为
③平衡时体系中SO3的百分含量(体积分数)为
④平衡常数K为
您最近一年使用:0次
填空题
|
较易
(0.85)
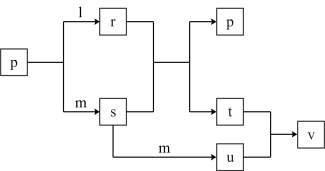
【推荐2】短周期主族元素X、Y、Z的原子序数依次增大,X的某种同位素不含中子,Y与Z同族,Z的原子序数是Y的两倍,l、m、p分别为元素X、Y、Z对应的单质,r、s、t、u、v为X、Y、Z形成的二元或三元化合物,这些物质有如下图所示转化关系(反应条件及部分产物已略去),回答下列问题:
(1)r具有_________ 气味, r与s生成p和t的化学方程式为__________ 。
(2)r______ (填“能”或“不能”)用v的浓溶液干燥,用化学方程式解释其原因_________ 。
(3)用r、空气和KOH溶液可以组成燃料电池,生成Z元素的+4价含氧酸正盐和水。电池工作时负极反应为_________ (用离子方程式表示)。
(4)将10 mol s、5 mol m充入10 L的恒容密闭容器,在500 K条件下生成u气体,平衡时,反应物与生成物的物质的量相等,则s的平衡转化率为_________ ,该反应的平衡常数为___________ 。

(1)r具有
(2)r
(3)用r、空气和KOH溶液可以组成燃料电池,生成Z元素的+4价含氧酸正盐和水。电池工作时负极反应为
(4)将10 mol s、5 mol m充入10 L的恒容密闭容器,在500 K条件下生成u气体,平衡时,反应物与生成物的物质的量相等,则s的平衡转化率为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
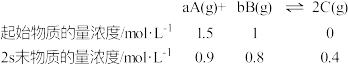
请回答下列问题。
(1)该可逆反应的化学方程式可表示为_______ 。
(2)用物质B来表示0~2s的平均反应速率为_______ 。
(3)从反应开始到2s末,A的转化率为_______ 。
(4)下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是_______ (填序号)。
A.vB(消耗)=vC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.vA:vB:vC=3:1:2
E.容器内气体C的物质的量分数保持不变
(5)若平衡后改变温度,使得容器中气体的平均摩尔质量变大,则反应向_______ (填“反应物”或“生成物”)的方向移动。
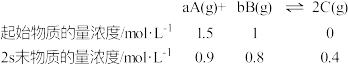
请回答下列问题。
(1)该可逆反应的化学方程式可表示为
(2)用物质B来表示0~2s的平均反应速率为
(3)从反应开始到2s末,A的转化率为
(4)下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
A.vB(消耗)=vC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.vA:vB:vC=3:1:2
E.容器内气体C的物质的量分数保持不变
(5)若平衡后改变温度,使得容器中气体的平均摩尔质量变大,则反应向
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】I. 下面列出了几组物质,请将物质的合适序号填写在空格上。
同位素___________ ;同系物____________ ;同分异构体___________ 。
①金刚石与石墨; ②D与T; ③12C和13C; ④O2与O3;
⑤CH4和CH3CH2CH3; ⑥CH2=CHCH3和CH2=CH2;
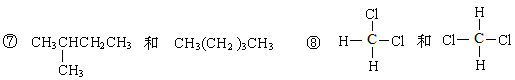
II.篮烷分子的键线式如图所示,试回答:
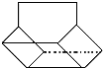
写出篮烷分子的化学式____________ ;篮烷分子的一氯取代物的种数为_______ 种。
III.在一定温度下,体积为2 L的密闭容器中,NO2和N2O4之间发生反应:2NO2 (g) N2O4(g) ,如图所示。
N2O4(g) ,如图所示。
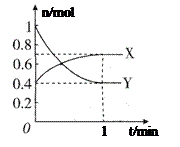
(1)曲线_____________ (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。
(2)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=18 mol/(L·min),乙中v(N2O4)=0.2 mol/(L·s),则______________ 中反应更快。
(3)在0到1 min中内用X表示该反应的速率是________ ,该反应达限度时,Y的转化率是_________ ,反应开始时与反应达平衡状态时的压强之比为______ 。
(4)若反应达平衡状态时再升高温度,容器内混合气体颜色加深,则正反应是_________ 反应(填“放热”或“吸热”。已知:降温有利于放热反应进行)。
同位素
①金刚石与石墨; ②D与T; ③12C和13C; ④O2与O3;
⑤CH4和CH3CH2CH3; ⑥CH2=CHCH3和CH2=CH2;
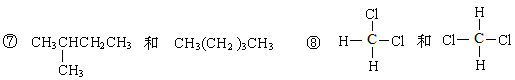
II.篮烷分子的键线式如图所示,试回答:

写出篮烷分子的化学式
III.在一定温度下,体积为2 L的密闭容器中,NO2和N2O4之间发生反应:2NO2 (g)
 N2O4(g) ,如图所示。
N2O4(g) ,如图所示。
(1)曲线
(2)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=18 mol/(L·min),乙中v(N2O4)=0.2 mol/(L·s),则
(3)在0到1 min中内用X表示该反应的速率是
(4)若反应达平衡状态时再升高温度,容器内混合气体颜色加深,则正反应是
您最近一年使用:0次




