为探究锌与0.1 mol/L稀硫酸的反应速率[以υ(H2)表示],对反应物作出如下改变。下列判断正确的是
| A.加入NH4HSO4固体,υ(H2)不变 |
| B.加入少量水,υ(H2)减小 |
| C.把0.1 mol/L稀硫酸改为0.2 mol/L盐酸,υ(H2)增大 |
| D.把稀硫酸改为98%的浓硫酸,υ(H2)增大 |
更新时间:2023-08-27 10:28:29
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列有关实验说法不正确的是
| A.用硫代硫酸钠和稀硫酸反应来研究不同温度对化学反应速率的影响时,通过观察气体放出的快慢来判断化学反应速率的快慢。 |
| B.用稀硫酸和锌粒制取H2时,加几滴CuSO4溶液以加快反应速率 |
| C.用容量瓶配制0.1mol/LNaOH溶液,定容时俯视刻度线,所配溶液浓度偏大 |
| D.测定中和反应的反应热是,将碱缓慢倒入酸中,所测出放出的热量偏小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】工业上通过熔融状态下的反应 来制取金属钾,反应温度通常为850℃,有关数据如下表所示,下列说法错误的是
来制取金属钾,反应温度通常为850℃,有关数据如下表所示,下列说法错误的是
 来制取金属钾,反应温度通常为850℃,有关数据如下表所示,下列说法错误的是
来制取金属钾,反应温度通常为850℃,有关数据如下表所示,下列说法错误的是| Na | K | NaCl | KCl | |
熔点/ | 97.8 | 63.7 | 801.0 | 770 |
沸点/ | 883 | 774 | 1413 | 1500 |
| A.钾比钠活泼 |
B.该反应的 |
| C.该反应的温度可低于774℃ |
D.850℃条件下该反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】一定量的盐酸和过量锌粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可以向盐酸中加入适量的
| A.NaOH固体 | B.水 | C.CuSO4固体 | D.硝酸钠溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】氮元素的化合物种类繁多,请结合以下工业制硝酸的原理示意图判断下列说法不正确的是
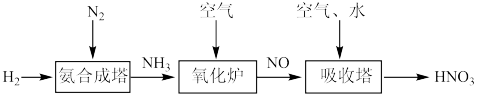

| A.氨合成塔中使用催化剂是为了提高合成NH3的反应速率 |
| B.氧化炉中NH3被氧化 |
| C.吸收塔中1 mol NO完全转化成HNO3电子转移3NA |
| D.此路线是雷雨固氮合成硝酸的主要途径 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间内(t)产生氢气体积(V)的数据,根据数据绘制如图,则曲线a、b、c、d所对应的实验组别可能是
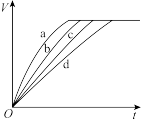

| 组别 | c(HCl)/(mol·L-1) | 温度/℃ | 铁的状态 |
| ① | 2.0 | 25 | 块状 |
| ② | 2.5 | 30 | 块状 |
| ③ | 2.5 | 50 | 粉末状 |
| ④ | 2.5 | 30 | 粉末状 |
| A.④-③-②-① | B.①-②-③-④ |
| C.③-④-②-① | D.①-②-④-③ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列实验内容能达到相应实验目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 向1mL  ,溶液中加入5mL ,溶液中加入5mL  溶液,充分反应后,加入2mL苯,充分振荡、静置,分液后将水层分装于两支小试管中,向其中一支小试管中滴加5~6滴15%的 溶液,充分反应后,加入2mL苯,充分振荡、静置,分液后将水层分装于两支小试管中,向其中一支小试管中滴加5~6滴15%的 溶液,观察并比较两支试管中溶液的颜色 溶液,观察并比较两支试管中溶液的颜色 | 证明 与 与 之间的反应属于可逆反应 之间的反应属于可逆反应 |
| B | 室温时,将等体积、等物质的量浓度的 、 、 ,溶液分别加入等体积的30%的 ,溶液分别加入等体积的30%的 溶液中,观察并比较两支试管中气泡产生的快慢 溶液中,观察并比较两支试管中气泡产生的快慢 | 探究 、 、 催化效果的优劣 催化效果的优劣 |
| C | 取两支试管,分别加入5mL4%、5mL12%的 溶液,向其中一支试管中加入少量 溶液,向其中一支试管中加入少量 粉末,观察并比较两支试管中气泡产生的快慢 粉末,观察并比较两支试管中气泡产生的快慢 | 探究浓度对反应速率的影响 |
| D | 将相同体积相同浓度的稀硫酸分别加入两支试管中,再向两支试管中分别加入不同体积、等浓度的 溶液,将两支试管分别放入盛有等温等量的热水的烧杯中,观察并比较两支试管中出现浑浊现象的快慢 溶液,将两支试管分别放入盛有等温等量的热水的烧杯中,观察并比较两支试管中出现浑浊现象的快慢 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】体积10 mL浓度为1 mol·L-1的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成量的是
| A.CH3COONa | B.KOH溶液 | C.几滴CuSO4溶液 | D.NaNO3溶液 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列措施不能改变相应化学反应速率的是
| A.在铁制品表面刷油漆——铁的腐蚀速率 | B.高炉炼铁增加炉高——CO的反应速率 |
| C.食物放在冰箱中储存——食物的腐败速率 | D.烧煤时用煤粉代替煤块——煤的燃烧速率 |
您最近一年使用:0次

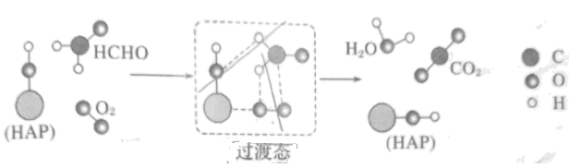
 CO2+H2O
CO2+H2O HBr+H的能量对反应历程的示意图甲进行判断,下列叙述中不正确的是
HBr+H的能量对反应历程的示意图甲进行判断,下列叙述中不正确的是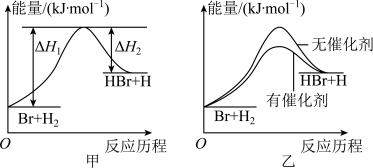
 与稀盐酸反应,加入NaCl溶液,不会改变反应速率
与稀盐酸反应,加入NaCl溶液,不会改变反应速率 溶液与
溶液与 溶液反应,加入KCl固体,将加快反应速率
溶液反应,加入KCl固体,将加快反应速率 ,改用98%的浓硫酸将加快
,改用98%的浓硫酸将加快

