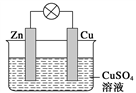
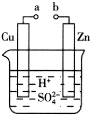
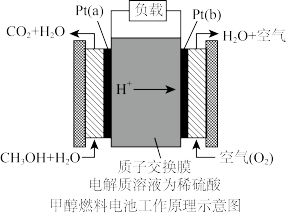
科学家预言,燃料电池将是21世纪获得电能的重要途径。近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过。其工作原理的示意图如图:
请回答下列问题:
(1)Pt(a)电极是电池的________ 极,电极反应式为_______ ;Pt(b)电极发生_______ (填“氧化”或“还原”)反应,电极反应式为________ 。
(2)电池的总反应方程式为_________ 。
(3)如果该电池工作时电路中通过2mol电子,则消耗的CH3OH有________ mol。
(4)使用该燃料电池的另一个好处是________ 。

请回答下列问题:
(1)Pt(a)电极是电池的
(2)电池的总反应方程式为
(3)如果该电池工作时电路中通过2mol电子,则消耗的CH3OH有
(4)使用该燃料电池的另一个好处是
23-24高二上·全国·课时练习 查看更多[1]
更新时间:2023-09-21 12:09:55
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)写出CH4和Cl2在光照的条件下生成CH3Cl的化学反应方程式___ 。
(2)如图原电池中氢离子流向___ 极(填“锌”或“铜”),正极电极反应式___ ,负极电极反应式___ 。
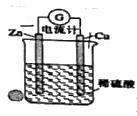
(2)如图原电池中氢离子流向

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】实验小组探究铝片做电极材料时的原电池反应,设计下表中装置进行实验并记录。
【实验1】
(1)实验1中,电解质溶液为盐酸,铝条做原电池的___________ 极
【实验2】
将实验1中的电解质溶液换为NaOH溶液进行实验2。
(2)该小组同学认为,此时原电池的总反应为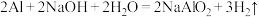 ,据此推测应该出现的实验现象为
,据此推测应该出现的实验现象为___________
实验2实际获得的现象如下:
(3)ⅰ中铝条表面放电的物质足溶解在溶液中的 ,则该电极反应式为
,则该电极反应式为___________
(4)ⅱ中“电流计指针逐渐向零刻度恢复”的原因是___________
【实验3和实验4】
为了排除Mg条的干扰,同学们重新设计装置并进行实验3和实验4,获得的实验现象如下:
(5)根据实验3和实验4可获得的正确推论是___________(填字母序号)
(6)由实验1~实验4可推知,铝片做电极材料时的原电池反应与___________ 等因素有关
【实验1】
| 装置 | 实验现象 |
 | 左侧装置电流计指针向右偏转,灯泡亮 右侧装置电流计指针向右偏转,镁条、铝条表面产生无色气泡 |
【实验2】
将实验1中的电解质溶液换为NaOH溶液进行实验2。
(2)该小组同学认为,此时原电池的总反应为
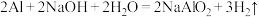 ,据此推测应该出现的实验现象为
,据此推测应该出现的实验现象为实验2实际获得的现象如下:
| 装置 | 实验现象 |
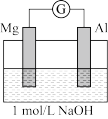 | ⅰ.电流计指针迅速向右偏转,镁条表面无气泡,铝条表面有气泡 ⅱ.电流计指针逐渐向零刻度恢复,经零刻度后继续向左偏转。镁条表面开始时无明显现象,一段时间后有少量气泡逸出,铝条表面持续有气泡逸出 |
 ,则该电极反应式为
,则该电极反应式为(4)ⅱ中“电流计指针逐渐向零刻度恢复”的原因是
【实验3和实验4】
为了排除Mg条的干扰,同学们重新设计装置并进行实验3和实验4,获得的实验现象如下:
| 编号 | 装置 | 实验现象 |
| 实验3 | 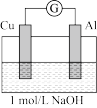 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象;约10分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
| 实验4 | 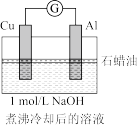 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象;约3分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
A.上述两装置中,开始时铜片表面得电子的物质是 |
| B.铜片表面开始产生气泡的时间长短与溶液中溶解氧的多少有关 |
C.铜片表面产生的气泡为 |
D.由“铝条表面气泡略有减少”能推测 在铜片表面得电子 在铜片表面得电子 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】依据氧化还原反应2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。
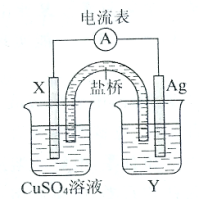
请回答下列问题:
(1)电极X的材料是_________________ ;电解质溶液Y是_________________ 。
(2)银电极为电池的_________________ 极,发生的电极反应为__________________ 。X电极上发生的电极反应为___________ 。外电路中的电子是从_________________ 极流向___ 极。
(3)此盐桥内为饱和KCl溶液,盐桥是通过_________________ 移动来导电的。在工作时,K+移向________________ 填“正极区”或“负极区”,下同),Cl-移向_________________ 。

请回答下列问题:
(1)电极X的材料是
(2)银电极为电池的
(3)此盐桥内为饱和KCl溶液,盐桥是通过
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】锂锰电池是常用的一次电池。该电池反应原理如图所示,其中电解质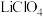 ,溶于混合有机溶剂中,
,溶于混合有机溶剂中, 通过电解质迁移入
通过电解质迁移入 晶格中,生成
晶格中,生成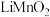 。回答下列问题:
。回答下列问题:
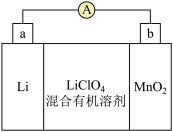
(1)负极的电极反应式为_______ 。
(2)正极的电极反应式为_______ 。
(3) 向
向_______ 极移动(填“a”或“b”)
(4)是否可用水代替电池中的混合有机溶剂?_______ (填“是”或“否”),原因是_______ 。
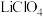 ,溶于混合有机溶剂中,
,溶于混合有机溶剂中, 通过电解质迁移入
通过电解质迁移入 晶格中,生成
晶格中,生成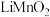 。回答下列问题:
。回答下列问题:
(1)负极的电极反应式为
(2)正极的电极反应式为
(3)
 向
向(4)是否可用水代替电池中的混合有机溶剂?
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】原电池的生活示例——水果电池
(1)水果电池中,水果的作用是_______ 。
(2)水果电池中,选择电极材料时应注意两电极不能相同,其中有一电极为活泼金属如Al、Fe等,另一电极可以是Cu片或_______ 等。
(3)原电池实验
(1)水果电池中,水果的作用是
(2)水果电池中,选择电极材料时应注意两电极不能相同,其中有一电极为活泼金属如Al、Fe等,另一电极可以是Cu片或
(3)原电池实验
| 电极材料 | 实验现象 | 解释 |
| 锌片、铜片 | 锌、铜、稀硫酸构成原电池, | |
| 锌片、石墨棒 | 锌、石墨、稀硫酸构成原电池, | |
| 铜片、石墨棒 | 铜片、石墨棒表面均无明显现象,电流表指针 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。在101 kPa下,1 g氢气完全燃烧生成液态水放出142.9 kJ的热量。
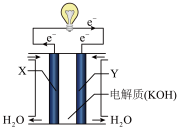
(1)请写出表示氢气燃烧热的热化学方程式__________________ 。
(2)将上述反应设计成下图所示的原电池,其中Y为________ 极(填“正”或“负”),该极电极反应式为___________________ 。

(1)请写出表示氢气燃烧热的热化学方程式
(2)将上述反应设计成下图所示的原电池,其中Y为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】氮氧化物(NOx)是硝酸工业和汽车尾气产生的主要污染物之一,通过气体传感器可以测定其含量。
(1)利用催化技术可将汽车尾气中的NO、CO转化为无污染的CO2和N2,反应的化学方程催化剂式为2NO(g)+2CO(g) N2(g)+2CO2(g)。该反应过程中的能量变化如图1所示,则该反应是
N2(g)+2CO2(g)。该反应过程中的能量变化如图1所示,则该反应是_________ (填“放热反应”或“吸热反应”),反应中断开反应物中化学键吸收的总能量_________ (填“大于”或“小于”)形成生成物中化学键放出的总能量。

(2)为了测定汽车尾气催化转化反应的反应速率,某温度下在恒容密闭容器中用气体传感器测得不同时间时NO浓度的变化如图2所示。

①0~2s内的平均反应速率v(CO2)=_________ 。
②该条件下,NO的平衡转化率为_________ 。
③下列有关上述反应的说法正确的是_________ (填字母)。
A.断裂N≡N键与形成C=O键数目之比为1∶2时,该反应达到平衡
B.消耗2molNO(g)的同时生成2molCO(g)时,该反应达到平衡
C.其他条件不变,缩小容器的体积,反应速率加快
(3)通过NO传感器可监测NO的含量,其工作原理如图3所示。
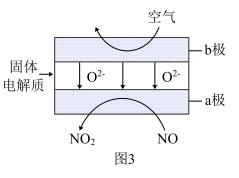
①a极是_________ (填“负极”或“正极”),发生的是_________ 反应(填“氧化”或“还原”)。
②工作时,a极的电极反应式是_________ 。
③每消耗标准状况下4.48LNO,理论上外电路中通过电子的物质的量是_________ 。
(1)利用催化技术可将汽车尾气中的NO、CO转化为无污染的CO2和N2,反应的化学方程催化剂式为2NO(g)+2CO(g)
 N2(g)+2CO2(g)。该反应过程中的能量变化如图1所示,则该反应是
N2(g)+2CO2(g)。该反应过程中的能量变化如图1所示,则该反应是
(2)为了测定汽车尾气催化转化反应的反应速率,某温度下在恒容密闭容器中用气体传感器测得不同时间时NO浓度的变化如图2所示。

①0~2s内的平均反应速率v(CO2)=
②该条件下,NO的平衡转化率为
③下列有关上述反应的说法正确的是
A.断裂N≡N键与形成C=O键数目之比为1∶2时,该反应达到平衡
B.消耗2molNO(g)的同时生成2molCO(g)时,该反应达到平衡
C.其他条件不变,缩小容器的体积,反应速率加快
(3)通过NO传感器可监测NO的含量,其工作原理如图3所示。

①a极是
②工作时,a极的电极反应式是
③每消耗标准状况下4.48LNO,理论上外电路中通过电子的物质的量是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】观察“简易氢氧燃料电池的实验”思考完成以下问题:
①简易氢氧燃料电池是如何将化学能转化成电能的?
②组装电池需要满足哪些基本条件?
氢氧燃料电池中发生的反应为:_______ 。氢分子中的氢原子在石墨电极上_______ 电子,氢气作为电池的_______ ;氧气分子中的氧原子在石墨电极上_______ 电子,氧气作为电池的_______ ;稀硫酸中存在的自由移动的离子起到_______ 的作用,导线起到_______ 的作用。简易氢氧燃料电池能够给用电器提供电势差,是由于在两个石墨电极上有_______ 不同的物质-氢气和氧气。
①简易氢氧燃料电池是如何将化学能转化成电能的?
②组装电池需要满足哪些基本条件?
氢氧燃料电池中发生的反应为:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】回答下列问题:
(1)氢氧燃料电池在电解质溶液为KOH溶液时,写出氢氧燃料电池工作时的负极电极反应式:_____
(2)在浓硝酸中放入铜片:开始反应的化学方程式为_______ ;若铜有剩余,则反应将要结束时的化学方程式_______ 。
(3)标准状状况下,排空法收集氯化氢气体,做喷泉实验时,如果气体没有溢出,实验完成时所得溶液的物质的量浓度为_______ mol/L(保留两位有效数字)
(4)SiO2在自然界中广泛存在,它是制备现代通讯材料_______ (写该材料名称)的主要原料。
(1)氢氧燃料电池在电解质溶液为KOH溶液时,写出氢氧燃料电池工作时的负极电极反应式:
(2)在浓硝酸中放入铜片:开始反应的化学方程式为
(3)标准状状况下,排空法收集氯化氢气体,做喷泉实验时,如果气体没有溢出,实验完成时所得溶液的物质的量浓度为
(4)SiO2在自然界中广泛存在,它是制备现代通讯材料
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】如图为原电池装置示意图。

请回答下列问题:
(1)若A为Zn片,B为石墨棒,电解质溶液为稀硫酸,则A电极是原电池的___ 极,写出正极的电极反应式:___ 。
(2)若A为铜片,B为银片,电解质溶液为AgNO3溶液,则银片为___ (填“正”或“负”)极,写出电极反应式:负极___ ,正极___ 。
(3)若A、B均为铂片,电解质溶液为KOH溶液,分别从A、B两极通H2、O2,该电池为氢氧燃烧电池,则其负极的电极反应式为___ 。

请回答下列问题:
(1)若A为Zn片,B为石墨棒,电解质溶液为稀硫酸,则A电极是原电池的
(2)若A为铜片,B为银片,电解质溶液为AgNO3溶液,则银片为
(3)若A、B均为铂片,电解质溶液为KOH溶液,分别从A、B两极通H2、O2,该电池为氢氧燃烧电池,则其负极的电极反应式为
您最近一年使用:0次