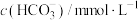银及其化合物在催化与电化学等领域中具有重要应用。
(1)在银催化下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)。根据图所示,回答下列问题:

①中间体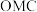 生成吸附态
生成吸附态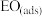 的活化能为
的活化能为_______  。
。
②由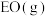 生成
生成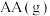 的热化学方程式为
的热化学方程式为_______ 。
(2)一定条件下,银催化剂表面上存在反应: ,该反应平衡压强
,该反应平衡压强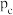 与温度
与温度 的关系如下:
的关系如下:
①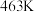 时的平衡常数
时的平衡常数
_______ 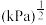 。
。
②起始状态Ⅰ中有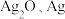 和
和 ,经下列过程达到各平衡状态:
,经下列过程达到各平衡状态:

已知状态Ⅰ和Ⅲ的固体质量相等,下列叙述正确的是_______ (填字母)。
A.从Ⅰ到Ⅱ的过程
B.
C.平衡常数: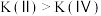
D.若体积 ,则
,则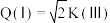
E.逆反应的速率: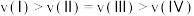
③某温度下,向恒容容器中加入 ,分解过程中反应速率
,分解过程中反应速率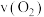 与压强
与压强 的关系为
的关系为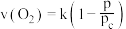 ,k为速率常数(定温下为常数)。当固体质量减少
,k为速率常数(定温下为常数)。当固体质量减少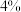 时,逆反应速率最大。若转化率为
时,逆反应速率最大。若转化率为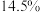 ,则
,则
_______ (用 表示)。
表示)。
(3) 可用作固体离子导体,能通过加热
可用作固体离子导体,能通过加热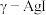 制得。上述两种晶体的晶胞示意图如图所示(为了简化,只画出了碘离子在晶胞中的位置)。
制得。上述两种晶体的晶胞示意图如图所示(为了简化,只画出了碘离子在晶胞中的位置)。

①测定晶体结构最常用的仪器是_______ (填字母)。
A.质谱仪 B.红外光谱仪 C.核磁共振仪 D. 射线衍射仪
射线衍射仪
②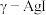 与
与 晶胞的体积之比为
晶胞的体积之比为_______ 。
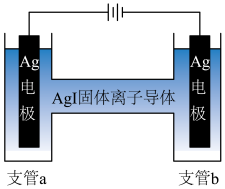
③测定 中导电离子类型的实验装置如图所示。实验测得支管a中
中导电离子类型的实验装置如图所示。实验测得支管a中 质量不变,可判定导电离子是
质量不变,可判定导电离子是 而不是
而不是 ,依据是
,依据是_______ 。
(1)在银催化下,乙烯与氧气反应生成环氧乙烷(EO)和乙醛(AA)。根据图所示,回答下列问题:

①中间体
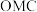 生成吸附态
生成吸附态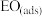 的活化能为
的活化能为 。
。②由
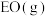 生成
生成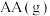 的热化学方程式为
的热化学方程式为(2)一定条件下,银催化剂表面上存在反应:
 ,该反应平衡压强
,该反应平衡压强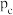 与温度
与温度 的关系如下:
的关系如下: | 401 | 443 | 463 |
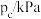 | 10 | 51 | 100 |
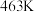 时的平衡常数
时的平衡常数
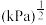 。
。②起始状态Ⅰ中有
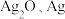 和
和 ,经下列过程达到各平衡状态:
,经下列过程达到各平衡状态:
已知状态Ⅰ和Ⅲ的固体质量相等,下列叙述正确的是
A.从Ⅰ到Ⅱ的过程

B.

C.平衡常数:
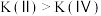
D.若体积
 ,则
,则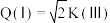
E.逆反应的速率:
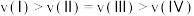
③某温度下,向恒容容器中加入
 ,分解过程中反应速率
,分解过程中反应速率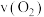 与压强
与压强 的关系为
的关系为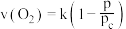 ,k为速率常数(定温下为常数)。当固体质量减少
,k为速率常数(定温下为常数)。当固体质量减少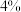 时,逆反应速率最大。若转化率为
时,逆反应速率最大。若转化率为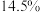 ,则
,则
 表示)。
表示)。(3)
 可用作固体离子导体,能通过加热
可用作固体离子导体,能通过加热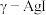 制得。上述两种晶体的晶胞示意图如图所示(为了简化,只画出了碘离子在晶胞中的位置)。
制得。上述两种晶体的晶胞示意图如图所示(为了简化,只画出了碘离子在晶胞中的位置)。
①测定晶体结构最常用的仪器是
A.质谱仪 B.红外光谱仪 C.核磁共振仪 D.
 射线衍射仪
射线衍射仪②
 与
与 晶胞的体积之比为
晶胞的体积之比为③测定
 中导电离子类型的实验装置如图所示。实验测得支管a中
中导电离子类型的实验装置如图所示。实验测得支管a中 质量不变,可判定导电离子是
质量不变,可判定导电离子是 而不是
而不是 ,依据是
,依据是
更新时间:2023-09-28 11:12:20
|
相似题推荐
解答题-原理综合题
|
困难
(0.15)
解题方法
【推荐1】甲烷的综合利用受到环境和能源领域的关注,是研究的重要课题。
(1)已知下列热化学方程式:
反应i:CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H1=-164.4kJ/mol
反应ii:CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41.5kJ/mol
反应iii:CH4(g)+H2O(g)=CO(g)+3H2(g) △H3
则反应iii的△H3=_______ kJ/mol,该反应在_______ (填“高温”“低温”或“任意温度”)下能自发进行。
(2)对于反应iii机理,可认为该反应分两步进行。
第一步:CH4催化裂解生成H2和碳(或碳氢物种),其中碳(或碳氢物种)吸附在催化剂上;第二步:碳(或碳氢物种)和H2O反应生成CO和H2。反应过程和能量变化图如下:

整个过程中决速的步骤是_______ (填Ⅰ或Ⅱ),其原因是_______ 。
(3)在体积都为2L的多个恒容密闭容器中,分别充入1molCO2和4molH2发生上述反应i(忽略反应ii和iii),在不同温度下反应相同时间,测得lgk(lgk正或lgk逆)、H2转化率与温度关系如图所示。已知该反应的速率方程为v正=k正c(CO2)∙c4(H2),v逆=k逆c(CH4)c2(H2O),其中、k正、k逆为速率常数,只受温度影响。
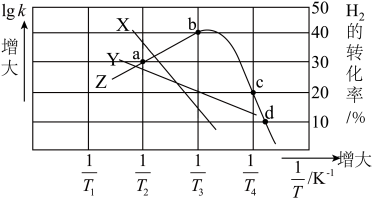
①代表lgk逆曲线的是_______ (填“X”或“Y”)。
②Z曲线上表示一定未达到化学平衡状态的点是_______ 。
③假设T,温度下经过30s反应达到a点状态,H2的平均反应速率为_______ ,该温度下平衡常数计算式为_______ 。
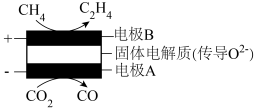
(4)利用某电化学装置可实现CH4和CO2的耦合转化,其原理如图所示。转化过程中阳极反应式为_______ 。
(1)已知下列热化学方程式:
反应i:CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H1=-164.4kJ/mol
反应ii:CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41.5kJ/mol
反应iii:CH4(g)+H2O(g)=CO(g)+3H2(g) △H3
则反应iii的△H3=
(2)对于反应iii机理,可认为该反应分两步进行。
第一步:CH4催化裂解生成H2和碳(或碳氢物种),其中碳(或碳氢物种)吸附在催化剂上;第二步:碳(或碳氢物种)和H2O反应生成CO和H2。反应过程和能量变化图如下:

整个过程中决速的步骤是
(3)在体积都为2L的多个恒容密闭容器中,分别充入1molCO2和4molH2发生上述反应i(忽略反应ii和iii),在不同温度下反应相同时间,测得lgk(lgk正或lgk逆)、H2转化率与温度关系如图所示。已知该反应的速率方程为v正=k正c(CO2)∙c4(H2),v逆=k逆c(CH4)c2(H2O),其中、k正、k逆为速率常数,只受温度影响。

①代表lgk逆曲线的是
②Z曲线上表示一定未达到化学平衡状态的点是
③假设T,温度下经过30s反应达到a点状态,H2的平均反应速率为
(4)利用某电化学装置可实现CH4和CO2的耦合转化,其原理如图所示。转化过程中阳极反应式为

您最近半年使用:0次
解答题-原理综合题
|
困难
(0.15)
名校
解题方法
【推荐2】研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼(C2H8N2)。
已知:①C2H8N2(l)+4O2(g)=2CO2(g)+N2(g)+4H2O(l) ΔH1=-2765.0kJ/mol
②2O2(g) +N2(g)=N2O4(l) ΔH2=-19.5kJ/mol
③H2O(g)= H2O(l) ΔH3=-44.0kJ/mol
则C2H8N2(1)+2N2O4(1)=3N2(g)+2CO2(g)+4H2O(g)的ΔH为_______ 。
(2)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步:I2(g)→2I(g)(快反应)
第二步:I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步:IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是_______
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=-746.8kJ-mol-1。实验测得:v正=k正·p2(NO)·p2(CO),v逆=k逆·p(N2)·p2(CO2)。其中k正、k逆分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=物质的量分数x总压)。
①达到平衡后,仅升高温度,k正增大的倍数_______ (填“大于”“小于”或“等于”)k逆增大的倍数。
②一定温度下在刚性密闭容器中充入CO、NO和N2物质的量之比为2:2:1,压强为p0kPa。达平衡时压强为0.9p0kPa,则
_______ 。
(4)我国科技人员计算了在一定温度范围内下列反应的平衡常数Kp:
①3N2H4(1)=4NH3(g)+N2(g) ΔH1 Kp1
②4NH3(g)=2N2(g)+6H2(g) ΔH2 Kp2
绘制pKp1-T和pKp2-T的线性关系图如图所示:(已知:pKp=-1gKp)
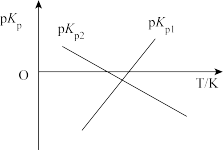
①由图可知,ΔH1_______ 0(填“>”或“<”)
②反应3N2H4(1)=3N2(g)+6H2(g)的K=_______ (用Kp1、Kp2表示);该反应的ΔH_______ 0(填“>”或“<”),写出推理过程_______
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼(C2H8N2)。
已知:①C2H8N2(l)+4O2(g)=2CO2(g)+N2(g)+4H2O(l) ΔH1=-2765.0kJ/mol
②2O2(g) +N2(g)=N2O4(l) ΔH2=-19.5kJ/mol
③H2O(g)= H2O(l) ΔH3=-44.0kJ/mol
则C2H8N2(1)+2N2O4(1)=3N2(g)+2CO2(g)+4H2O(g)的ΔH为
(2)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步:I2(g)→2I(g)(快反应)
第二步:I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步:IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是_______
| A.N2O分解反应中,k值与碘蒸气浓度大小有关 |
| B.v(第二步的逆反应)<v(第三步反应) |
| C.IO为反应的催化剂 |
| D.第二步活化能比第三步大 |
①达到平衡后,仅升高温度,k正增大的倍数
②一定温度下在刚性密闭容器中充入CO、NO和N2物质的量之比为2:2:1,压强为p0kPa。达平衡时压强为0.9p0kPa,则

(4)我国科技人员计算了在一定温度范围内下列反应的平衡常数Kp:
①3N2H4(1)=4NH3(g)+N2(g) ΔH1 Kp1
②4NH3(g)=2N2(g)+6H2(g) ΔH2 Kp2
绘制pKp1-T和pKp2-T的线性关系图如图所示:(已知:pKp=-1gKp)

①由图可知,ΔH1
②反应3N2H4(1)=3N2(g)+6H2(g)的K=
您最近半年使用:0次
解答题-原理综合题
|
困难
(0.15)
【推荐3】某小组探秘人体血液中的运载氧平衡及酸碱平衡,回答下列问题:
Ⅰ.人体运载氧平衡及CO中毒、解毒机制。
人体中的血红蛋白(Hb)能被CO结合而失去结合 能力,吸入高压氧可以使血红蛋白恢复结合
能力,吸入高压氧可以使血红蛋白恢复结合 能力,原理如下:
能力,原理如下:
ⅰ.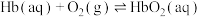

ⅱ.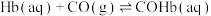

ⅱ.

ⅳ.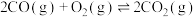

(1)
________ (用含a、b或c的代数式表示)。
(2) 也影响Hb结合
也影响Hb结合 的能力,反应如下:
的能力,反应如下:
 ,下列关于该反应的说法正确的是 。
,下列关于该反应的说法正确的是 。
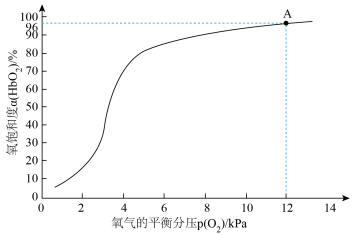
(3)36.5℃时,氧饱和度[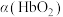 ,
,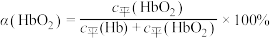 ]与氧气的平衡分压[
]与氧气的平衡分压[ ]关系如下图所示,计算36.5℃时A点反应ⅰ的平衡常数
]关系如下图所示,计算36.5℃时A点反应ⅰ的平衡常数
____________________ (写出计算过程;氧气的平衡浓度可用氧气的平衡分压代替)。
正常人体血液中主要含有 和形成的缓冲溶液,能缓解外界的酸碱影响而保持pH基本不变。正常人体和代谢性酸中毒病人的血气分析结果见表:
和形成的缓冲溶液,能缓解外界的酸碱影响而保持pH基本不变。正常人体和代谢性酸中毒病人的血气分析结果见表:
(4)37℃时 的水解常数
的水解常数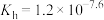 ,
,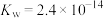 ,已知某同学血浆中
,已知某同学血浆中 ,写出人体血液中存在的水解平衡方程式
,写出人体血液中存在的水解平衡方程式___________ ;请判断该同学血液的pH是否正常________ 。(填“是”或“否”)
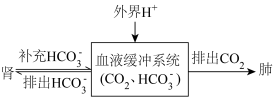
(5)人体酸碱平衡维持机制简要表达如下图: 会
会__________ (选填“增加”或“减少”)。
②对于重度代谢性酸中毒的病人应该采用什么治疗方法__________ 。(选填字母)
A.口服0.9% KCl溶液 B.口服5%葡萄糖溶液
C.静脉注射5% 溶液 D.静脉注射0.9% NaCl溶液
溶液 D.静脉注射0.9% NaCl溶液
Ⅰ.人体运载氧平衡及CO中毒、解毒机制。
人体中的血红蛋白(Hb)能被CO结合而失去结合
 能力,吸入高压氧可以使血红蛋白恢复结合
能力,吸入高压氧可以使血红蛋白恢复结合 能力,原理如下:
能力,原理如下:ⅰ.
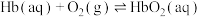

ⅱ.
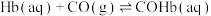

ⅱ.


ⅳ.
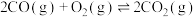

(1)

(2)
 也影响Hb结合
也影响Hb结合 的能力,反应如下:
的能力,反应如下:
 ,下列关于该反应的说法正确的是 。
,下列关于该反应的说法正确的是 。A.当 不变时,反应达到平衡 不变时,反应达到平衡 | B.若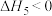 ,则该反应任意温度下能自发 ,则该反应任意温度下能自发 |
C.高氧条件下,血液中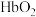 浓度增加 浓度增加 | D.人体代谢酸增加,该反应K值变大 |
(3)36.5℃时,氧饱和度[
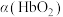 ,
,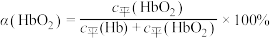 ]与氧气的平衡分压[
]与氧气的平衡分压[ ]关系如下图所示,计算36.5℃时A点反应ⅰ的平衡常数
]关系如下图所示,计算36.5℃时A点反应ⅰ的平衡常数
正常人体血液中主要含有
 和形成的缓冲溶液,能缓解外界的酸碱影响而保持pH基本不变。正常人体和代谢性酸中毒病人的血气分析结果见表:
和形成的缓冲溶液,能缓解外界的酸碱影响而保持pH基本不变。正常人体和代谢性酸中毒病人的血气分析结果见表:项目名称 | 结果浓度 | 参考范围 | |
正常人 | 代谢性酸中毒病人 | ||
| 40 | 50 | 35~45 |
| 24.2 | 19 | 23.3~24.8 |
血液酸碱度(pH) | 7.40 | 7.21 | 7.35~7.45 |
(4)37℃时
 的水解常数
的水解常数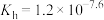 ,
,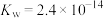 ,已知某同学血浆中
,已知某同学血浆中 ,写出人体血液中存在的水解平衡方程式
,写出人体血液中存在的水解平衡方程式(5)人体酸碱平衡维持机制简要表达如下图:
 会
会②对于重度代谢性酸中毒的病人应该采用什么治疗方法
A.口服0.9% KCl溶液 B.口服5%葡萄糖溶液
C.静脉注射5%
 溶液 D.静脉注射0.9% NaCl溶液
溶液 D.静脉注射0.9% NaCl溶液
您最近半年使用:0次
解答题-原理综合题
|
困难
(0.15)
【推荐1】硼酸(H3BO3)溶于水,大量用于玻璃(光学玻璃、耐酸玻璃、耐热玻璃等)工业。
(1)常温下,向20 mL 0.2 mol·L-1硼酸溶液中滴加0.2 mol·L-1 NaOH溶液,其pH随NaOH溶液体积的变化如图所示:
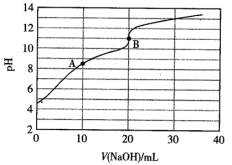
已知:H3BO3+NaOH=NaBO2+2H2O。
①A点溶液中的离子浓度由大到小的顺序是______ 。
②H3BO3的电离常数约为______ mol·L-1。
(2)用惰性电极电解法制备硼酸的工作原理如图所示。

①已知阳离子交换膜和阴离子交换膜分别只允许阳离子和阴离子通过,则X膜是______ ,Y膜是______ ,Z膜是______ 。
②m为直流电源的______ 极,N极的电极反应式为______ 。
(1)常温下,向20 mL 0.2 mol·L-1硼酸溶液中滴加0.2 mol·L-1 NaOH溶液,其pH随NaOH溶液体积的变化如图所示:

已知:H3BO3+NaOH=NaBO2+2H2O。
①A点溶液中的离子浓度由大到小的顺序是
②H3BO3的电离常数约为
(2)用惰性电极电解法制备硼酸的工作原理如图所示。

①已知阳离子交换膜和阴离子交换膜分别只允许阳离子和阴离子通过,则X膜是
②m为直流电源的
您最近半年使用:0次
解答题-原理综合题
|
困难
(0.15)
解题方法
【推荐2】二氧化碳被认为是加剧温室效应的主要来源。2014年11月12日中美两国在北
京发表《中美气候变化联合声明》,中国政府承诺到2030年前停止增加二氧化碳排放,
为此政府大力推广二氧化碳的综合开发和利用。以CO2和NH3为原料合成尿素是固定和
利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g) NH2CO2NH4(s) △H1 =" a" kJ·mol-1
NH2CO2NH4(s) △H1 =" a" kJ·mol-1
反应Ⅱ:NH2CO2NH4(s) CO(NH2)2(s)+H2O(g) △H2 =+72.49kJ·mol-1
CO(NH2)2(s)+H2O(g) △H2 =+72.49kJ·mol-1
总反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) △H3 =-86.98kJ·mol-1
CO(NH2)2(s)+H2O(g) △H3 =-86.98kJ·mol-1
请回答下列问题:
(1)反应Ⅰ的△H1 =__________ kJ·mol-1(用具体数据表示)。
(2)反应Ⅲ中影响CO2平衡转化率的因素很多,图1为某特定条件下,不同水碳比n(H2O)/n(CO2)和温度影响CO2平衡转化率变化的趋势曲线。
①其他条件相同时,为提高CO2的平衡转化率,生产中可以采取的措施是_________ (填“提高”或“降低”)水碳比。
②当温度高于190℃后,CO2平衡转化率出现如图1所示的变化趋势,其原因是__________________ 。
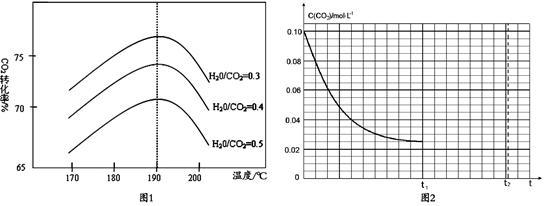
(3)反应Ⅰ的平衡常数表达式K1 =____________________ 。
(4)某研究小组为探究反应Ⅰ中影响c(CO2)的因素,在恒温下将0.4molNH3和0.2molCO2放入容积为2L的密闭容器中,从反应开始到达到平衡过程中c(CO2)随时间t变化趋势的曲线如图2所示。若其他条件不变,t1时将容器体积压缩到1L,请画出t1后c(CO2)随时间t变化趋势曲线(t2达到新的平衡)____ 。
(5)尿素在土壤中会发生反应CO(NH2)2+2H2O (NH4)2CO3。下列物质中与尿素有类似性质的是
(NH4)2CO3。下列物质中与尿素有类似性质的是______ 。
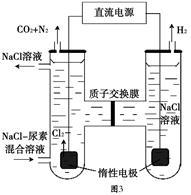
(6)人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如图3。阳极室中发生的反应为_________________________ 、________________________________ 。
京发表《中美气候变化联合声明》,中国政府承诺到2030年前停止增加二氧化碳排放,
为此政府大力推广二氧化碳的综合开发和利用。以CO2和NH3为原料合成尿素是固定和
利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g)
 NH2CO2NH4(s) △H1 =" a" kJ·mol-1
NH2CO2NH4(s) △H1 =" a" kJ·mol-1反应Ⅱ:NH2CO2NH4(s)
 CO(NH2)2(s)+H2O(g) △H2 =+72.49kJ·mol-1
CO(NH2)2(s)+H2O(g) △H2 =+72.49kJ·mol-1总反应Ⅲ:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) △H3 =-86.98kJ·mol-1
CO(NH2)2(s)+H2O(g) △H3 =-86.98kJ·mol-1请回答下列问题:
(1)反应Ⅰ的△H1 =
(2)反应Ⅲ中影响CO2平衡转化率的因素很多,图1为某特定条件下,不同水碳比n(H2O)/n(CO2)和温度影响CO2平衡转化率变化的趋势曲线。
①其他条件相同时,为提高CO2的平衡转化率,生产中可以采取的措施是
②当温度高于190℃后,CO2平衡转化率出现如图1所示的变化趋势,其原因是

(3)反应Ⅰ的平衡常数表达式K1 =
(4)某研究小组为探究反应Ⅰ中影响c(CO2)的因素,在恒温下将0.4molNH3和0.2molCO2放入容积为2L的密闭容器中,从反应开始到达到平衡过程中c(CO2)随时间t变化趋势的曲线如图2所示。若其他条件不变,t1时将容器体积压缩到1L,请画出t1后c(CO2)随时间t变化趋势曲线(t2达到新的平衡)
(5)尿素在土壤中会发生反应CO(NH2)2+2H2O
 (NH4)2CO3。下列物质中与尿素有类似性质的是
(NH4)2CO3。下列物质中与尿素有类似性质的是| A.NH2COONH4 |
| B.H2NOCCH2CH2CONH2 |
| C.HOCH2CH2OH |
| D.HOCH2CH2NH2 |
(6)人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如图3。阳极室中发生的反应为

您最近半年使用:0次
【推荐3】工业上可电解 溶液制备电池用高纯
溶液制备电池用高纯 。
。
(1) 溶液的制备
溶液的制备
利用菱锰矿粉(主要成分为 ,还含有少量
,还含有少量 、
、 、CoO、
、CoO、 等杂质)制备
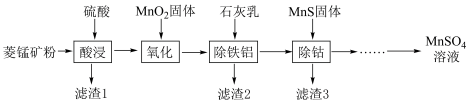
等杂质)制备 溶液的流程如下:
溶液的流程如下:
已知:25℃时, ,
,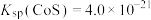 ,
,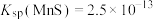 。在本实验条件下
。在本实验条件下 不能被
不能被 氧化。
氧化。
①“酸浸”过程中加入过量硫酸的目的是___________ 。
②“氧化”过程中发生反应的离子方程式为___________ 。
③“除钴”过程中加入过量的难溶电解质MnS,所得悬油液由
___________ 。
(2)高纯 的制备
的制备
①以石墨为电极材料电解 溶液可制备
溶液可制备 ,阳极的电极方程式为
,阳极的电极方程式为___________ 。
②电解后,从电极棒表面剥离出粗 ,粉碎处理后经清洗得到高纯
,粉碎处理后经清洗得到高纯 。粗
。粗 表面的可溶性杂质除少量
表面的可溶性杂质除少量 以外,还有
以外,还有___________ (填化学式)。
③ 的一种长方体晶胞结构如图所示,每个锰原子被6个氧原子包围,形成的空间构型为
的一种长方体晶胞结构如图所示,每个锰原子被6个氧原子包围,形成的空间构型为___________ 。

 溶液制备电池用高纯
溶液制备电池用高纯 。
。(1)
 溶液的制备
溶液的制备利用菱锰矿粉(主要成分为
 ,还含有少量
,还含有少量 、
、 、CoO、
、CoO、 等杂质)制备
等杂质)制备 溶液的流程如下:
溶液的流程如下:
已知:25℃时,
 ,
, ,
,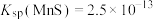 。在本实验条件下
。在本实验条件下 不能被
不能被 氧化。
氧化。①“酸浸”过程中加入过量硫酸的目的是
②“氧化”过程中发生反应的离子方程式为
③“除钴”过程中加入过量的难溶电解质MnS,所得悬油液由

(2)高纯
 的制备
的制备①以石墨为电极材料电解
 溶液可制备
溶液可制备 ,阳极的电极方程式为
,阳极的电极方程式为②电解后,从电极棒表面剥离出粗
 ,粉碎处理后经清洗得到高纯
,粉碎处理后经清洗得到高纯 。粗
。粗 表面的可溶性杂质除少量
表面的可溶性杂质除少量 以外,还有
以外,还有③
 的一种长方体晶胞结构如图所示,每个锰原子被6个氧原子包围,形成的空间构型为
的一种长方体晶胞结构如图所示,每个锰原子被6个氧原子包围,形成的空间构型为
您最近半年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
【推荐1】超分子化学已逐渐扩展到化学的各个分支,还扩展到生命科学和物理学等领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。___________ ;核外未成对电子数是___________ 个。
(2)该超分子中存在的化学键类型有___________ 。
A σ键Bπ键C离子键D氢键
(3)该超分子中配体CO提供孤电子对的原子是___________ (填元素符号),p-甲酸丁酯吡啶配体中C原子的杂化方式有___________ 。
(4)从电负性角度解释CF3COOH的酸性强于CH3COOH的原因___________ 。
(5)C60与金刚石互为同素异形体,从结构与性质之间的关系解释C60的熔点远低于金刚石的原因是___________ 。
(6)已知:某晶胞中各原子的相对位置可用如图所示的原子坐标表示,其中所有顶点原子坐标均为(0,0,0)。___________ 。已知该晶体的密度是ρg·cm-3,Mo的摩尔质量是M g·mol-1,阿伏伽德罗常数是NA,晶体中距离最近的Mo原子核之间的距离为___________ pm。

(2)该超分子中存在的化学键类型有
A σ键Bπ键C离子键D氢键
(3)该超分子中配体CO提供孤电子对的原子是
(4)从电负性角度解释CF3COOH的酸性强于CH3COOH的原因
(5)C60与金刚石互为同素异形体,从结构与性质之间的关系解释C60的熔点远低于金刚石的原因是
(6)已知:某晶胞中各原子的相对位置可用如图所示的原子坐标表示,其中所有顶点原子坐标均为(0,0,0)。

您最近半年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
【推荐2】[化学—选修3:物质结构与性质]
(1)已知X和Y均为短周期元素,其原子的第一至第五电离能如下表所示:
根据上述信息:
①X和氯元素形成的简单分子的空间构型为________ 。
②Y的基态原子的核外电子排布式为________ ,若Y和氯元素形成的分子的相对分子质量为267,请在下列方框中写出该分子的结构式(若存在配位键,用“→”表示)
_____
(2)碳元素可以形成多种单质及化合物:
①C60的结构如图1。C60中的碳原子的杂化轨道类型是________ ;

解释:②金刚石中的C-C的键长大于C60中C-C的键长的原因是________ ;
③金刚石的熔点高于C60的原因是________ ;
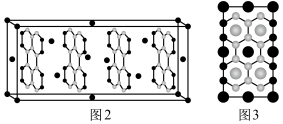
(3)如图2是钾的石墨插层化合物的晶胞图(图中大球表示K原子,小球表示C原子),如图3是晶胞沿右侧方向的投影.
①该化合物的化学式是__________________ ;
②K层与C层之间的作用力是____________________________ ;
③K层中K原子之间的最近距离是C-C键的键长dC-C的_______________ 倍
(4)SiC的晶胞与金刚石的晶胞相似,设碳原子的直径为a cm,硅原子的直径为b cm,则晶胞的边长为_____________ cm(用含a、b的式子表示)。
(1)已知X和Y均为短周期元素,其原子的第一至第五电离能如下表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 | I5 |
| X | 801 | 2427 | 3660 | 25026 | 32827 |
| Y | 577.5 | 1816.7 | 2744.8 | 11577 | 14842 |
①X和氯元素形成的简单分子的空间构型为
②Y的基态原子的核外电子排布式为
(2)碳元素可以形成多种单质及化合物:
①C60的结构如图1。C60中的碳原子的杂化轨道类型是

| 碳元素单质 | C-C键长/pm | 熔点/℃ |
| 金刚石 | 154.45 | 3900 |
| C60 | 145~140 | 600(升华) |
③金刚石的熔点高于C60的原因是
(3)如图2是钾的石墨插层化合物的晶胞图(图中大球表示K原子,小球表示C原子),如图3是晶胞沿右侧方向的投影.

①该化合物的化学式是
②K层与C层之间的作用力是
③K层中K原子之间的最近距离是C-C键的键长dC-C的
(4)SiC的晶胞与金刚石的晶胞相似,设碳原子的直径为a cm,硅原子的直径为b cm,则晶胞的边长为
您最近半年使用:0次
解答题-结构与性质
|
困难
(0.15)
解题方法
【推荐3】(1)氮化硼(BN)是一种用途广泛的无机非金属材料,常见有立方氮化硼与六方氮化硼两种结构。六方氮化硼是一种白色难熔的耐高温物质,它具有类似石墨层状结构,被成为白石墨,常用作润滑剂,虽然六方氮化硼结构与石墨相似,但六方氮化硼却并不导电,具有优良的绝缘性能。立方氮化硼是棕色或暗红色的晶体,为闪锌矿结构,硬度仅次于金刚石,具有很高的热稳定性和化学惰性,因此,立方氮化硼磨具的磨削性能十分优异。
①写出氮化硼中B和N的基态电子排布式_______ 。
②氮化硼非常稳定,在红热时才能与水蒸气发生水解反应,写出该化学方程式_______ 。
③H3BO3是一元酸,试从分子结构角度解释原因_______ 。
④判断六方氮化硼中B与N的杂化类型_______ 、_______ 。
⑤从化学键角度解释为什么六方氮化硼的结构与石墨相似,但六方氮化硼却并不导电_______ 。
(2)PH3可由白磷(P4)和氢气反应生成。已知键能:P-P:213kJ·mol-1,H-H:435kJ·mol-1,P-H:326kJ·mol-1。
①画出白磷的结构式(空间结构)_______ 。
②写出所对应反应的化学方程式_______ 。
③根据键能计算该反应的焓变(反应物和产物均为气态,写出简要的计算过程)_______ 。
(3)锡的利用在我国有几千年历史,青铜器中就含有锡,殷墟中还出土过锡制品。锡的熔点232℃,有两种常见的同素异形体一白锡和灰锡,二者在一定温度下可以相互转化。
①锡的密度为7.28g·cm-3,晶胞参数a=583pmc=318pm,延展性好,质软。通过计算求出一个白锡晶胞中的锡原子数_______ 。
②灰锡的密度为5.75g·cm-3,有金刚石的结构。灰锡和白锡的部分热力学数据如下:
通过计算说明常温(25℃)时,灰锡和白锡哪种更稳定_______ ;
③锡做的茶叶罐不能放在冰箱中冷冻保存,通过计算说明原因_______ 。
①写出氮化硼中B和N的基态电子排布式
②氮化硼非常稳定,在红热时才能与水蒸气发生水解反应,写出该化学方程式
③H3BO3是一元酸,试从分子结构角度解释原因
④判断六方氮化硼中B与N的杂化类型
⑤从化学键角度解释为什么六方氮化硼的结构与石墨相似,但六方氮化硼却并不导电
(2)PH3可由白磷(P4)和氢气反应生成。已知键能:P-P:213kJ·mol-1,H-H:435kJ·mol-1,P-H:326kJ·mol-1。
①画出白磷的结构式(空间结构)
②写出所对应反应的化学方程式
③根据键能计算该反应的焓变(反应物和产物均为气态,写出简要的计算过程)
(3)锡的利用在我国有几千年历史,青铜器中就含有锡,殷墟中还出土过锡制品。锡的熔点232℃,有两种常见的同素异形体一白锡和灰锡,二者在一定温度下可以相互转化。
①锡的密度为7.28g·cm-3,晶胞参数a=583pmc=318pm,延展性好,质软。通过计算求出一个白锡晶胞中的锡原子数
②灰锡的密度为5.75g·cm-3,有金刚石的结构。灰锡和白锡的部分热力学数据如下:
 /kJ·mol-1 /kJ·mol-1 | 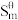 J/-1·K-1·mol-1 J/-1·K-1·mol-1 | |
| Sn(灰) Sn(白) | -2.12 0 | 44.15 51.55 |
通过计算说明常温(25℃)时,灰锡和白锡哪种更稳定
③锡做的茶叶罐不能放在冰箱中冷冻保存,通过计算说明原因
您最近半年使用:0次