2021年以来,全国十六个省市将氢能源写入“十四五”规划中,氢能是助力“碳达峰、碳中和”战略目标实现的重要新能源,以CH4为原料制H2具有广阔的应用前景。在一定条件下CH4与CO2催化重整制 涉及以下反应:
涉及以下反应:
主反应:CH4(g)+CO2(g) 2CO(g)+2H2(g) △H1=+248 kJ·mol-1
2CO(g)+2H2(g) △H1=+248 kJ·mol-1
副反应:CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41 kJ·mol-1
CO(g)+H2O(g) △H2=+41 kJ·mol-1
(1)写出CH4与H2O反应生成CO和H2的热化学方程式___________ 。
(2)我国学者模拟主反应重整制H2,研究在Pt-Ni合金和Sn-Ni合金催化下。甲烷逐级脱氢的反应。不同催化剂的甲烷脱氢反应历程与相对能量关系如图所示(*表示吸附在催化剂表面的物质,吸附过程产生的能量称为吸附能)。
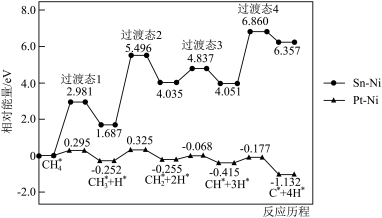
使用Sn-Ni合金作为催化剂的历程中最大能垒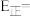
___________ eV;脱氢反应阶段选择Pt-Ni合金作为催化剂效果更好,理由是___________ 。
(3)恒压P0条件下,CO2与CH4以等物质的量投料进行催化重整实验,CO2和CH4的平衡转化率随温度的变化曲线如图所示。

①曲线___________ (填“A”或“B”)表示CO2的平衡转化率。
②X点的速率:v(正)___________ v(逆)(填“>”“<”或“=”)。
③800 K时,主反应的平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
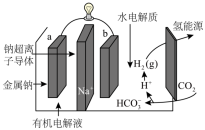
(4)科学家研发出一种新系统,通过“溶解”水中的CO2触发电化学反应,该装置可有效减少碳的排放,并得到氢能源,其工作原理如图所示。则生成H2的电极反应式为___________ 。
 涉及以下反应:
涉及以下反应:主反应:CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H1=+248 kJ·mol-1
2CO(g)+2H2(g) △H1=+248 kJ·mol-1副反应:CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41 kJ·mol-1
CO(g)+H2O(g) △H2=+41 kJ·mol-1(1)写出CH4与H2O反应生成CO和H2的热化学方程式
(2)我国学者模拟主反应重整制H2,研究在Pt-Ni合金和Sn-Ni合金催化下。甲烷逐级脱氢的反应。不同催化剂的甲烷脱氢反应历程与相对能量关系如图所示(*表示吸附在催化剂表面的物质,吸附过程产生的能量称为吸附能)。

使用Sn-Ni合金作为催化剂的历程中最大能垒
(3)恒压P0条件下,CO2与CH4以等物质的量投料进行催化重整实验,CO2和CH4的平衡转化率随温度的变化曲线如图所示。

①曲线
②X点的速率:v(正)
③800 K时,主反应的平衡常数Kp=
(4)科学家研发出一种新系统,通过“溶解”水中的CO2触发电化学反应,该装置可有效减少碳的排放,并得到氢能源,其工作原理如图所示。则生成H2的电极反应式为

更新时间:2023-09-21 13:38:06
|
相似题推荐
【推荐1】一定条件下 能氧化
能氧化 制
制 ,这对资源综合利用有重要意义。相关的化学反应如下:
,这对资源综合利用有重要意义。相关的化学反应如下:
I.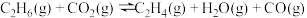
II.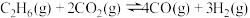
(1)已知反应的能量变化如图1所示。
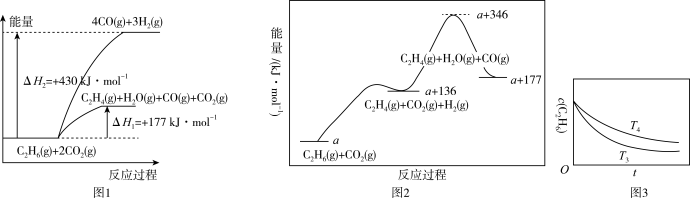
①当生成等物质的量的 时,反应
时,反应_______ (填“I”或“II”)吸收的热量更多。
②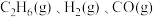 生成
生成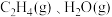 的热化学方程式为
的热化学方程式为_______ 。
(2)反应II不利于乙烯的生成的原因是_______ 。
(3)有研究表明,在催化剂作用下,反应I分两步进行,其反应过程及能量变化如图2所示。
①决定反应I的反应速率的步骤是_______ (填“第一步”或“第二步”),原因是_______ 。
②第一步的化学方程式为_______ 。
(4)在恒容密闭的容器中充入一定量的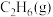 和
和 ,保持其他条件不变,控制反应温度分别为
,保持其他条件不变,控制反应温度分别为 和
和 ,测得
,测得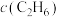 随时间
随时间 的变化曲线如图3所示,则
的变化曲线如图3所示,则
_______  (填“大于”或“小于”)
(填“大于”或“小于”) ,原因是
,原因是_______ 。
(5)温度为T时,向一密闭容器中通入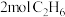 和
和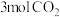 ,一段时间后,反应Ⅰ和反应Ⅱ均达到平衡,
,一段时间后,反应Ⅰ和反应Ⅱ均达到平衡, 的转化率为50%,
的转化率为50%, 的选择性为60%,此时容器容积为
的选择性为60%,此时容器容积为 ,则该温度下反应I的平衡常数
,则该温度下反应I的平衡常数
_______ 。
 能氧化
能氧化 制
制 ,这对资源综合利用有重要意义。相关的化学反应如下:
,这对资源综合利用有重要意义。相关的化学反应如下:I.
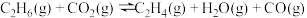
II.
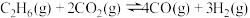
(1)已知反应的能量变化如图1所示。

①当生成等物质的量的
 时,反应
时,反应②
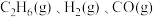 生成
生成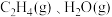 的热化学方程式为
的热化学方程式为(2)反应II不利于乙烯的生成的原因是
(3)有研究表明,在催化剂作用下,反应I分两步进行,其反应过程及能量变化如图2所示。
①决定反应I的反应速率的步骤是
②第一步的化学方程式为
(4)在恒容密闭的容器中充入一定量的
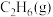 和
和 ,保持其他条件不变,控制反应温度分别为
,保持其他条件不变,控制反应温度分别为 和
和 ,测得
,测得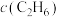 随时间
随时间 的变化曲线如图3所示,则
的变化曲线如图3所示,则
 (填“大于”或“小于”)
(填“大于”或“小于”) ,原因是
,原因是(5)温度为T时,向一密闭容器中通入
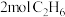 和
和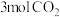 ,一段时间后,反应Ⅰ和反应Ⅱ均达到平衡,
,一段时间后,反应Ⅰ和反应Ⅱ均达到平衡, 的转化率为50%,
的转化率为50%, 的选择性为60%,此时容器容积为
的选择性为60%,此时容器容积为 ,则该温度下反应I的平衡常数
,则该温度下反应I的平衡常数
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】国家主席习近平提出了中国应对气候变化的两个目标:二氧化碳排放力争于2030年前达到峰值,于2060年前实现碳中和。因此,科学家研发 利用技术、降低空气中
利用技术、降低空气中 含量成为了热点。回答下列问题:
含量成为了热点。回答下列问题:
(1) 还原
还原 制
制 的部分反应如下:
的部分反应如下:
①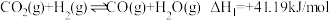
②
反应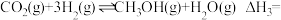
______ 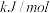
(2)在一定条件下,向 恒容密闭容器中充入
恒容密闭容器中充入 和
和 发生反应
发生反应 ,测得在相同时间内,不同温度下
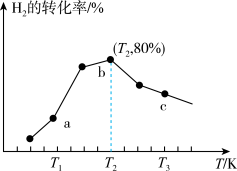
,测得在相同时间内,不同温度下 的转化率如图所示。a、b、c点
的转化率如图所示。a、b、c点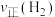 的大小顺序为
的大小顺序为_______________ ; 时,若达到平衡时所用时间为
时,若达到平衡时所用时间为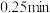 ,则
,则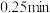 内
内 的平均反应速率为
的平均反应速率为___________  (保留三位有效数字),若平衡时压强为
(保留三位有效数字),若平衡时压强为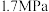 ,
,
_______ 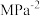 (保留三位有效数字,
(保留三位有效数字, 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
(3)一定条件下,反应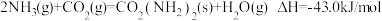 ,达到平衡.欲使反应速率增大且平衡向正反应方向移动,需要改变的条件为
,达到平衡.欲使反应速率增大且平衡向正反应方向移动,需要改变的条件为_______________ (任写一种)。
(4)温度为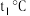 时,将等物质的量的
时,将等物质的量的 和
和 充入体积为
充入体积为 的密闭容器中发生反应:
的密闭容器中发生反应: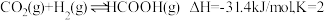 。实验测得:
。实验测得: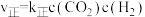 、
、 ,
, 、
、 为速率常数。
为速率常数。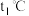 时,
时,
_____ ;温度为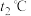 时,
时,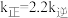 ,则
,则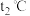
_____ (填“>”“<”或“=”)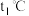 。
。
 利用技术、降低空气中
利用技术、降低空气中 含量成为了热点。回答下列问题:
含量成为了热点。回答下列问题:(1)
 还原
还原 制
制 的部分反应如下:
的部分反应如下:①
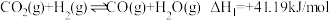
②

反应
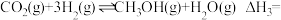
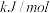
(2)在一定条件下,向
 恒容密闭容器中充入
恒容密闭容器中充入 和
和 发生反应
发生反应 ,测得在相同时间内,不同温度下
,测得在相同时间内,不同温度下 的转化率如图所示。a、b、c点
的转化率如图所示。a、b、c点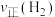 的大小顺序为
的大小顺序为 时,若达到平衡时所用时间为
时,若达到平衡时所用时间为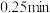 ,则
,则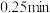 内
内 的平均反应速率为
的平均反应速率为 (保留三位有效数字),若平衡时压强为
(保留三位有效数字),若平衡时压强为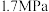 ,
,
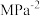 (保留三位有效数字,
(保留三位有效数字, 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
(3)一定条件下,反应
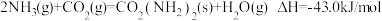 ,达到平衡.欲使反应速率增大且平衡向正反应方向移动,需要改变的条件为
,达到平衡.欲使反应速率增大且平衡向正反应方向移动,需要改变的条件为(4)温度为
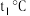 时,将等物质的量的
时,将等物质的量的 和
和 充入体积为
充入体积为 的密闭容器中发生反应:
的密闭容器中发生反应: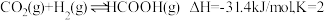 。实验测得:
。实验测得: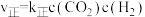 、
、 ,
, 、
、 为速率常数。
为速率常数。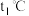 时,
时,
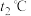 时,
时,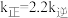 ,则
,则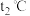
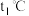 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】化石燃料的开发、利用和燃烧尾气处理成为研究的热点。
(1)利用焦炉煤气制取甲醇,发生的主要反应为CO(g)+2H2(g) CH3OH(g)。下表所列为常见化学键的键能数据:(提示CO和N2是等电子体,其电子式相似)
CH3OH(g)。下表所列为常见化学键的键能数据:(提示CO和N2是等电子体,其电子式相似)
则CO(g)+2H2(g) CH3OH(g)的△H=
CH3OH(g)的△H=__________ kJ·mol-1,若想提高CH3COH的产率,可以采取的措施有__________ 、__________ (任写2条)。
(2)可以用H2等清洁能源代替天然气(主要成分CH4),两者的热化学方程式如下:H2(g) + O2(g) = H2O(1) △H= -286 kJ·mol-1;CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890 kJ/mol。现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热2034 kJ,则原混合气体中H2与CH4的物质的量之比是
O2(g) = H2O(1) △H= -286 kJ·mol-1;CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890 kJ/mol。现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热2034 kJ,则原混合气体中H2与CH4的物质的量之比是_______ 。反应过程中消耗的氧气在标注状况下的体积为_________ 。
(3)化石燃料会排放含SO2的烟气会形成酸雨,危害环境。工业上常用催化还原法和碱吸收法处理SO2体。1molCH4完全燃烧生成气态水和1molS(g)燃烧的能量变化如下图所示:
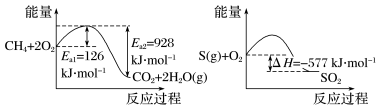
在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式:__________ ;也可以用NaOH吸收化石燃料燃烧产生的SO2,然后通入足量的O2,这样做的目的是__________ ;
(4)第(3)题中得到的S在O2中燃烧生成SO2,在催化剂的作用下与O2发生反应产生SO3,所发生的的化学方程式为2SO2(g) +O2(g) 2SO3(g),在温度不变的情况下,同时加快该反应的化学反应速率和提高SO2的转化率的措施有
2SO3(g),在温度不变的情况下,同时加快该反应的化学反应速率和提高SO2的转化率的措施有__________ (任写1条)。
(1)利用焦炉煤气制取甲醇,发生的主要反应为CO(g)+2H2(g)
 CH3OH(g)。下表所列为常见化学键的键能数据:(提示CO和N2是等电子体,其电子式相似)
CH3OH(g)。下表所列为常见化学键的键能数据:(提示CO和N2是等电子体,其电子式相似)| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能(kJ/mol) | 348 | 414 | 436 | 327 | 1032 | 464 |
则CO(g)+2H2(g)
 CH3OH(g)的△H=
CH3OH(g)的△H=(2)可以用H2等清洁能源代替天然气(主要成分CH4),两者的热化学方程式如下:H2(g) +
 O2(g) = H2O(1) △H= -286 kJ·mol-1;CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890 kJ/mol。现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热2034 kJ,则原混合气体中H2与CH4的物质的量之比是
O2(g) = H2O(1) △H= -286 kJ·mol-1;CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890 kJ/mol。现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热2034 kJ,则原混合气体中H2与CH4的物质的量之比是(3)化石燃料会排放含SO2的烟气会形成酸雨,危害环境。工业上常用催化还原法和碱吸收法处理SO2体。1molCH4完全燃烧生成气态水和1molS(g)燃烧的能量变化如下图所示:

在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式:
(4)第(3)题中得到的S在O2中燃烧生成SO2,在催化剂的作用下与O2发生反应产生SO3,所发生的的化学方程式为2SO2(g) +O2(g)
 2SO3(g),在温度不变的情况下,同时加快该反应的化学反应速率和提高SO2的转化率的措施有
2SO3(g),在温度不变的情况下,同时加快该反应的化学反应速率和提高SO2的转化率的措施有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题。
(1)实验①的目的是___________________________________________ ,实验中滴加FeCl3溶液的目的是________________________________ 。
(2)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是________________________________________________________ (用实验中所提供的几种试剂)。
(3)某同学在50 mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如下图甲所示,则A、B、C三点所表示的瞬时反应速率最慢的是_____________ 。

(4)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图乙、丙所示的实验。请回答相关问题:
①定性分析:如图乙可通过观察_________________________________ ,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_______________________________________ 。
②定量分析:用图丙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是______________________________ 。
(5)通过对上述实验过程的分析,在实验设计时,要考虑_________ 方法的应用。
| 编号 | 实验操作 | 实验现象 |
| ① | 分别在试管A、B中加入5 mL 5% H2O2溶液,各滴入2滴1 mol/L FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 | 试管A中不再产生气泡; 试管B中产生的气泡量增大。 |
| ② | 另取两支试管分别加入5 mL 5% H2O2溶液和5 mL 10% H2O2溶液。 | 试管A、B中均未明显见到有气泡产生。 |
(2)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是
(3)某同学在50 mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如下图甲所示,则A、B、C三点所表示的瞬时反应速率最慢的是

(4)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图乙、丙所示的实验。请回答相关问题:
①定性分析:如图乙可通过观察
②定量分析:用图丙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是
(5)通过对上述实验过程的分析,在实验设计时,要考虑
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】腓 是一种应用广泛的化工原料。工业上先合成氨气,再进一步制备肼。对于合成氨反应,
是一种应用广泛的化工原料。工业上先合成氨气,再进一步制备肼。对于合成氨反应,
 。完成下列填空:
。完成下列填空:
(1)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行试验,所得结果如图所示,(其他条件相同):
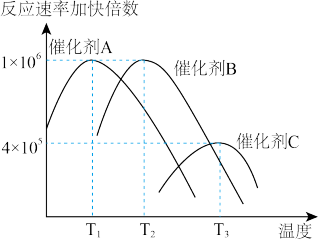
则生产中适宜选择的催化剂是_______ (填“A”或B”或“C”),理由是:_______ 。
(2)恒温恒容时,下列判断可以作为该反应达到平衡的标志的是_______ 。
a.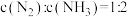 b.混合气体的平均分子量不变
b.混合气体的平均分子量不变
c.混合气体的密度保持不变 d.
(3)在一体积为 的密闭容器中充入了
的密闭容器中充入了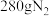 ,
,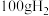 ,反应半小时后,测得有
,反应半小时后,测得有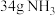 生成,则用
生成,则用 表示该反应的速率为
表示该反应的速率为_______ 。上述反应的平衡常数K值变大,该反应_______ (选填编号)。
a.一定向正反应方向移动 b.平衡移动时,逆反应速率先减小后增大
c.一定向逆反应方向移动 d.平衡移动时,正反应速率先增大后减小
(4)T℃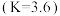 的某一时刻下,
的某一时刻下,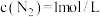 ,
,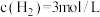 ,
,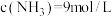 ,在这种情况下该反应是否处于平衡状态
,在这种情况下该反应是否处于平衡状态_______ (选填“是”、“否”),此时反应速率是v正_______ v逆(选填“>”、“<”、“=”);判断理由是_______ 。
(5)合成氨的造气过程中发生反应: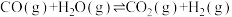 。恒容容器中放入一定量的
。恒容容器中放入一定量的 和
和 ,若
,若 的平衡物质的量浓度与温度T的关系如图所示,则:
的平衡物质的量浓度与温度T的关系如图所示,则:

①平衡状态A与C相比,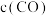 更大的是
更大的是_______ (选填A或C);
②在 时,若反应处于状态D,则一定有v正
时,若反应处于状态D,则一定有v正_______ v逆(选填“>”、“<”、“=”);
③若 、
、 时的平衡常数分别为
时的平衡常数分别为 、
、 ,则
,则
_______  (选填“>”、“<”、“=”);
(选填“>”、“<”、“=”);
④830℃,反应平衡常数 ,则在恒容密闭容器中加入
,则在恒容密闭容器中加入 的
的 和
和 的
的 ,达到平衡时,
,达到平衡时, 的转化率为
的转化率为_______ 。
(6)肼可作为火箭燃料, 在
在 气体中燃烧生成氮气和气态水,放出
气体中燃烧生成氮气和气态水,放出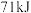 的热量,写出该反应的热化学方程式:
的热量,写出该反应的热化学方程式:_______ 。上述反应中,氧化剂是_______ (写化学式),每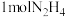 参加反应,转移的电子是
参加反应,转移的电子是_______  。
。
(7) 固体中滴入浓氨水会产生大量氨气,原因除了
固体中滴入浓氨水会产生大量氨气,原因除了 溶于水放热外,还有(从平衡移动角度说明):
溶于水放热外,还有(从平衡移动角度说明):_______ 。
 是一种应用广泛的化工原料。工业上先合成氨气,再进一步制备肼。对于合成氨反应,
是一种应用广泛的化工原料。工业上先合成氨气,再进一步制备肼。对于合成氨反应,
 。完成下列填空:
。完成下列填空:(1)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行试验,所得结果如图所示,(其他条件相同):

则生产中适宜选择的催化剂是
(2)恒温恒容时,下列判断可以作为该反应达到平衡的标志的是
a.
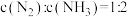 b.混合气体的平均分子量不变
b.混合气体的平均分子量不变c.混合气体的密度保持不变 d.

(3)在一体积为
 的密闭容器中充入了
的密闭容器中充入了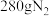 ,
,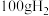 ,反应半小时后,测得有
,反应半小时后,测得有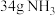 生成,则用
生成,则用 表示该反应的速率为
表示该反应的速率为a.一定向正反应方向移动 b.平衡移动时,逆反应速率先减小后增大
c.一定向逆反应方向移动 d.平衡移动时,正反应速率先增大后减小
(4)T℃
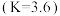 的某一时刻下,
的某一时刻下,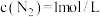 ,
,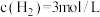 ,
,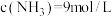 ,在这种情况下该反应是否处于平衡状态
,在这种情况下该反应是否处于平衡状态(5)合成氨的造气过程中发生反应:
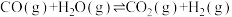 。恒容容器中放入一定量的
。恒容容器中放入一定量的 和
和 ,若
,若 的平衡物质的量浓度与温度T的关系如图所示,则:
的平衡物质的量浓度与温度T的关系如图所示,则:
①平衡状态A与C相比,
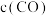 更大的是
更大的是②在
 时,若反应处于状态D,则一定有v正
时,若反应处于状态D,则一定有v正③若
 、
、 时的平衡常数分别为
时的平衡常数分别为 、
、 ,则
,则
 (选填“>”、“<”、“=”);
(选填“>”、“<”、“=”);④830℃,反应平衡常数
 ,则在恒容密闭容器中加入
,则在恒容密闭容器中加入 的
的 和
和 的
的 ,达到平衡时,
,达到平衡时, 的转化率为
的转化率为(6)肼可作为火箭燃料,
 在
在 气体中燃烧生成氮气和气态水,放出
气体中燃烧生成氮气和气态水,放出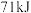 的热量,写出该反应的热化学方程式:
的热量,写出该反应的热化学方程式: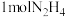 参加反应,转移的电子是
参加反应,转移的电子是 。
。(7)
 固体中滴入浓氨水会产生大量氨气,原因除了
固体中滴入浓氨水会产生大量氨气,原因除了 溶于水放热外,还有(从平衡移动角度说明):
溶于水放热外,还有(从平衡移动角度说明):
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】 可作为水溶液中
可作为水溶液中 歧化反应
歧化反应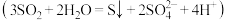 的催化剂。某实验小组为探究浓度、催化剂和溶液酸性对
的催化剂。某实验小组为探究浓度、催化剂和溶液酸性对 歧化反应速率的影响,分别在盛有反应物的试管中加入2mL相应试剂,密闭放置观察现象。
歧化反应速率的影响,分别在盛有反应物的试管中加入2mL相应试剂,密闭放置观察现象。
回答下列问题:
(1)实验①、②说明 是水溶液中
是水溶液中 歧化反应的催化剂,则a应是
歧化反应的催化剂,则a应是___________ (填化学式)。
(2)实验②、③的目的是___________ 。
(3)实验①、⑤说明___________ ,实验②是实验④的对比实验,则
___________ ,可得出的结论是___________ 。
(4) 可作为水溶液中
可作为水溶液中 歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
i.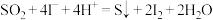
ii.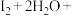 ___________
___________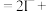 ___________+
___________+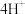 。
。___________
 可作为水溶液中
可作为水溶液中 歧化反应
歧化反应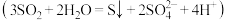 的催化剂。某实验小组为探究浓度、催化剂和溶液酸性对
的催化剂。某实验小组为探究浓度、催化剂和溶液酸性对 歧化反应速率的影响,分别在盛有反应物的试管中加入2mL相应试剂,密闭放置观察现象。
歧化反应速率的影响,分别在盛有反应物的试管中加入2mL相应试剂,密闭放置观察现象。| 实验编号 | 反应物 | 试剂组成 | 实验现象 |
| ① | 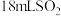 饱和溶液 饱和溶液 | a | 无明显现象 |
| ② | 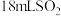 饱和溶液 饱和溶液 | 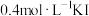 | 一段时间出现浑浊 |
| ③ | 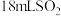 稀溶液 稀溶液 | 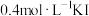 | 出现浑浊较②慢 |
| ④ | 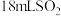 饱和溶液 饱和溶液 | 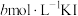 、 、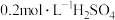 | 出现浑浊较②快 |
| ⑤ | 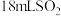 饱和溶液 饱和溶液 | 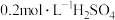 | 无明显现象 |
(1)实验①、②说明
 是水溶液中
是水溶液中 歧化反应的催化剂,则a应是
歧化反应的催化剂,则a应是(2)实验②、③的目的是
(3)实验①、⑤说明

(4)
 可作为水溶液中
可作为水溶液中 歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
歧化反应的催化剂,可能的催化过程如下。将ii补充完整。i.
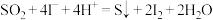
ii.
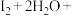 ___________
___________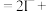 ___________+
___________+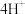 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】据2021年最新统计,中国机动车保有量达到3.8亿辆,稳居世界第一
I.正戊烷异构化为异戊烷是油品升级的一项重要技术,正戊烷和异戊烷的部分性质如表:
(1)稳定性:正戊烷_______ 异戊烷(填“>”或“=”或“<”)。
(2)25°C,10lkPa 时,正戊烷异构化成异戊烷的热化学反应方程式为_______ 。
(3)在合适催化剂和一定压强下,正戊烷的平衡转化率随温度变化如图所示。
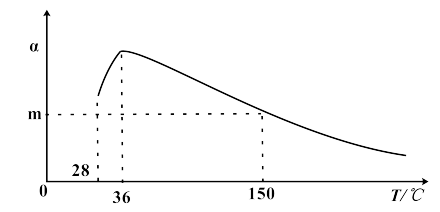
①28-36°C时,随温度升高,正戊烷的平衡转化率增大,原因是_______
②150 °C时,体系压强从100kPa升高到500kPa,正戊烷的平衡转化率_______ (填“增大”、“减小”或“不变”。)
II.不断改进汽车尾气净化技术是减轻大气污染的重要举增。其中一种“净化反应”的原理为:2CO(g)+2NO(g) 2CO2(g)+N2(g) ∆H<0
2CO2(g)+N2(g) ∆H<0
(4)以下情况能说明净化反应达到平衡状态的是_______
(5)净化反应速率v=v正·v逆=k正p2(CO)p2(NO)·k逆P2(CO2)·p(N2),其中k正、k逆分别为正、逆反应的速率常数,p为气体的分压(分压=总压×物质的量分数)。
①升高温度,
______ (填“增大”、“减小”或“不变”):
②保持压强为P1、温度为t1不变,按照n(CO): n(NO)=1: 1投料反应,平衡时CO的转化宰为80%,则该反应的Kp=_______ (Kp 为用分压代替浓度计算的平衡常数)。
I.正戊烷异构化为异戊烷是油品升级的一项重要技术,正戊烷和异戊烷的部分性质如表:
| 名称 | 结构简式 | 熔点/℃ | 沸点/℃ | 燃烧热/kJ mol-1 mol-1 |
| 正戊烷 | CH3CH2CH2CH2CH3 | -130 | 36 | 3506.1 |
| 异戊烷 | (CH3)2CHCH2CH3 | -159.4 | 27.8 | 3504.1 |
(1)稳定性:正戊烷
(2)25°C,10lkPa 时,正戊烷异构化成异戊烷的热化学反应方程式为
(3)在合适催化剂和一定压强下,正戊烷的平衡转化率随温度变化如图所示。

①28-36°C时,随温度升高,正戊烷的平衡转化率增大,原因是
②150 °C时,体系压强从100kPa升高到500kPa,正戊烷的平衡转化率
II.不断改进汽车尾气净化技术是减轻大气污染的重要举增。其中一种“净化反应”的原理为:2CO(g)+2NO(g)
 2CO2(g)+N2(g) ∆H<0
2CO2(g)+N2(g) ∆H<0(4)以下情况能说明净化反应达到平衡状态的是_______
| A.混合气体的平均相对分子质量不变 | B.NO的体积分数保持不变 |
| C.p(CO) : p(N2)=2:1 | D.2v正(CO)=v逆(N2) |
①升高温度,

②保持压强为P1、温度为t1不变,按照n(CO): n(NO)=1: 1投料反应,平衡时CO的转化宰为80%,则该反应的Kp=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氢气是一种清洁能源。制氢和储氢作为氢能利用的关键技术,是当前科学家主要关注的热点问题。
(1)已知; (g)+H2(g)→
(g)+H2(g)→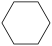 (g) ∆H=-119.6kJ/mol
(g) ∆H=-119.6kJ/mol
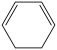 (g)+2H2(g)→
(g)+2H2(g)→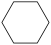 (g) ∆H=-237.1kJ/mol
(g) ∆H=-237.1kJ/mol
 (g)+3H2(g)→
(g)+3H2(g)→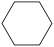 (g) ∆H=-208.4kJ/mol
(g) ∆H=-208.4kJ/mol
请求出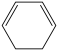 (g)+H2(g)→
(g)+H2(g)→ (g) ∆H=
(g) ∆H=________ kJ/mol
(2)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢。
 (g)
(g)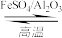
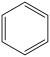 (g)+3H2(g)
(g)+3H2(g)
在某温度下,向恒容容器中加入环己烷,其起始浓度为a mol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=_______ (用含a、b的关系式表达)。
(3)一定条件下,如下图所示装置可实现有机物的电化学储氢(除目标产物外,近似认为无其它有机物生成)。

①实现有机物储氢的电极是__________ ;A 正极 B 负极 C 阴极 D 阳极
其电极反应方程为:___________ 。
②实验研究表明,当外加电压超过一定值以后,发现电极D产物中苯(g)的体积分数随着电压的增大而减小,其主要原因是相关电极除目标产物外,还有一种单质气体生成,这种气体是__________ 。已知单质气体为2 mol,求此装置的电流效率η=__________ 。[η=(生成目标产物消耗的电子数/转移的电子总数)×100%,计算结果保留小数点后1位]。
(1)已知;
 (g)+H2(g)→
(g)+H2(g)→ (g) ∆H=-119.6kJ/mol
(g) ∆H=-119.6kJ/mol (g)+2H2(g)→
(g)+2H2(g)→ (g) ∆H=-237.1kJ/mol
(g) ∆H=-237.1kJ/mol  (g)+3H2(g)→
(g)+3H2(g)→ (g) ∆H=-208.4kJ/mol
(g) ∆H=-208.4kJ/mol请求出
 (g)+H2(g)→
(g)+H2(g)→ (g) ∆H=
(g) ∆H=(2)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢。
 (g)
(g)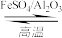
 (g)+3H2(g)
(g)+3H2(g)在某温度下,向恒容容器中加入环己烷,其起始浓度为a mol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=
(3)一定条件下,如下图所示装置可实现有机物的电化学储氢(除目标产物外,近似认为无其它有机物生成)。

①实现有机物储氢的电极是
其电极反应方程为:
②实验研究表明,当外加电压超过一定值以后,发现电极D产物中苯(g)的体积分数随着电压的增大而减小,其主要原因是相关电极除目标产物外,还有一种单质气体生成,这种气体是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】N2O4是一种无色气体,常被用作火箭推进剂组分中的氧化剂。
(1)已知:①2O2(g)+N2(g) N2O4(l) △H1;
N2O4(l) △H1;
②N2O4 (l)+O2(g) N2(g)+2H2O(g) △H2;
N2(g)+2H2O(g) △H2;
联氨和从N2O4作为火箭推进剂时发生反应:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) 的△H=_________ (用含△H1、△H2的式子表示)。
(2)一定温度下,在容积为2L的恒容密闭容器中充入xmolN2O4(g),发生反应:N2O4(g) 2NO2(g) △H=+24.4kJ/mol。体系中NO2浓度随时间变化的情况如图所示。
2NO2(g) △H=+24.4kJ/mol。体系中NO2浓度随时间变化的情况如图所示。
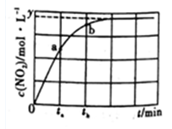
①下列可作为判断反应达到平衡的依据是_______ (填序号)。
a.v正(N2O4)=2v逆(NO2). b.体系颜色不变
c.气体平均相对分子质量不变 d.气体密度不变
② ta时,v正_________ v逆(填“>”“ =”或“<”,下同);ta时v逆____________ tb时v逆。
③该反应的平衡常数K=__________ 。
④对于气体参与的反应,平衡常数也可用气体组分(B)的平衡分压p(B)代替该气体的平衡浓度c(B),
则该反应平衡常数KP=_____________ (用表达式表示);已知:上述反应中,正反应速率为v正=k正·p(N2O4),逆反应速率v逆= k逆·p2(NO2),其中k正、k逆为速率常数,则k正为_______________ 以k逆、KP表示)
(1)已知:①2O2(g)+N2(g)
 N2O4(l) △H1;
N2O4(l) △H1;②N2O4 (l)+O2(g)
 N2(g)+2H2O(g) △H2;
N2(g)+2H2O(g) △H2; 联氨和从N2O4作为火箭推进剂时发生反应:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) 的△H=
(2)一定温度下,在容积为2L的恒容密闭容器中充入xmolN2O4(g),发生反应:N2O4(g)
 2NO2(g) △H=+24.4kJ/mol。体系中NO2浓度随时间变化的情况如图所示。
2NO2(g) △H=+24.4kJ/mol。体系中NO2浓度随时间变化的情况如图所示。
①下列可作为判断反应达到平衡的依据是
a.v正(N2O4)=2v逆(NO2). b.体系颜色不变
c.气体平均相对分子质量不变 d.气体密度不变
② ta时,v正
③该反应的平衡常数K=
④对于气体参与的反应,平衡常数也可用气体组分(B)的平衡分压p(B)代替该气体的平衡浓度c(B),
则该反应平衡常数KP=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】硝基苯是一种具有稳定化学性质、高毒性、难生物降解的污染物。工业上采用吸附、还原、氧化等方法可有效降解废水中的硝基苯。
(1)活性炭因为有较大的比表面积、多孔结构而具有较强的吸附能力,其物理吸附平衡建立如图1所示。活性炭处理低浓度的硝基苯废水时,当温度超过50℃,活性炭对硝基苯的吸附量显著下降,原因是___________ (请从平衡移动角度解释)。

(2)铁炭混合物中极小颗粒的炭分散在铁屑内,具有吸附作用,同时作正极材料构成原电池加快反应速率,还能防止铁屑结块。
①酸性环境中,铁炭混合物处理硝基苯废水,难生物降解的硝基苯首先被还原为亚硝基苯( ),然后进一步被还原成可生物降解的苯胺,写出生成亚硝基苯的电极反应式:
),然后进一步被还原成可生物降解的苯胺,写出生成亚硝基苯的电极反应式:___________ 。
②硝基苯的降解率随pH变化如图2所示。pH为4时,降解率达100%,pH为10时,降到50%左右。在碱性条件下,随着pH升高,降解率降低的原因是___________ 。
(3)研究发现,H2O2在Fe2+、Mn2+等离子作用下能够生成羟基自由基(HO)。HO具有很强的氧化作用,是氧化硝基苯的有效因子。H2O2、KMnO4作为强氧化剂,也可以与硝基苯直接发生氧化降解反应。
①相同条件下,三种氧化剂降解硝基苯的去除率如图3,则该条件下最佳的氧化剂是___________ (填化学式)。

②向含有Fe2+的酸性溶液中滴加H2O2,写出生成HO的离子反应方程式:___________ 。
③通过电激发也可以产生HO,可能的机理如图4,产生过程可描述为___________ 。
(1)活性炭因为有较大的比表面积、多孔结构而具有较强的吸附能力,其物理吸附平衡建立如图1所示。活性炭处理低浓度的硝基苯废水时,当温度超过50℃,活性炭对硝基苯的吸附量显著下降,原因是

(2)铁炭混合物中极小颗粒的炭分散在铁屑内,具有吸附作用,同时作正极材料构成原电池加快反应速率,还能防止铁屑结块。
①酸性环境中,铁炭混合物处理硝基苯废水,难生物降解的硝基苯首先被还原为亚硝基苯(
 ),然后进一步被还原成可生物降解的苯胺,写出生成亚硝基苯的电极反应式:
),然后进一步被还原成可生物降解的苯胺,写出生成亚硝基苯的电极反应式:②硝基苯的降解率随pH变化如图2所示。pH为4时,降解率达100%,pH为10时,降到50%左右。在碱性条件下,随着pH升高,降解率降低的原因是
(3)研究发现,H2O2在Fe2+、Mn2+等离子作用下能够生成羟基自由基(HO)。HO具有很强的氧化作用,是氧化硝基苯的有效因子。H2O2、KMnO4作为强氧化剂,也可以与硝基苯直接发生氧化降解反应。
①相同条件下,三种氧化剂降解硝基苯的去除率如图3,则该条件下最佳的氧化剂是

②向含有Fe2+的酸性溶液中滴加H2O2,写出生成HO的离子反应方程式:
③通过电激发也可以产生HO,可能的机理如图4,产生过程可描述为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)现有以下物质:a.NaOH溶液,b.液氨,c.Ba(OH)2固体,d.NaHSO4,e.Fe(OH)3胶体,f.铜,g.CO2,h.CH3COOH。
①以上物质中属于电解质的是___________ (填字母)。
②写出d在熔融时的电离方程式:___________ 。
③在d的水溶液中加入过量c的水溶液,发生反应的离子方程式为___________ 。
(2)高锰酸钾(硫酸酸化)溶液和草酸溶液的反应可用于测定血钙的含量。方法是取2mL血液用蒸馏水稀释后,向其中加入足量草酸铵晶体[化学式为(NH4)2C2O4],反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解后得到H2C2O4,再用KMnO4溶液滴定。
①高锰酸钾(硫酸酸化)溶液和草酸溶液的反应的化学方程式为:___________ ;
②用KMnO4溶液滴定H2C2O4时,判断滴定终点的方法是___________ 。
(3)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用受到广泛关注。SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为___________ 。
(4)①钢铁在自然界中发生电化学腐蚀时的负极反应式为___________ ;
②碱性条件下,甲醇空气燃料电池的负极反应式为___________ 。
(1)现有以下物质:a.NaOH溶液,b.液氨,c.Ba(OH)2固体,d.NaHSO4,e.Fe(OH)3胶体,f.铜,g.CO2,h.CH3COOH。
①以上物质中属于电解质的是
②写出d在熔融时的电离方程式:
③在d的水溶液中加入过量c的水溶液,发生反应的离子方程式为
(2)高锰酸钾(硫酸酸化)溶液和草酸溶液的反应可用于测定血钙的含量。方法是取2mL血液用蒸馏水稀释后,向其中加入足量草酸铵晶体[化学式为(NH4)2C2O4],反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解后得到H2C2O4,再用KMnO4溶液滴定。
①高锰酸钾(硫酸酸化)溶液和草酸溶液的反应的化学方程式为:
②用KMnO4溶液滴定H2C2O4时,判断滴定终点的方法是
(3)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用受到广泛关注。SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为
(4)①钢铁在自然界中发生电化学腐蚀时的负极反应式为
②碱性条件下,甲醇空气燃料电池的负极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】镍电池广泛应用于混合动力汽车系统,电极材料由NiO2、Fe和碳粉涂在铝箔上制成。放电过程中产生Ni(OH)2和Fe(OH)2,Fe(OH)2最终氧化、脱水生成氧化铁。由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行回收研究。
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。
②某温度下一些金属氢氧化物的Ksp及开始沉淀和完全沉淀时的理论pH如表所示:
回答下列问题:
(1)该电池的负极材料是___________________ ,正极反应式为_________________ ,
(2)若电池输出电压为3V,给2W灯泡供电,当电池消耗0.02gFe,理论上电池工作__________ min(小数点后保留2位)。(已知F=96500C/mol)
(3)将电池电极材料用盐酸溶解后加入适量双氧水,其目的是_____________ 。过滤,在滤液中慢慢加入NiO固体,则开始析出沉淀时的离子方程式是_______________ 和___________________ 。若将两种杂质阳离子都沉淀析出,pH应控制在___________ (离子浓度小于或等于1×10-5mol/L为完全沉淀,lg2=0.3、lg3=0.5);设计将析出的沉淀混合物中的两种物质分离开来的实验方案_____________ 。
(4)将加入NiO过滤后的溶液加入Na2C2O4,得到NiC2O4·2H2O和滤液A,A的主要成分是_____________ ;电解滤液A,在阴极产生气体B______ (填分子式);在阳极产生气体C______ (填分子式)。将NiC2O4·2H2O加入到电解后的溶液,再通入电解时某电解产生的气体,即可得到回收产品Ni(OH)3,所通入气体为______ (填“B”、“C”)极气体,判断依据是_________ 。
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。
②某温度下一些金属氢氧化物的Ksp及开始沉淀和完全沉淀时的理论pH如表所示:
M(OH)n | Ksp | pH | |
开始沉淀 | 沉淀完全 | ||
Al(OH)3 | 2.0×10-32 | 3.8 | —— |
Fe(OH)3 | 4.0×10-38 | 1.9 | 3.2 |
Fe(OH)2 | 8.0×10-16 | 6.95 | 9.95 |
Ni(OH)2 | 6.5×10-18 | 5.9 | 8.9 |
回答下列问题:
(1)该电池的负极材料是
(2)若电池输出电压为3V,给2W灯泡供电,当电池消耗0.02gFe,理论上电池工作
(3)将电池电极材料用盐酸溶解后加入适量双氧水,其目的是
(4)将加入NiO过滤后的溶液加入Na2C2O4,得到NiC2O4·2H2O和滤液A,A的主要成分是
您最近一年使用:0次



