 时,草酸
时,草酸 的
的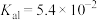 、
、 ,硒化氢
,硒化氢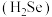 的
的 、
、 。回答下列问题:
。回答下列问题:(1)写出
 在水中的第一步电离方程式:
在水中的第一步电离方程式:(2)草酸具有较强的还原性,将
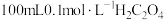 溶液加入少量酸性
溶液加入少量酸性 溶液中。
溶液中。①反应过程中的现象为
②忽略二者混合之后的温度变化,在反应过程中,下列物理量始终增大的是
A.
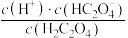 B.
B. C.
C.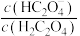 D.
D.
(3)25℃时,
 的
的 溶液中,
溶液中,
 ”、“
”、“ ”或“
”或“ ”)
”)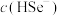 ;往该溶液中加入
;往该溶液中加入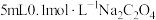 溶液,反应的化学方程式为
溶液,反应的化学方程式为 的电离程度
的电离程度
更新时间:2023-10-28 18:31:49
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答问题:
(1)写出下列物质在水中的电离方程式。
① :
:___________ 。
② :
:___________ 。
(2)常温下,有下列2种溶液:盐酸、醋酸
①向等体积、等浓度的盐酸和醋酸溶液中加入大小相同的镁条,开始时反应速率分别为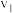 、
、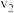 ,其大小关系为
,其大小关系为___________ 。
②等体积、等pH的盐酸和醋酸溶液分别与足量的等浓度的NaOH溶液反应,消耗NaOH溶液的体积分别为a、b,其大小关系为___________ 。
(3)处理含CO、 烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知: 与适量的
与适量的 反应生成
反应生成 和
和 时,放出135 kJ的热量,则此反应的热化学方程式为
时,放出135 kJ的热量,则此反应的热化学方程式为___________ 。
(4)已知在常温下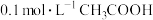 溶液电离程度是百分之一,求其电离平衡常数为
溶液电离程度是百分之一,求其电离平衡常数为___________ 。
(1)写出下列物质在水中的电离方程式。
①
 :
:②
 :
:(2)常温下,有下列2种溶液:盐酸、醋酸
①向等体积、等浓度的盐酸和醋酸溶液中加入大小相同的镁条,开始时反应速率分别为
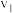 、
、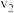 ,其大小关系为
,其大小关系为②等体积、等pH的盐酸和醋酸溶液分别与足量的等浓度的NaOH溶液反应,消耗NaOH溶液的体积分别为a、b,其大小关系为
(3)处理含CO、
 烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知: 与适量的
与适量的 反应生成
反应生成 和
和 时,放出135 kJ的热量,则此反应的热化学方程式为
时,放出135 kJ的热量,则此反应的热化学方程式为(4)已知在常温下
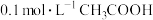 溶液电离程度是百分之一,求其电离平衡常数为
溶液电离程度是百分之一,求其电离平衡常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在常温常压下,有以下9种物质,请回答下列问题:
①干冰 ②氯化钠 ③蔗糖 ④稀硫酸 ⑤ 溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧氯化氢 ⑨
溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧氯化氢 ⑨
(1)其中能导电的是___________ (填写序号,下同);属于电解质的是___________ ;
(2)写出物质⑤在水中的电离方程式:___________ 。
(3)写出物质⑤和⑥在水中发生反应的离子方程式:___________ 。
①干冰 ②氯化钠 ③蔗糖 ④稀硫酸 ⑤
 溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧氯化氢 ⑨
溶液 ⑥碳酸氢钠 ⑦氢氧化钡溶液 ⑧氯化氢 ⑨
(1)其中能导电的是
(2)写出物质⑤在水中的电离方程式:
(3)写出物质⑤和⑥在水中发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】阅读下列科普短文并填空:
海洋的水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 ,
, 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和 用以生产
用以生产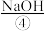 、
、 、
、 、
、 、
、 等,苦卤经过氯气氧化、热空气吹出、
等,苦卤经过氯气氧化、热空气吹出、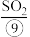 吸收等一系列操作可获得
吸收等一系列操作可获得 。电解熔融氯化钠可冶炼
。电解熔融氯化钠可冶炼 。海底埋藏大量可燃冰资源,
。海底埋藏大量可燃冰资源, 是一种清洁能源。
是一种清洁能源。
(1)上述标有序号的物质中属于电解质的是___________ (填序号,下同);属于非电解质的是___________ 。
(2)写出⑤溶于水的电离方程式:___________ 。
将⑦通入④的溶液中,写出离子反应方程式___________ 。
将⑨通入足量④的溶液中,写出离子反应方程式___________ 。
将⑤与④的溶液混合,写出离子反应方程式___________ 。
(3)海水提溴的过程中涉及的反应有 ,
, ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为___________ 。
(4)实验室检验自来水中含有氯离子的化学试剂为___________ 。
海洋的水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
 ,
, 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和 用以生产
用以生产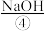 、
、 、
、 、
、 、
、 等,苦卤经过氯气氧化、热空气吹出、
等,苦卤经过氯气氧化、热空气吹出、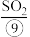 吸收等一系列操作可获得
吸收等一系列操作可获得 。电解熔融氯化钠可冶炼
。电解熔融氯化钠可冶炼 。海底埋藏大量可燃冰资源,
。海底埋藏大量可燃冰资源, 是一种清洁能源。
是一种清洁能源。(1)上述标有序号的物质中属于电解质的是
(2)写出⑤溶于水的电离方程式:
将⑦通入④的溶液中,写出离子反应方程式
将⑨通入足量④的溶液中,写出离子反应方程式
将⑤与④的溶液混合,写出离子反应方程式
(3)海水提溴的过程中涉及的反应有
 ,
, ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为(4)实验室检验自来水中含有氯离子的化学试剂为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有浓度为0.10 mol·L-1的氨水和 0.10 mol·L-1的 NH4Cl溶液。回答下列问题:
(1)氨水显碱性的原因是______ (用电离方程式表示)。向氨水中加入 NH4Cl 固体,氨水的电离程度______ (填“增大”“减小”或“不变”),原因是______ ,溶液的 pH______ (填“增大”“减小”或“不变”)。
(2)NH4Cl 溶液显______ 性,原因是______ (用离子方程式表示)。室温下,若向 NH4Cl溶液中加入少量氨水,使溶液中c( )=c(Cl-),则溶液的 pH
)=c(Cl-),则溶液的 pH______ 7(填“>”“<”或“=”)。
(3)Mg(OH)2浊液中存在 Mg(OH)2 的沉淀溶解平衡。向此浊液中加入浓的 NH4Cl溶液,观察到的现象是______ ,反应原理是______ (用离子方程式表示)。
(1)氨水显碱性的原因是
(2)NH4Cl 溶液显
 )=c(Cl-),则溶液的 pH
)=c(Cl-),则溶液的 pH(3)Mg(OH)2浊液中存在 Mg(OH)2 的沉淀溶解平衡。向此浊液中加入浓的 NH4Cl溶液,观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)有下列物质:①碳酸钙;②熔融的KHSO4;③HNO3;④稀硫酸;⑤CO2;⑥铜;⑦盐酸;⑧乙醇;⑨NaHCO3固体,⑩CH3COOH。上述状态下的物质可导电的是___________ (填序号,下同);属于强电解质的是___________ ;属于非电解质的是___________ ;
(2)在一定温度下,对冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答下列问题:

①a、b、c三点对应的溶液中,c(H+)由小到大的顺序为___________ 。
②a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是___________ 。
③若使c点对应的溶液中的c(CH3COO-)增大,则下列措施中,可行的是___________ (填字母,下同)。
A.加热 B.加入NaOH固体 C.加入K2CO3固体 D.加水 E.加入浓硫酸
④在稀释过程中,随着醋酸浓度的减小,下列始终保持增大趋势的是___________ 。
A.c(H+) B.n(H+) C.CH3COOH分子数 D.
(1)有下列物质:①碳酸钙;②熔融的KHSO4;③HNO3;④稀硫酸;⑤CO2;⑥铜;⑦盐酸;⑧乙醇;⑨NaHCO3固体,⑩CH3COOH。上述状态下的物质可导电的是
(2)在一定温度下,对冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答下列问题:

①a、b、c三点对应的溶液中,c(H+)由小到大的顺序为
②a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是
③若使c点对应的溶液中的c(CH3COO-)增大,则下列措施中,可行的是
A.加热 B.加入NaOH固体 C.加入K2CO3固体 D.加水 E.加入浓硫酸
④在稀释过程中,随着醋酸浓度的减小,下列始终保持增大趋势的是
A.c(H+) B.n(H+) C.CH3COOH分子数 D.

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)氨的水溶液显弱碱性,其原因为___ (用离子方程表示):0.1mol•L-1的氨水中加入少量NH4Cl固体,溶液的pH___ (填“升高”或“降低”);若加入少量明矾,溶液中NH 的浓度
的浓度___ (填“增大”或“减小”)。
(2)硝酸铵加热分解可得到N2O和H2O.250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为___ ,平衡常数表达式为___ ;若有1mol硝酸铵完全分解,转移的电子数为___ mol。
(1)氨的水溶液显弱碱性,其原因为
 的浓度
的浓度(2)硝酸铵加热分解可得到N2O和H2O.250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】水是一种极其微弱的电解质。
(1)已知t℃时纯水的 ,计算该温度下水的离子积
,计算该温度下水的离子积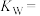
_______ ,该温度下 的硫酸溶液中水电离出的
的硫酸溶液中水电离出的
_______  。
。
(2)对水进行下列操作,能抑制水的电离的是_______。
(3)已知水的电离平衡曲线如图所示:回答下列问题:
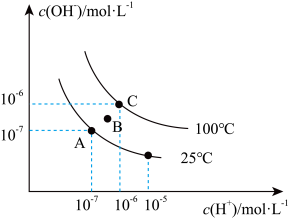
A、B、C、D四点 的关系是
的关系是_______ ( 、
、 …表示)。
…表示)。
(4)室温下,实验测得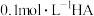 溶液的
溶液的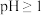 ,下列说法正确的是
,下列说法正确的是_______ 。
a. 可能呈酸性
可能呈酸性
b. 溶液中
溶液中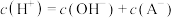
c.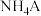 可能呈中性
可能呈中性
(1)已知t℃时纯水的
 ,计算该温度下水的离子积
,计算该温度下水的离子积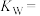
 的硫酸溶液中水电离出的
的硫酸溶液中水电离出的
 。
。(2)对水进行下列操作,能抑制水的电离的是_______。
A.加入一小块 | B.加入适量 溶液 溶液 |
| C.升温至60℃ | D.通入适量 气体 气体 |
(3)已知水的电离平衡曲线如图所示:回答下列问题:

A、B、C、D四点
 的关系是
的关系是 、
、 …表示)。
…表示)。(4)室温下,实验测得
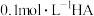 溶液的
溶液的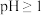 ,下列说法正确的是
,下列说法正确的是a.
 可能呈酸性
可能呈酸性b.
 溶液中
溶液中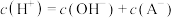
c.
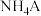 可能呈中性
可能呈中性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】磷能形成多种含氧酸。
(1)一元中强酸次磷酸(H3PO2)是一种精细化工产品,向10 mL H3PO2溶液中加入10 mL等物质的量浓度的NaOH溶液后,所得的溶液中只有H2PO2-、OH-两种阴离子。
① 写出H3PO2溶液与足量NaOH 溶液反应后形成的正盐的化学式:_______ ,该正盐溶液中各离子浓度由大到小的顺序为____________ 。
② 若25℃时,K (H3PO2) = 1×10-2,则0.01 mol · L-1的H3PO2溶液的pH =________ 。
(2)亚磷酸(H3PO3)是二元中强酸,25℃时亚磷酸的电离常数为K1= 3.7×10-2、K2=2.6×10-7。
试从电离平衡移动的角度解释K1、K2数据的差异______________ 。
(3) 25 ℃时,HF的电离常数为K = 3.6×10-4; H3PO4的电离常数为K1=7.5×10-3,K2=6.2×10-8,K3=4.4×10-13。足量NaF溶液和H3PO4溶液反应的离子方程式为______ 。
(4)相同温度下,等物质的量浓度的上述三种磷的含氧酸中。c(H+)由大到小的顺序为______________________________________________________ (用酸的分子式表示)。
(1)一元中强酸次磷酸(H3PO2)是一种精细化工产品,向10 mL H3PO2溶液中加入10 mL等物质的量浓度的NaOH溶液后,所得的溶液中只有H2PO2-、OH-两种阴离子。
① 写出H3PO2溶液与足量NaOH 溶液反应后形成的正盐的化学式:
② 若25℃时,K (H3PO2) = 1×10-2,则0.01 mol · L-1的H3PO2溶液的pH =
(2)亚磷酸(H3PO3)是二元中强酸,25℃时亚磷酸的电离常数为K1= 3.7×10-2、K2=2.6×10-7。
试从电离平衡移动的角度解释K1、K2数据的差异
(3) 25 ℃时,HF的电离常数为K = 3.6×10-4; H3PO4的电离常数为K1=7.5×10-3,K2=6.2×10-8,K3=4.4×10-13。足量NaF溶液和H3PO4溶液反应的离子方程式为
(4)相同温度下,等物质的量浓度的上述三种磷的含氧酸中。c(H+)由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某一元弱酸(用HA表示)在水中的电离方程式是: ,回答下列问题:
,回答下列问题:
(1)适当加热溶液,以上平衡将向_______ (填“左”、“右”)移动。
(2)向溶液中加入适量NaA固体,以上平衡将向_______ (填“左”、“右”)移动。
(3)若向溶液中加入适量NaCl溶液,以上平衡将向_______ (填“左”、“右”、或“不”)移动,溶液pH将_______ (填“增大”、“减小”或“不变”), 的比值
的比值_______ (填“增大”、“减小”或“不变”)。
(4)在25℃下,将 的氨水与
的氨水与 的盐酸等体积混合,反应平衡时溶液中
的盐酸等体积混合,反应平衡时溶液中 ,则溶液呈中性,用含a的代数式表示
,则溶液呈中性,用含a的代数式表示 的电离常数
的电离常数
_______ 。
 ,回答下列问题:
,回答下列问题:(1)适当加热溶液,以上平衡将向
(2)向溶液中加入适量NaA固体,以上平衡将向
(3)若向溶液中加入适量NaCl溶液,以上平衡将向
 的比值
的比值(4)在25℃下,将
 的氨水与
的氨水与 的盐酸等体积混合,反应平衡时溶液中
的盐酸等体积混合,反应平衡时溶液中 ,则溶液呈中性,用含a的代数式表示
,则溶液呈中性,用含a的代数式表示 的电离常数
的电离常数
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.已知25℃时,醋酸、氢硫酸、氢氰酸的电离平衡常数如下表:(单位省略)
(1)体积相同、c(H+)相同的三种酸溶液a.CH3COOH;b.HCN;c.H2SO4分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)_______ 。
(2)25℃时,等浓度的三种溶液①NaCN 溶液、②Na2S溶液、③CH3COONa溶液,pH由大到小的顺序为_______ (填序号)。
(3)25℃时,浓度均为0.01mol/L的①NaCN、②CH3COONa、③NaCl 溶液中,阴离子总浓度由大到小的顺序为_______ (填序号)。
(4)将浓度为0.02mol/L的HCN 与0.01mol/L NaOH 溶液等体积混合,测得混合溶液中c(Na+)>c(CN-),下列关系正确的是_______ 。
a.c(H+)<c(OH-) b.c(H+)+c(HCN)=c(OH-)+c(CN-) c.c(HCN)+c(CN-)=0.01mol/L
(5)25℃时,向NaCN溶液中通入少量H2S,反应的离子方程式为_______ 。
Ⅱ.NaCN是一种重要的基本化工原料,同时也是一种剧毒物质,严重危害人类健康。
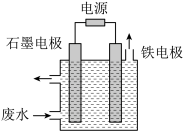
含氰废水中的氰化物常以[Fe(CN)6]3-和CN-的形式存在,工业上有多种废水处理方法。其中电解处理法如图:用如图所示装置处理含CN-废水时,控制溶液pH为9~10并加入一定量的NaCl,一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去。铁电极为_______ (填“阴极”或“阳极”),阳极产生的ClO-的电极反应为_______ ,阳极产生的ClO-将CN-氧化为无害物质而除去的离子方程式为_______ 。
| 醋酸 | 氢硫酸 | 氢氰酸 |
| Ka=1.8×10-5 | Ka1=9.1×10-8 Ka2=1.1×10-12 | Ka=4.9×10-10 |
(2)25℃时,等浓度的三种溶液①NaCN 溶液、②Na2S溶液、③CH3COONa溶液,pH由大到小的顺序为
(3)25℃时,浓度均为0.01mol/L的①NaCN、②CH3COONa、③NaCl 溶液中,阴离子总浓度由大到小的顺序为
(4)将浓度为0.02mol/L的HCN 与0.01mol/L NaOH 溶液等体积混合,测得混合溶液中c(Na+)>c(CN-),下列关系正确的是
a.c(H+)<c(OH-) b.c(H+)+c(HCN)=c(OH-)+c(CN-) c.c(HCN)+c(CN-)=0.01mol/L
(5)25℃时,向NaCN溶液中通入少量H2S,反应的离子方程式为
Ⅱ.NaCN是一种重要的基本化工原料,同时也是一种剧毒物质,严重危害人类健康。
含氰废水中的氰化物常以[Fe(CN)6]3-和CN-的形式存在,工业上有多种废水处理方法。其中电解处理法如图:用如图所示装置处理含CN-废水时,控制溶液pH为9~10并加入一定量的NaCl,一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去。铁电极为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,有关物质的电离平衡常数如下:
回答下列问题。
(1)常温下,醋酸钠的溶液呈___________ 性,原因是___________ (写方程式)
(2)物质的量浓度为 的下列四种溶液,pH由大到小的顺序是___________(填编号)。
的下列四种溶液,pH由大到小的顺序是___________(填编号)。
(3)体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。则HX的电离平衡常数___________ (填“大于”、“等于”或“小于”)醋酸的电离平衡常数:HX是___________ 酸(填“强”或“弱”),理由是___________ 。
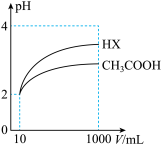
(4)25℃时,若测得CH3COOH与CH3COONa的混合溶液的pH=6,写出溶液中电荷守恒的式子:___________
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 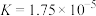 |   | 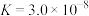 |
(1)常温下,醋酸钠的溶液呈
(2)物质的量浓度为
 的下列四种溶液,pH由大到小的顺序是___________(填编号)。
的下列四种溶液,pH由大到小的顺序是___________(填编号)。| A.Na2CO3 | B.NaClO | C.CH3COONa | D.NaHCO3 |

(4)25℃时,若测得CH3COOH与CH3COONa的混合溶液的pH=6,写出溶液中电荷守恒的式子:
您最近一年使用:0次
【推荐3】医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。回答下列问题:
( ) H++( ) MnO4-+( ) H2C2O4→( ) CO2↑+ ( ) Mn2++( ) ____
(1)配平以上离子方程式,并在横线中填上所需的微粒。
(2)该反应中的还原剂是_____________ (填化学式)。
(3)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为_________ mol。
(4)测定血钙含量的方法是:取2.0mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是__________________________ 。
②溶解沉淀时______ (填“能”或“不能”)用稀盐酸,原因是________________ 。
③若消耗了1.0×10-4 mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙_____ g。
(5)草酸系统命名为乙二酸,请写出乙二酸的结构简式_____________________ 。
(6)已知:Ka1(H2C2O4)=5.9×10—2,Ka2(H2C2O4)=6.4×10—5;Ka(HF)=3.53×10—4,请写出足量草酸(H2C2O4)与NaF溶液反应的化学方程式:______ 。
(1)配平以上离子方程式,并在横线中填上所需的微粒。
(2)该反应中的还原剂是
(3)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为
(4)测定血钙含量的方法是:取2.0mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是
②溶解沉淀时
③若消耗了1.0×10-4 mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙
(5)草酸系统命名为乙二酸,请写出乙二酸的结构简式
(6)已知:Ka1(H2C2O4)=5.9×10—2,Ka2(H2C2O4)=6.4×10—5;Ka(HF)=3.53×10—4,请写出足量草酸(H2C2O4)与NaF溶液反应的化学方程式:
您最近一年使用:0次



