 (简称LFP)主要用于各种锂离子电池,是最安全的锂离子电池正极材料,不含任何对人体有害的重金属元素。以盐湖卤水(主要含有NaCl、
(简称LFP)主要用于各种锂离子电池,是最安全的锂离子电池正极材料,不含任何对人体有害的重金属元素。以盐湖卤水(主要含有NaCl、 、LiCl和
、LiCl和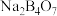 等)为原料制备
等)为原料制备 的工艺流程如图。
的工艺流程如图。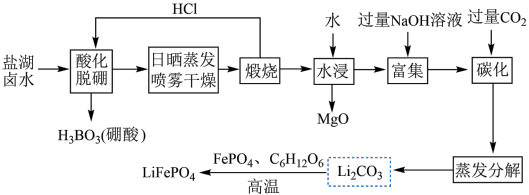
注:日晒蒸发、喷雾干燥后固体含NaCl、LiCl、
 等。
等。(1)
 中Li在元素周期表中的位置为第
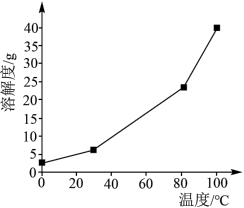
中Li在元素周期表中的位置为第(2)硼酸在水中的溶解度随温度的变化关系如图所示。
已知:
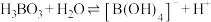
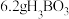 最多与
最多与 溶液完全反应。“酸化脱硼”中采用
溶液完全反应。“酸化脱硼”中采用(3)“煅烧”过程中,常需要搅拌,搅拌的目的是
(4)“蒸发分解”的化学方程式为
(5)已知不同温度下蒸发分解得到
 的产率及其溶解度随温度的变化关系如图所示。则“蒸发分解”的最佳温度是
的产率及其溶解度随温度的变化关系如图所示。则“蒸发分解”的最佳温度是 后需要洗涤,具体操作为
后需要洗涤,具体操作为
(6)用
 、
、 、
、 制备
制备 时,有
时,有 产生,则参与反应的
产生,则参与反应的 和
和 的物质的量之比为
的物质的量之比为
23-24高三上·陕西汉中·阶段练习 查看更多[2]
更新时间:2023-11-03 23:20:27
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】氯化亚铜(CuCl)可用作催化剂、杀菌剂和脱色剂,实验室制备CuCl实验步骤如下:


回答下列问题:
(1)步骤I中,配制0.50 mol/LCuCl2溶液时,不需要使用下列仪器中的___________ (填仪器名称)。
(2)步骤Ⅱ中,充分反应后铜元素转化为无色的[CuCl2]-,其发生可逆反应的离子方程式为___________ 。在加Cu粉前,通常加一定量的NaCl固体,其目的是___________ 。
(3)在进行制备[CuCl2]- 的实验时,为保持安全的实验环境,可以采取的措施是___________ 。
(4)步骤Ⅲ中,用无水乙醇洗涤沉淀的原因是___________ 。
(5)取2.500 g CuCl产品于锥形瓶中,加入稍过量的FeCl3溶液充分反应,再加50 mL水,以邻菲罗啉作指示剂,用1.000 mol/L Ce(SO4)2标准溶液滴定Fe2+,分析样品中CuCl的含量。
已知:滴定原理: Ce4+ +Fe2+ =Ce3++Fe3+; 邻菲罗啉可分别与Fe3+、Fe2+形成浅蓝色和红色的络离子。
①“再加50mL水”的目的是___________ 。
②滴定终点的现象是___________ 。
③若消耗Ce(SO4)2标准溶液的体积为24.00 mL,该样品中CuCl的质量分数是___________ 。


回答下列问题:
(1)步骤I中,配制0.50 mol/LCuCl2溶液时,不需要使用下列仪器中的

(2)步骤Ⅱ中,充分反应后铜元素转化为无色的[CuCl2]-,其发生可逆反应的离子方程式为
(3)在进行制备[CuCl2]- 的实验时,为保持安全的实验环境,可以采取的措施是
(4)步骤Ⅲ中,用无水乙醇洗涤沉淀的原因是
(5)取2.500 g CuCl产品于锥形瓶中,加入稍过量的FeCl3溶液充分反应,再加50 mL水,以邻菲罗啉作指示剂,用1.000 mol/L Ce(SO4)2标准溶液滴定Fe2+,分析样品中CuCl的含量。
已知:滴定原理: Ce4+ +Fe2+ =Ce3++Fe3+; 邻菲罗啉可分别与Fe3+、Fe2+形成浅蓝色和红色的络离子。
①“再加50mL水”的目的是
②滴定终点的现象是
③若消耗Ce(SO4)2标准溶液的体积为24.00 mL,该样品中CuCl的质量分数是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】氮元素单质及其化合物在工农业生产中有重要应用。
(1)氮原子最外层电子的轨道表示式为___ ;氮气分子的电子式为:__ ;已CS2与CO2分子结构相似,CS2熔点高于CO2,其原因是___ 。
(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

浓盐酸液滴附近会出现白烟,发生反应的化学方程式为___ ;浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,其中所含的正盐作一种化肥俗称:__ ,长期施用容易造成土壤酸化板结;FeSO4液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生的反应包括Fe2++2NH3·H2O=Fe(OH)2↓+2NH 和
和___ 。
(3)空气吹脱法是目前消除NH3对水体污染的重要方法。在一定条件下,向水体中加入适量NaOH可使NH3的脱除率增大,用平衡移动原理解释其原因:___ 。
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为___ ,若反应中有0.3mol电子发生转移,生成亚硝酸的质量为___ g(小数点后保留两位有效数字)。
(1)氮原子最外层电子的轨道表示式为
(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
 和
和(3)空气吹脱法是目前消除NH3对水体污染的重要方法。在一定条件下,向水体中加入适量NaOH可使NH3的脱除率增大,用平衡移动原理解释其原因:
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为
您最近一年使用:0次
【推荐3】能将KI氧化为I2的若干种氧化剂有H2O2、Cl2、KIO3、HNO3、KClO3、KMnO4等。
(1)上述试剂最适合贴上的一个标签是_______ (填序号)。
A. B.
B.  C.
C. D.
D.
(2)配平方程式:KClO3+KI+H2SO4=K2SO4+KCl+I2+H2O,____________ 。已知过量KClO3会引起副反应:KClO3+I2→KIO3+Cl2,据此判断:I2和Cl2相比,氧化性较强的是_______ 。
(3)写出KI溶液与Cl2反应的离子方程式为_______ 。
(4)以单线桥法表示下列氧化还原反应的电子转移:H2O2+2H++3I-= +2H2O,
+2H2O,_____________ 。
(5)已知下列四种氧化剂(氧化KI后)对应的还原产物情况如下:
请判断,等物质的量的四种氧化剂分别与足量KI作用,得到I2最多的是_______ 。
(6)根据信息“氧化性Cl2>Br2>HNO3>I2”思考:对于I-、Br-混合溶液,若控制性氧化I-而不氧化Br-,请提出两种合理的氧化方案:①加入_______ ;②加入_______ 。
(1)上述试剂最适合贴上的一个标签是
A.
 B.
B.  C.
C. D.
D.
(2)配平方程式:KClO3+KI+H2SO4=K2SO4+KCl+I2+H2O,
(3)写出KI溶液与Cl2反应的离子方程式为
(4)以单线桥法表示下列氧化还原反应的电子转移:H2O2+2H++3I-=
 +2H2O,
+2H2O,(5)已知下列四种氧化剂(氧化KI后)对应的还原产物情况如下:
| 氧化剂 | KMnO4 | KIO3 | H2O2 | HNO3 |
| 还原产物 | Mn2+ | I2 | H2O | NO |
(6)根据信息“氧化性Cl2>Br2>HNO3>I2”思考:对于I-、Br-混合溶液,若控制性氧化I-而不氧化Br-,请提出两种合理的氧化方案:①加入
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】二氧化碳是用途非常广泛的化工基础原料,回答下列问题:
(1)工业上可以用CO2来生产燃料甲醇。已知:
CO2(g) + 3H2(g) CH3OH(l) + H2O(l) ΔH1 = -131.0 kJ·mol−1
CH3OH(l) + H2O(l) ΔH1 = -131.0 kJ·mol−1
H2(g) + O2(g) = H2O(l) ΔH2 = -285.8 kJ·mol−1
O2(g) = H2O(l) ΔH2 = -285.8 kJ·mol−1
则CH3OH的燃烧热ΔH =________________ 。
(2)在催化剂作用下,CO2和CH4可以直接转化为乙酸:CO2(g) + CH4(g) CH3COOH(g) ΔH = +36.0 kJ·mol−1
CH3COOH(g) ΔH = +36.0 kJ·mol−1
欲使乙酸的平衡产率提高,应采取的措施是__________ (填标号)。
A.升高温度 B.降低温度 C.增大压强 D.降低压强
(3)高温下,CO2与足量的碳在密闭容器中实现反应:C(s) + CO2(g) 2CO(g)。
2CO(g)。
① 该反应的平衡常数表达式K =_____________ 。
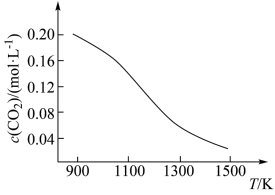
② 向容积为1 L的恒容容器中加入足量的碳和0.2 mol CO2,在不同温度下达到平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示。则该反应为__________ (填“放热”或“吸热”)反应。某温度下,若向该平衡体系中再通入0.2 mol CO2,达到新平衡后,体系中CO的百分含量______________ (填“变大”或“变小”或“不变”,下同),平衡常数__________ 。
(1)工业上可以用CO2来生产燃料甲醇。已知:
CO2(g) + 3H2(g)
 CH3OH(l) + H2O(l) ΔH1 = -131.0 kJ·mol−1
CH3OH(l) + H2O(l) ΔH1 = -131.0 kJ·mol−1H2(g) +
 O2(g) = H2O(l) ΔH2 = -285.8 kJ·mol−1
O2(g) = H2O(l) ΔH2 = -285.8 kJ·mol−1则CH3OH的燃烧热ΔH =
(2)在催化剂作用下,CO2和CH4可以直接转化为乙酸:CO2(g) + CH4(g)
 CH3COOH(g) ΔH = +36.0 kJ·mol−1
CH3COOH(g) ΔH = +36.0 kJ·mol−1欲使乙酸的平衡产率提高,应采取的措施是
A.升高温度 B.降低温度 C.增大压强 D.降低压强
(3)高温下,CO2与足量的碳在密闭容器中实现反应:C(s) + CO2(g)
 2CO(g)。
2CO(g)。① 该反应的平衡常数表达式K =
② 向容积为1 L的恒容容器中加入足量的碳和0.2 mol CO2,在不同温度下达到平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示。则该反应为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】甲醇是重要的有机化工原料,目前世界甲醇年产量超过2.1×107吨,在能源紧张的今天,甲醇的需求也在增大。甲醇的合成方法是:
(i)CO(g)+2H2(g) CH3OH(g) ∆H=-90.1 kJ·mol-1
CH3OH(g) ∆H=-90.1 kJ·mol-1
(ii)2CO(g)+O2(g)=2CO2(g) ∆H=-566.0 kJ·mol-1
(iii)2H2(g)+O2(g)=2H2O(l) ∆H=-572.0 kJ·mol-1
若混合气体中有二氧化碳存在时,还发生下列反应:
(iv)CO2(g)+H2(g) CO(g)+H2O(g) ∆H=+41.1 kJ·mol-1
CO(g)+H2O(g) ∆H=+41.1 kJ·mol-1
回答下列问题:
(1)CH3OH(g)+ O2(g)=CO2(g)+2H2O(l) ∆H=
O2(g)=CO2(g)+2H2O(l) ∆H=_____ kJ·mol-1。
(2)在恒温恒容的密闭容器中发生反应(i),各物质的浓度如表:
①x=_______ 。
②前2min内H2的平均反应速率v(H2)=______ 。该温度下,反应(i)的平衡常数K=_____ (保留2位有效数字)。
③反应进行到第2min时,改变了反应条件,改变的这个条件可能是______ (填字母)。
a.使用催化剂 b.降低温度 c.增加H2的浓度
(3)图中是温度、压强与反应(i)中CO转化率的关系。
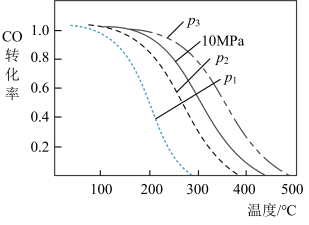
p1、p2、p3的大小关系为________ 。
②实际生产往往采用300~400℃和10 MPa的条件,其原因是_______ 。
(i)CO(g)+2H2(g)
 CH3OH(g) ∆H=-90.1 kJ·mol-1
CH3OH(g) ∆H=-90.1 kJ·mol-1(ii)2CO(g)+O2(g)=2CO2(g) ∆H=-566.0 kJ·mol-1
(iii)2H2(g)+O2(g)=2H2O(l) ∆H=-572.0 kJ·mol-1
若混合气体中有二氧化碳存在时,还发生下列反应:
(iv)CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H=+41.1 kJ·mol-1
CO(g)+H2O(g) ∆H=+41.1 kJ·mol-1回答下列问题:
(1)CH3OH(g)+
 O2(g)=CO2(g)+2H2O(l) ∆H=
O2(g)=CO2(g)+2H2O(l) ∆H=(2)在恒温恒容的密闭容器中发生反应(i),各物质的浓度如表:
 | c(CO) | c(H2) | c(CH3OH) |
| 0 | 0.8 | 1.6 | 0 |
| 2 | 0.6 | x | 0.2 |
| 4 | 0.3 | 0.6 | 0.5 |
| 6 | 0.3 | 0.6 | 0.5 |
①x=
②前2min内H2的平均反应速率v(H2)=
③反应进行到第2min时,改变了反应条件,改变的这个条件可能是
a.使用催化剂 b.降低温度 c.增加H2的浓度
(3)图中是温度、压强与反应(i)中CO转化率的关系。

p1、p2、p3的大小关系为
②实际生产往往采用300~400℃和10 MPa的条件,其原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】氧化钪(Sc2O3)在合金、电光源、催化剂、激活剂和陶瓷等领域有广泛的应用,利用钪精矿为原料(主要成分为Sc2O3,还含有Fe2O3、MnO等杂质)生产氧化钪的一种工艺流程如下:

(1)“酸溶”步骤中,钪的浸出率结果如图所示。由图可知,为使钪的浸出率达90%左右,所采用的生产条件为___________________ 。

(2)加入氨水调节pH=3,过滤,滤渣主要成分是_____________ ;若再向滤液加入氨水调节pH=6,滤液中 Sc3+能否沉淀完全(离子浓度小于10−5 mol/L)______________ (列式计算并作判断)。(25℃时,Ksp[Mn(OH)2]=1.9×10−13、Ksp[Fe(OH)3]=2.6×10−39,Ksp[Sc(OH)3]=9.0×10−31)
(3)已知钪与铝类似,其氢氧化物具有两性。反萃取步骤中,加入NaOH使溶液呈碱性,碱性条件下双氧水可以氧化锰离子生成滤渣,写出该反应的离子方程式______________ 。
(4)“沉钪”前先加入稀盐酸调节溶液至酸性,然后用草酸“沉钪”。25℃时pH=2的草酸溶液中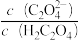 =
=_________________________ 。写出“沉钪”得到草酸钪(难溶于稀酸)的离子方程式___________________ [25℃时,草酸电离平衡常数为Ka1=5.0×10−2,Ka2=5.4×10−5]。
(5)草酸钪“灼烧”的化学方程式为_______________________ 。

(1)“酸溶”步骤中,钪的浸出率结果如图所示。由图可知,为使钪的浸出率达90%左右,所采用的生产条件为

(2)加入氨水调节pH=3,过滤,滤渣主要成分是
(3)已知钪与铝类似,其氢氧化物具有两性。反萃取步骤中,加入NaOH使溶液呈碱性,碱性条件下双氧水可以氧化锰离子生成滤渣,写出该反应的离子方程式
(4)“沉钪”前先加入稀盐酸调节溶液至酸性,然后用草酸“沉钪”。25℃时pH=2的草酸溶液中
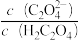 =
=(5)草酸钪“灼烧”的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑨九种元素在周期表中的位置。请用化学用语回答:
(1)填元素符号:③是___________ ,⑧是___________ ,化学性质最不活泼的是___________ 。
(2)在①、②、③三种元素的氧化物对应的水化物中,碱性最强的是___________ (填化学式)。
(3)①、②、③三种元素按原子半径由大到小的顺序依次为___________ (填元素符号)。
(4)⑥元素氢化物的电子式是___________ (填电子式),该氢化物在常温下与②发生反应的化学方程式为___________ ,所得溶液的pH___________ (填“<”、“>”或“=”)7。
(5)9种元素所形成的最高价氧化物对应水化物中酸性最强的是___________ ,呈两性的是___________ (填化学式)
(6)用电子式表示③与⑦反应得到的化合物的形成过程___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑨ | |||
| 4 | ② | ⑧ |
(2)在①、②、③三种元素的氧化物对应的水化物中,碱性最强的是
(3)①、②、③三种元素按原子半径由大到小的顺序依次为
(4)⑥元素氢化物的电子式是
(5)9种元素所形成的最高价氧化物对应水化物中酸性最强的是
(6)用电子式表示③与⑦反应得到的化合物的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。

完成下列填空(填元素符号或化学式):
(1)元素B在元素周期表中的位置是____ ,A、B、C三种元素原子半径从大到小的顺序是____ ;
(2)D简单离子的结构示意图为____ ,D、E中金属性较强的元素是___________ 。D单质在空气中燃烧可生成淡黄色粉末X(D2O2),X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和下图所示实验装置证明X有提供氧气的作用。

(3)装置A使用石灰石与盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是___________ ;
(4)装置C中X与CO2反应的化学方程式是___________ ;
(5)为检验试管F收集的气体的方法,___________ ,即证明X可作供氧剂。

完成下列填空(填元素符号或化学式):
(1)元素B在元素周期表中的位置是
(2)D简单离子的结构示意图为

(3)装置A使用石灰石与盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是
(4)装置C中X与CO2反应的化学方程式是
(5)为检验试管F收集的气体的方法,
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是元素周期表的一部分,表中所列的每个序号分别代表某一元素。

(1)元素②在周期表的位置是_______ 。元素③④组成原子个数比为1∶1的化合物的电子式_______ 。
(2)⑦⑧⑨分别形成的简单离子,它们的离子半径由小到大的顺序是_______ 。
(3)请写出元素⑤最高价氧化物对应水化物与⑦最高价氧化物对应水化物反应的离子反应方程式_______ 。
(4)写出工业制取元素⑥的单质的化学方程式_______ 。
(5)第四周期中分别与①、②同主族的Ga、As形成的GaAs的熔点为1238℃,其熔融状态下不导电。GaAs属于_______ (填“离子化合物”或“共价化合物”);元素⑤与Ga性质相似,下列关于Ga说法错误的是_______ (填写序号)。
A.一定条件下,Ga可溶于强酸与强碱 B.常温下,Ga可与冷水剧烈反应
C. 受热能分解 D.一定条件下,
受热能分解 D.一定条件下, 可与NaOH溶液反应
可与NaOH溶液反应

(1)元素②在周期表的位置是
(2)⑦⑧⑨分别形成的简单离子,它们的离子半径由小到大的顺序是
(3)请写出元素⑤最高价氧化物对应水化物与⑦最高价氧化物对应水化物反应的离子反应方程式
(4)写出工业制取元素⑥的单质的化学方程式
(5)第四周期中分别与①、②同主族的Ga、As形成的GaAs的熔点为1238℃,其熔融状态下不导电。GaAs属于
A.一定条件下,Ga可溶于强酸与强碱 B.常温下,Ga可与冷水剧烈反应
C.
 受热能分解 D.一定条件下,
受热能分解 D.一定条件下, 可与NaOH溶液反应
可与NaOH溶液反应
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】金属铂(Pt)对气体(特别是H2、O2和CO)具有较强的吸附能力。因此常用来做电极材料,从某废旧电极材料(主要含有Pt、C、Al2O3、MgO)中回收Pt的一种工艺流程如图所示。
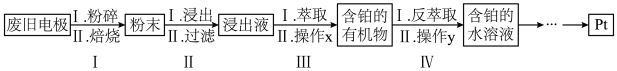
回答下列问题:
(1)过程Ⅰ中“焙烧”之前将废旧电极“粉碎”的目的是___________ 。
(2)实验人员采用三种不同的浸出液分别研究过程Ⅱ中Pt的浸出率。所用浸出液甲、乙、丙分别是HCl-H2SO4-NaClO3、HCI-NaClO3和HCl-H2O2。
①将浸出液为乙时的离子方程式补充完整:_____________
3Pt+___________Cl-+___________ +___________=3[PtCl6]2-+___________H2O
+___________=3[PtCl6]2-+___________H2O
②当NaClO3或H2O2作为氧化剂浸出等量Pt时,n(NaClO3):n(H2O2)=___________ 。
③c(H+)相同、浸出时间相同时,甲、乙、丙三种浸出液对Pt的浸出率如下表。[注:c(NaClO3)按照②中的物质的量关系换算成c(H2O2)计]。
a.以HCl-NaClO3为例,说明当其中氧化剂浓度大于0.2mol/L时,Pt的浸出率降低的原因:随着c(NaClO3)增大,其氧化性增强,部分 被
被___________ 还原而消耗。
b.氧化剂浓度均为0.2mol/L时,甲中Pt的浸出率最低的可能原因:由于三种浸出液中的c(H+)均相同,
(3)过程Ⅲ中萃取剂(R3N)的萃取机理如下(O表示有机体系,A表示水溶液体系)。
ⅰ.R3N(O)+ +
+
 R3NHCl(O)。
R3NHCl(O)。
ⅱ.2R3NHCl(O)+
 (R3NH)2[PtCl6](O)+2
(R3NH)2[PtCl6](O)+2
①分离操作x是___________ 。
②“反萃取”时向含Pt的有机物中加入NaOH溶液,可使[PtCl6]2-进入水溶液体系,反应的离子方程式是___________ 。

回答下列问题:
(1)过程Ⅰ中“焙烧”之前将废旧电极“粉碎”的目的是
(2)实验人员采用三种不同的浸出液分别研究过程Ⅱ中Pt的浸出率。所用浸出液甲、乙、丙分别是HCl-H2SO4-NaClO3、HCI-NaClO3和HCl-H2O2。
①将浸出液为乙时的离子方程式补充完整:
3Pt+___________Cl-+___________
 +___________=3[PtCl6]2-+___________H2O
+___________=3[PtCl6]2-+___________H2O②当NaClO3或H2O2作为氧化剂浸出等量Pt时,n(NaClO3):n(H2O2)=
③c(H+)相同、浸出时间相同时,甲、乙、丙三种浸出液对Pt的浸出率如下表。[注:c(NaClO3)按照②中的物质的量关系换算成c(H2O2)计]。
| 编号 | 氧化剂浓度/mol·L-1 | 0.1 | 0.2 | 0.3 | 0.4 |
| 甲 | HCl-H2SO4-NaClO3对Pt的浸出率/% | 72.7 | 78.2 | 77.5 | 75.4 |
| 乙 | HCl-NaClO3对Pt的浸出率/% | 79.6 | 85.3. | 82.1 | 81.6. |
| 丙 | HCl-H2O2对Pt的浸出率/% | 80.0 | 85.6. | 83.2 | 82.5 |
 被
被b.氧化剂浓度均为0.2mol/L时,甲中Pt的浸出率最低的可能原因:由于三种浸出液中的c(H+)均相同,
(3)过程Ⅲ中萃取剂(R3N)的萃取机理如下(O表示有机体系,A表示水溶液体系)。
ⅰ.R3N(O)+
 +
+
 R3NHCl(O)。
R3NHCl(O)。ⅱ.2R3NHCl(O)+

 (R3NH)2[PtCl6](O)+2
(R3NH)2[PtCl6](O)+2
①分离操作x是
②“反萃取”时向含Pt的有机物中加入NaOH溶液,可使[PtCl6]2-进入水溶液体系,反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】碘化亚铜( )可用作有机反应催化剂。某化学兴趣小组以黄铜矿(主要成分为
)可用作有机反应催化剂。某化学兴趣小组以黄铜矿(主要成分为 ,其中
,其中 的化合价为+2)为原料制备
的化合价为+2)为原料制备 的流程如下:
的流程如下:

已知: 是白色粉末,不溶于水,能与过量
是白色粉末,不溶于水,能与过量 继续反应:
继续反应: ,从而溶于
,从而溶于 溶液中。
溶液中。
回答下列问题:
(1)“浸取”时,反应的化学方程式为_______ ;该步骤使用的 溶液的浓度为560
溶液的浓度为560 ,则其物质的量浓度为
,则其物质的量浓度为_______  (保留2位小数)。
(保留2位小数)。
(2)“滤渣处理”过程中发生的基本反应类型为_______ 。
(3)“溶解”时, 被还原为
被还原为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:_______ 。
(4)“转化”时生成 的离子方程式为
的离子方程式为_______ ,该步骤需要控制 溶液的用量,其原因是
溶液的用量,其原因是_______ 。
(5)用 溶液洗涤沉淀的目的是
溶液洗涤沉淀的目的是_______ 。
(6)已知: ,
, ,取2.00g
,取2.00g 放入锥形瓶中,加入100
放入锥形瓶中,加入100 a
a
 溶液,充分振荡后,测得溶液中
溶液,充分振荡后,测得溶液中 ,则a约为
,则a约为_______ (保留1位小数,溶液体积变化忽略不计)。
 )可用作有机反应催化剂。某化学兴趣小组以黄铜矿(主要成分为
)可用作有机反应催化剂。某化学兴趣小组以黄铜矿(主要成分为 ,其中
,其中 的化合价为+2)为原料制备
的化合价为+2)为原料制备 的流程如下:
的流程如下:
已知:
 是白色粉末,不溶于水,能与过量
是白色粉末,不溶于水,能与过量 继续反应:
继续反应: ,从而溶于
,从而溶于 溶液中。
溶液中。回答下列问题:
(1)“浸取”时,反应的化学方程式为
 溶液的浓度为560
溶液的浓度为560 ,则其物质的量浓度为
,则其物质的量浓度为 (保留2位小数)。
(保留2位小数)。(2)“滤渣处理”过程中发生的基本反应类型为
(3)“溶解”时,
 被还原为
被还原为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(4)“转化”时生成
 的离子方程式为
的离子方程式为 溶液的用量,其原因是
溶液的用量,其原因是(5)用
 溶液洗涤沉淀的目的是
溶液洗涤沉淀的目的是(6)已知:
 ,
, ,取2.00g
,取2.00g 放入锥形瓶中,加入100
放入锥形瓶中,加入100 a
a
 溶液,充分振荡后,测得溶液中
溶液,充分振荡后,测得溶液中 ,则a约为
,则a约为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】三氧化二钴(Co2O3)常用作催化剂、氧化剂及制滤光眼镜的添加剂等。工业上以含钴废料(主要成分为CoO、Co2O3,含有少量MnO2、NiO、Fe2O3杂质)为原料制备Co2O3的流程如下图所示:

已知:“酸浸”后的浸出液中含的金属阳离子主要有Co2+、Fe3+、Ni2+。
回答下列问题:
(1)含钴废料“酸浸”前要研磨处理,其目的是___________ 。
(2)“酸浸”时加入H2O2作___________ (填“氧化剂”或“还原剂”)。生产过程中发现实际消耗双氧水的量大于理论值,主要原因可能___________ 。
(3)“滤渣I”的主要成分为___________ 。
(4)某萃取剂对金属离子的萃取率与溶液pH的关系如图所示,使用该萃取剂时应控制的pH约为___________ (填选项)。
a.2 b.3 c.4 d.5

(5)“沉钴”步骤反应的离子方程式___________ 。
(6)“结晶”得到的主要副产品是___________ 。
(7)“高温煅烧”发生反应化学方程式为___________ 。

已知:“酸浸”后的浸出液中含的金属阳离子主要有Co2+、Fe3+、Ni2+。
回答下列问题:
(1)含钴废料“酸浸”前要研磨处理,其目的是
(2)“酸浸”时加入H2O2作
(3)“滤渣I”的主要成分为
(4)某萃取剂对金属离子的萃取率与溶液pH的关系如图所示,使用该萃取剂时应控制的pH约为
a.2 b.3 c.4 d.5

(5)“沉钴”步骤反应的离子方程式
(6)“结晶”得到的主要副产品是
(7)“高温煅烧”发生反应化学方程式为
您最近一年使用:0次



