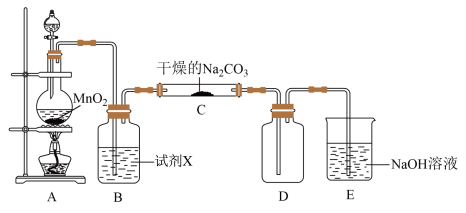
某学习小组探究潮湿的Cl2与Na2CO3反应的产物,进行如图实验:
请回答:
(1)试剂X是______ 。
(2)请写出装置A中的离子方程式______ 。
(3)装置C中潮湿的Cl2和Na2CO3以等物质的量反应,生成NaHCO3气体Cl2O和NaCl,试写出该反应化学方程式______ 。
(4)写出氯气进入装置E发生反应的化学方程式______ 。
(5)用下列两种方法制取氯气,则所得氯气______。
①用含氯化氢146克的浓盐酸与足量的二氧化锰反应
②用87克二氧化锰与足量的浓盐酸反应
(6)将Cl₂通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时, 的物质的量之比为
的物质的量之比为______ 。

请回答:
(1)试剂X是
(2)请写出装置A中的离子方程式
(3)装置C中潮湿的Cl2和Na2CO3以等物质的量反应,生成NaHCO3气体Cl2O和NaCl,试写出该反应化学方程式
(4)写出氯气进入装置E发生反应的化学方程式
(5)用下列两种方法制取氯气,则所得氯气______。
①用含氯化氢146克的浓盐酸与足量的二氧化锰反应
②用87克二氧化锰与足量的浓盐酸反应
| A.②比①多 | B.①比②多 | C.一样多 | D.无法比较 |
(6)将Cl₂通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时,
 的物质的量之比为
的物质的量之比为
更新时间:2023-11-15 15:16:36
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某溶液中可能含有 中的一种或几种。现进行以下实验:取上述溶液少量,加入过量
中的一种或几种。现进行以下实验:取上述溶液少量,加入过量 溶液,产生白色沉淀,过滤,向沉淀中加入过量的稀硝酸,沉淀部分溶解,并产生气体。
溶液,产生白色沉淀,过滤,向沉淀中加入过量的稀硝酸,沉淀部分溶解,并产生气体。
由以上实验判断:
(1)该溶液中肯定存在的离子有_______ 。
(2)肯定不存在的离子为_______ 。
(3)白色沉淀加入硝酸后,部分溶解,反应的离子方程式为_______ 。
 中的一种或几种。现进行以下实验:取上述溶液少量,加入过量
中的一种或几种。现进行以下实验:取上述溶液少量,加入过量 溶液,产生白色沉淀,过滤,向沉淀中加入过量的稀硝酸,沉淀部分溶解,并产生气体。
溶液,产生白色沉淀,过滤,向沉淀中加入过量的稀硝酸,沉淀部分溶解,并产生气体。由以上实验判断:
(1)该溶液中肯定存在的离子有
(2)肯定不存在的离子为
(3)白色沉淀加入硝酸后,部分溶解,反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】化学是人类利用自然资源和应对环境问题的重要科学依据。
Ⅰ.工业上以铝土矿(主要成分为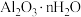 )为原料冶炼金属铝,主要步骤包括:①将粉碎后的铝土矿溶解在氢氧化钠溶液中;②向①所得溶液中通入过量二氧化碳,获得氢氧化铝固体:③使氢氧化铝脱水生成氧化铝;④……
)为原料冶炼金属铝,主要步骤包括:①将粉碎后的铝土矿溶解在氢氧化钠溶液中;②向①所得溶液中通入过量二氧化碳,获得氢氧化铝固体:③使氢氧化铝脱水生成氧化铝;④……
(1)步骤①所涉及的反应_______ (填“是”或“不是”)氧化还原反应。
(2)步骤②中生成氢氧化铝的化学方程式为____________ 。
(3)步骤④为冶炼金属铝的过程,应选择的方法是________ (填序号)。
A.利用铝热反应原理还原 B.电解法 C.热分解法
Ⅱ.从某含Br—的废水中提取 的过程有关实验装置如图所示,包括:过滤、氧化、萃取及蒸馏等步骤。有关物质的密度和沸点如下表所示。已知:溴易溶于四氯化碳和正十二烷。
的过程有关实验装置如图所示,包括:过滤、氧化、萃取及蒸馏等步骤。有关物质的密度和沸点如下表所示。已知:溴易溶于四氯化碳和正十二烷。

(4)甲装置中 发生反应的离子方程式为
发生反应的离子方程式为________ ,氢氧化钠溶液的作用是_______ 。
(5)用装置乙进行萃取操作,溴被萃取在a层中,则选用的萃取剂为_______ (填“四氯化碳”或“正十二烷”)。
(6)用丙装置进行蒸馏操作,先收集到的物质是_______ (填化学式)。
Ⅰ.工业上以铝土矿(主要成分为
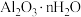 )为原料冶炼金属铝,主要步骤包括:①将粉碎后的铝土矿溶解在氢氧化钠溶液中;②向①所得溶液中通入过量二氧化碳,获得氢氧化铝固体:③使氢氧化铝脱水生成氧化铝;④……
)为原料冶炼金属铝,主要步骤包括:①将粉碎后的铝土矿溶解在氢氧化钠溶液中;②向①所得溶液中通入过量二氧化碳,获得氢氧化铝固体:③使氢氧化铝脱水生成氧化铝;④……(1)步骤①所涉及的反应
(2)步骤②中生成氢氧化铝的化学方程式为
(3)步骤④为冶炼金属铝的过程,应选择的方法是
A.利用铝热反应原理还原 B.电解法 C.热分解法
Ⅱ.从某含Br—的废水中提取
 的过程有关实验装置如图所示,包括:过滤、氧化、萃取及蒸馏等步骤。有关物质的密度和沸点如下表所示。已知:溴易溶于四氯化碳和正十二烷。
的过程有关实验装置如图所示,包括:过滤、氧化、萃取及蒸馏等步骤。有关物质的密度和沸点如下表所示。已知:溴易溶于四氯化碳和正十二烷。物质 |
|
| 正十二烷 |
密度/( | 3.1 | 1.59 | 0.75 |
沸点/℃ | 58.8 | 76.8 | 216.3 |
在水中溶解性 | 微溶 | 难溶 | 难溶 |

(4)甲装置中
 发生反应的离子方程式为
发生反应的离子方程式为(5)用装置乙进行萃取操作,溴被萃取在a层中,则选用的萃取剂为
(6)用丙装置进行蒸馏操作,先收集到的物质是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】黄铜矿(主要成分二硫化亚铁铜,化学式为CuFeS2)为原料可制备金属铜及其化合物,还可以制得铁红、硫磺等,工艺流程如图:
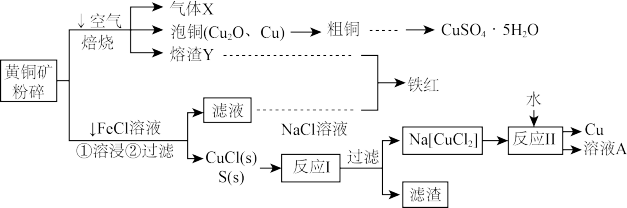
请回答下列问题:
(1)气体X的名称是________ 。
(2)“铁红”化学式为________ 。向粗铜中加入硫酸和稀硝酸的混酸溶液制取硫酸铜时(杂质不参加反应),混酸中H2SO4与HNO3的最佳物质的量之比为________ 。
(3)FeCl3溶液浸取工艺中,溶浸时CuFeS2与FeCl3溶液反应的离子方程式为__________ 。
(4)反应Ⅰ化学方程式为_________ ,反应Ⅱ所得“溶液A”成分是(填化学式)________ 。

请回答下列问题:
(1)气体X的名称是
(2)“铁红”化学式为
(3)FeCl3溶液浸取工艺中,溶浸时CuFeS2与FeCl3溶液反应的离子方程式为
(4)反应Ⅰ化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下图中每一个方格表示有关的一种反应物或生成物(部分的产物已省略);X加热产生等物质的量的A、B、C三种物质,常温下A、C为无色气体,B是一种生活中常见的液体;X与NaOH溶液在加热作用下产生一种能遇浓盐酸产生白烟的气体C;X与HCl反应产生一种无色无味的气体A,它能使澄清石灰变浑浊。请填下列空白:

(1)物质X是_______ (填写化学式)
(2)X中阳离子的检验方法是_______ 。
(3)反应①的化学方程式_______ 。
(4)F→G的化学方程式_______ 。
(5)G→E的离子方程式_______ 。
(6)将2.56 g Cu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12 L(标准状况),则反应中消耗HNO3的物质的量为_______ mol

(1)物质X是
(2)X中阳离子的检验方法是
(3)反应①的化学方程式
(4)F→G的化学方程式
(5)G→E的离子方程式
(6)将2.56 g Cu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12 L(标准状况),则反应中消耗HNO3的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】二氧化钛是钛的重要化合物,钛白(纯净的二氧化钛)是一种折射率高、着色力和遮盖力强、化学性质稳定的白色颜料。钛精矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有Fe2O3、SiO2等杂质,由钛精矿制取一氧化钛,常用硫酸法,其流程如下:

(1)基态22Ti原子的价电子排布式为___________ 。
(2)钛精矿主要成分与硫酸反应的主要产物是TiOSO4和FeSO4,该反应的化学方程式为___________ 。
(3)矿渣主要成分___________ ,试剂X为___________ (填化学式)。
(4)为了从溶液I中获取纯净的FeSO4·7H2O,应采取的操作是___________ 、___________ 、过滤、洗涤、干燥。
(5)用氧化还原滴定法测定制备得到的中间产品中TiO2的质量分数:在一定条件下,将一定量的产品溶解并将TiO2还原为Ti3+,再以KSCN溶液作为指示剂,用硫酸铁铵 [NH4Fe(SO4)2]标准溶液滴定Ti3+至全部生成Ti4+。
①滴定终点的现象是:加入最后半滴标准液时,___________ 。
②滴定分析时,称取TiO2试样0.2g,消耗0.1mol/L[NH4Fe(SO4)2]标准溶液24.00mL,则TiO2的质量分数为(计算结果保留小数点后一位)___________ 。

(1)基态22Ti原子的价电子排布式为
(2)钛精矿主要成分与硫酸反应的主要产物是TiOSO4和FeSO4,该反应的化学方程式为
(3)矿渣主要成分
(4)为了从溶液I中获取纯净的FeSO4·7H2O,应采取的操作是
(5)用氧化还原滴定法测定制备得到的中间产品中TiO2的质量分数:在一定条件下,将一定量的产品溶解并将TiO2还原为Ti3+,再以KSCN溶液作为指示剂,用硫酸铁铵 [NH4Fe(SO4)2]标准溶液滴定Ti3+至全部生成Ti4+。
①滴定终点的现象是:加入最后半滴标准液时,
②滴定分析时,称取TiO2试样0.2g,消耗0.1mol/L[NH4Fe(SO4)2]标准溶液24.00mL,则TiO2的质量分数为(计算结果保留小数点后一位)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaClO2),其工艺流程如下:

已知:①NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。
②高氯酸是至今为止人们已知酸中的最强酸,沸点90 ℃。
请回答下列问题:
(1)反应器Ⅰ中发生反应的化学方程式为_____________ ,冷却的目的是__________________ ,能用蒸馏法分离出高氯酸的原因是___________________ 。
(2)反应器Ⅱ中发生反应的离子方程式为__________________________ 。
(3)通入反应器Ⅱ中的SO2用H2O2代替同样能生成NaClO2,请简要说明双氧水在反应中能代替SO2的原因是___________________ 。
(4) Ca(ClO)2、ClO2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,是因为它们都具有__________ ,请写出工业上用氯气和消石灰生产漂粉精的化学方程式:___________ 。

已知:①NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。
②高氯酸是至今为止人们已知酸中的最强酸,沸点90 ℃。
请回答下列问题:
(1)反应器Ⅰ中发生反应的化学方程式为
(2)反应器Ⅱ中发生反应的离子方程式为
(3)通入反应器Ⅱ中的SO2用H2O2代替同样能生成NaClO2,请简要说明双氧水在反应中能代替SO2的原因是
(4) Ca(ClO)2、ClO2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,是因为它们都具有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】氯碱厂电解饱和食盐水制取氢氧化钠的工艺流程示意图如下:
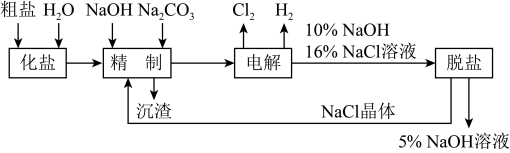
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为_______________________ ,与电源负极相连的电极附近,溶液pH值_____________ (选填:不变、升高或下降)
(2)工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为_______________________ ,_______________________ 。
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是___________ (选填a、b、c,多选扣分)
a、Ba(OH)2 b、Ba(NO3)2 c、BaCl2
(4)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为____________ (选填a,b,c多选扣分)
a、先加NaOH,后加Na2CO3,再加钡试剂
b、先加NaOH,后加钡试剂,再加Na2CO3
c、先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过__________ 、冷却、___________ (填写操作名称)除去NaCl
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和 ,相应的化学方程式为
,相应的化学方程式为______________________ 。

(7)电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2____________ (填“>”、“=”或“<”)2L,原因是_____________________ 。
(8)实验室制备H2和Cl2通常采用下列反应:Zn+H2SO4→ZnSO4+H2↑、MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O

据此,制备并收集干燥、纯净Cl2的装置是______ (填代号)。

依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为
(2)工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是
a、Ba(OH)2 b、Ba(NO3)2 c、BaCl2
(4)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为
a、先加NaOH,后加Na2CO3,再加钡试剂
b、先加NaOH,后加钡试剂,再加Na2CO3
c、先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和
 ,相应的化学方程式为
,相应的化学方程式为
(7)电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2
(8)实验室制备H2和Cl2通常采用下列反应:Zn+H2SO4→ZnSO4+H2↑、MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
据此,制备并收集干燥、纯净Cl2的装置是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】含氯化合物KClO3和NaClO广泛应用于杀菌、消毒及化工领域。甲同学利用下图装置(部分装置省略)制备KClO3和NaClO,并探究其性质。

已知b、c中的试管分别盛装的是15 mL 30% KOH溶液、15 mL 8% NaOH溶液。
回答下列问题:
(1)盛放浓盐酸的仪器名称是_______ ;a中的试剂为_______ ,若取消此装置,对该实验的影响是_______ 。
(2)比较制取KClO3和NaClO的条件,二者的差异是:①_______ ;②_______ 。
(3)取少量的KClO3溶液和NaClO溶液分别置于两支试管中,分别滴加KI溶液。盛装KClO3溶液的试管中颜色不变;盛装NaClO溶液的试管中,溶液变为棕色,该试管中反应的离子方程式为_______ ,可证明氧化能力KClO3_______ NaClO(填“大于”或“小于”)。
(4)装置c中制备的NaClO中混有杂质NaCl,为测定混合物中NaClO的含量,乙同学进行了如下实验。称取3.0 g样品于锥形瓶中,加适量水使其完全溶解,调pH,向溶液中加入40 mL 3.0 mol·L-1的FeSO4溶液(过量),充分反应,再向反应后的溶液中滴加1.0 mol·L-1的K2Cr2O7溶液,当Fe2+恰好完全反应时消耗K2Cr2O7溶液10.00 mL。
①滴入K2Cr2O7溶液前,锥形瓶中发生反应的离子方程式为_______ ;
②样品中NaClO的质量分数为_______ %(精确到0.1%)。

已知b、c中的试管分别盛装的是15 mL 30% KOH溶液、15 mL 8% NaOH溶液。
回答下列问题:
(1)盛放浓盐酸的仪器名称是
(2)比较制取KClO3和NaClO的条件,二者的差异是:①
(3)取少量的KClO3溶液和NaClO溶液分别置于两支试管中,分别滴加KI溶液。盛装KClO3溶液的试管中颜色不变;盛装NaClO溶液的试管中,溶液变为棕色,该试管中反应的离子方程式为
(4)装置c中制备的NaClO中混有杂质NaCl,为测定混合物中NaClO的含量,乙同学进行了如下实验。称取3.0 g样品于锥形瓶中,加适量水使其完全溶解,调pH,向溶液中加入40 mL 3.0 mol·L-1的FeSO4溶液(过量),充分反应,再向反应后的溶液中滴加1.0 mol·L-1的K2Cr2O7溶液,当Fe2+恰好完全反应时消耗K2Cr2O7溶液10.00 mL。
①滴入K2Cr2O7溶液前,锥形瓶中发生反应的离子方程式为
②样品中NaClO的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某化学小组为了证明二氧化硫和氯水的漂白性,设计了如图所示的实装置:
(1)用来制取氯气的装置是___________ (填字母序号)。
(2)反应开始一段时间后,B、D试管中的品红溶液均褪色。停止通气后,再将B、D两个试管分别加热,___________ (填“B”或“D”)试管中无明显现象。
(3)装置C的主要作用是______________________ 。
(4)该小组同学将两种气体混合后通入品红溶液中,发现漂白效果并不像预期的一样增强。查阅资料得知:两种气体混合,再与水反应可生成两种常见的酸,因而漂白作用减弱,该反应的化学方程式是_________________________ 。

(1)用来制取氯气的装置是
(2)反应开始一段时间后,B、D试管中的品红溶液均褪色。停止通气后,再将B、D两个试管分别加热,
(3)装置C的主要作用是
(4)该小组同学将两种气体混合后通入品红溶液中,发现漂白效果并不像预期的一样增强。查阅资料得知:两种气体混合,再与水反应可生成两种常见的酸,因而漂白作用减弱,该反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】水合肼(N2H4∙H2O)可用作抗氧剂等,常用尿素[CO(NH2)2]和NaClO 溶液反应制备水合肼与无水Na2SO3.已知:①Cl2+2OH-=ClO- +Cl- +H2O是放热反应;②N2H4∙H2O沸点118℃,具有强还原性,能与NaClO剧烈反应生成氮气。
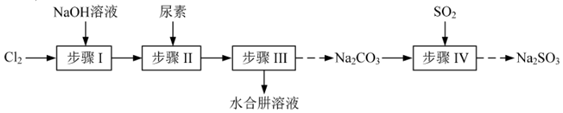
I.制备NaClO溶液
(1)步骤I制备NaClO溶液时,若温度超过40℃,有副反应发生生成 NaClO3,该副反应的离子方程式为_______ 。为了避免副反应的发生除了用冰水浴降温,还可以采取的措施有_______ 。
II.制取水合肼:合成N2H4∙H2O的装置如图1所示。
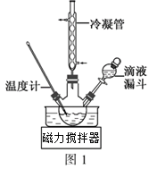
(2)图1中NaClO碱性溶液与尿素CO(NH2)2水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。实验中通过滴液漏斗滴加的溶液是_______ (填“NaClO碱性溶液”或“CO(NH2)2水溶液”);使用冷凝管的目的是_______ 。
(3)三颈烧瓶中反应的化学方程式_______ 。
III.步骤IV用步骤III得到的副产品Na2CO3制备无水Na2SO3,水溶液中H2SO3、 、
、 随pH的分布如图2所示,Na2SO3的溶解度曲线如图3所示。
随pH的分布如图2所示,Na2SO3的溶解度曲线如图3所示。
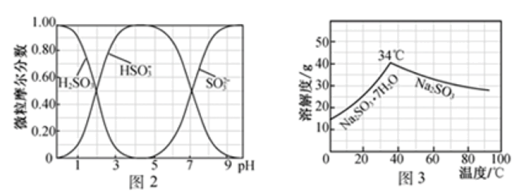
(4)边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液,实验中当溶液pH约为_______ 停止通SO2。
(5)请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案:边搅拌边向NaHSO3溶液中滴加NaOH溶液,测量溶液pH,pH约为10时,停止滴加NaOH溶液,加热浓缩溶液至有大量晶体析出,_______ ,用少量无水乙醇洗涤,干燥,密封包装。

I.制备NaClO溶液
(1)步骤I制备NaClO溶液时,若温度超过40℃,有副反应发生生成 NaClO3,该副反应的离子方程式为
II.制取水合肼:合成N2H4∙H2O的装置如图1所示。

(2)图1中NaClO碱性溶液与尿素CO(NH2)2水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。实验中通过滴液漏斗滴加的溶液是
(3)三颈烧瓶中反应的化学方程式
III.步骤IV用步骤III得到的副产品Na2CO3制备无水Na2SO3,水溶液中H2SO3、
 、
、 随pH的分布如图2所示,Na2SO3的溶解度曲线如图3所示。
随pH的分布如图2所示,Na2SO3的溶解度曲线如图3所示。
(4)边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液,实验中当溶液pH约为
(5)请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案:边搅拌边向NaHSO3溶液中滴加NaOH溶液,测量溶液pH,pH约为10时,停止滴加NaOH溶液,加热浓缩溶液至有大量晶体析出,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】钠和氯是我们熟悉的典型金属元素与非金属元素,研究它们的性质对于生产、生活、科研具有重要意义。
Ⅰ.某化学兴趣小组为了探究“干燥的 不能与
不能与 反应”而“潮湿的
反应”而“潮湿的 能与
能与 反应”,设计了如图1所示装置进行实验(夹持仪器已省略)。
反应”,设计了如图1所示装置进行实验(夹持仪器已省略)。

回答下列问题:
(1)实验开始前先通入一段时间的 ,目的是
,目的是___________ 。
(2)饱和 溶液的作用是
溶液的作用是___________ ,试剂 是
是___________
(3)实验时,首先打开装置A中分液漏斗的活塞,加入稀盐酸;然后关闭 ,打开
,打开 ,实验中观察到E中灼热的铜丝颜色未发生变化,则得出的结论是
,实验中观察到E中灼热的铜丝颜色未发生变化,则得出的结论是___________ 。
(4)写出 中
中 与
与 反应的化学方程式
反应的化学方程式___________ 。
Ⅱ.为探究氯气的性质,某同学利用此原理制氯气并设计了如图2所示的实验装置(A为氯气制取装置,未画出)。

(5)装置B、C中依次盛放的是干燥的红色布条和湿润的红色布条,其目的是证明干燥的氯气不具有漂白性。实验过程中该同学发现装置B中的布条也褪色,说明该装置存在明显的缺陷,改进的方法是___________ 。
(6)E中 溶液吸收氯气时发生反应的离子方程式是
溶液吸收氯气时发生反应的离子方程式是___________ 。
(7)D中氯气可将 氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是
氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是___________ (提示: 遇盐酸生成
遇盐酸生成 气体。写出操作试剂和现象)
气体。写出操作试剂和现象)
Ⅰ.某化学兴趣小组为了探究“干燥的
 不能与
不能与 反应”而“潮湿的
反应”而“潮湿的 能与
能与 反应”,设计了如图1所示装置进行实验(夹持仪器已省略)。
反应”,设计了如图1所示装置进行实验(夹持仪器已省略)。
回答下列问题:
(1)实验开始前先通入一段时间的
 ,目的是
,目的是(2)饱和
 溶液的作用是
溶液的作用是 是
是(3)实验时,首先打开装置A中分液漏斗的活塞,加入稀盐酸;然后关闭
 ,打开
,打开 ,实验中观察到E中灼热的铜丝颜色未发生变化,则得出的结论是
,实验中观察到E中灼热的铜丝颜色未发生变化,则得出的结论是(4)写出
 中
中 与
与 反应的化学方程式
反应的化学方程式Ⅱ.为探究氯气的性质,某同学利用此原理制氯气并设计了如图2所示的实验装置(A为氯气制取装置,未画出)。

(5)装置B、C中依次盛放的是干燥的红色布条和湿润的红色布条,其目的是证明干燥的氯气不具有漂白性。实验过程中该同学发现装置B中的布条也褪色,说明该装置存在明显的缺陷,改进的方法是
(6)E中
 溶液吸收氯气时发生反应的离子方程式是
溶液吸收氯气时发生反应的离子方程式是(7)D中氯气可将
 氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是
氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是 遇盐酸生成
遇盐酸生成 气体。写出操作试剂和现象)
气体。写出操作试剂和现象)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某学习小组用MnO2和浓盐酸共热制取氯气,再用氯气与潮湿的消石灰反应制取漂白粉(这是一个放热反应)。
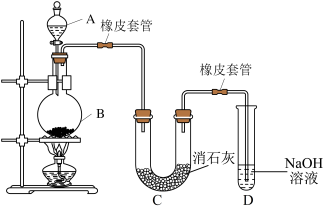
(1)圆底烧瓶内发生反应的化学方程式为_______ ;
(2)漂粉精在空气中起漂白作用的原理是_______ (用化学方程式表示)。
(3)此实验Ca(ClO)2产率太低。经分析发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是_______ 。
②试判断另一个副反应:_______ (用化学方程式表示)。

(1)圆底烧瓶内发生反应的化学方程式为
(2)漂粉精在空气中起漂白作用的原理是
(3)此实验Ca(ClO)2产率太低。经分析发现,主要原因是在U形管中存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
②试判断另一个副反应:
您最近一年使用:0次


 )
)

