下表为元素周期表的一部分,请根据所学知识回答下列问题:

(1)写出J在周期表中的位置___________ 。
(2)B、D、E的简单离子半径由大到小的顺序是___________ (填离子符号)。
(3)上述元素的原子中,写出未成对电子数最多的元素基态原子的核外电子排布式:___________ 。
(4)上述7种元素中金属性最强的元素与B可形成原子个数比为1:1的化合物甲,则甲的电子式为___________ 。
(5)判断B和D的非金属性强弱,并从结构角度说明原因:___________ 。

(1)写出J在周期表中的位置
(2)B、D、E的简单离子半径由大到小的顺序是
(3)上述元素的原子中,写出未成对电子数最多的元素基态原子的核外电子排布式:
(4)上述7种元素中金属性最强的元素与B可形成原子个数比为1:1的化合物甲,则甲的电子式为
(5)判断B和D的非金属性强弱,并从结构角度说明原因:
更新时间:2023/10/25 23:41:32
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】短周期元素a、b、c、d在元素周期表中的相对位置如图所示,其中d在同周期中原子半径最小。回答下列问题:
(1)属于碱金属元素的有___ (填元素符号)。
(2)d在元素周期表中的位置是___ 。
(3)写出由a、b形成的既含极性键又含非极性键的化合物的电子式:___ 。
(4)如图表示某些物质之间的转化关系,其中化合物A是由c、d两种元素组成的二元化合物,L为b的一种单质;常温下M为深红棕色液体,Q可用来检验淀粉的存在。
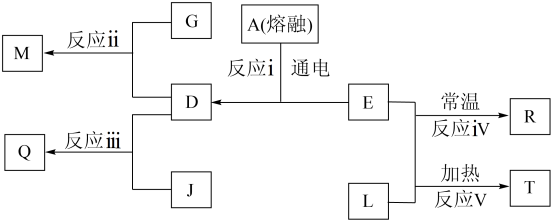
①化合物A在熔融时的电离方程式是___ 。
②反应ⅱ、反应ⅲ说明元素非金属性的强弱关系是___ (用元素符号表示)。
③写出T与水反应的离子方程式:___ 。
| a | |||||
| …… | b | ||||
| c | d | ||||
(2)d在元素周期表中的位置是
(3)写出由a、b形成的既含极性键又含非极性键的化合物的电子式:
(4)如图表示某些物质之间的转化关系,其中化合物A是由c、d两种元素组成的二元化合物,L为b的一种单质;常温下M为深红棕色液体,Q可用来检验淀粉的存在。

①化合物A在熔融时的电离方程式是
②反应ⅱ、反应ⅲ说明元素非金属性的强弱关系是
③写出T与水反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物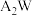 和
和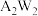 ,E元素的周期序数与主族序数相等。
,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置________ 。将B过量的最高价氧化物通入E的含氧酸盐溶液中,可以观察到的现象为_____ 。
(2)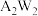 分子中存在的,不同于
分子中存在的,不同于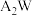 中的化学键被称为
中的化学键被称为_______ 。用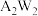 和稀硫酸浸泡废印刷电路板可溶解其中的
和稀硫酸浸泡废印刷电路板可溶解其中的 ,试写出反应的离子方程式
,试写出反应的离子方程式___________ 。
(3) 和入足量的水充分反应,生成气体的体积为
和入足量的水充分反应,生成气体的体积为_______ (标准状况下).
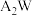 和
和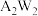 ,E元素的周期序数与主族序数相等。
,E元素的周期序数与主族序数相等。(1)E元素在周期表中的位置
(2)
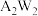 分子中存在的,不同于
分子中存在的,不同于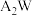 中的化学键被称为
中的化学键被称为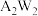 和稀硫酸浸泡废印刷电路板可溶解其中的
和稀硫酸浸泡废印刷电路板可溶解其中的 ,试写出反应的离子方程式
,试写出反应的离子方程式(3)
 和入足量的水充分反应,生成气体的体积为
和入足量的水充分反应,生成气体的体积为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
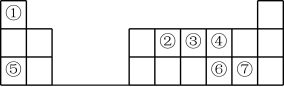
【推荐3】元素周期表的建立是化学发展史上重要的里程碑之一,它揭示了元素之间的内在联系。如图是元素周期表的短周期示意图,相应方格中每个序号代表处于该位置的一种元素。
(1)元素①的名称为___________ 。
(2)元素③的最高价氧化物的水化物___________ (填化学式)
(3)⑥和⑦两种元素的气态氢化物中稳定性较强的是___________ (填化学式)。
(4)②和④两种元素形成的常见气态化合物中化学键类型为___________ 。
(5)⑦的单质与⑤的最高价氧化物对应水化物反应的化学方程式为___________ 。
(1)元素①的名称为
(2)元素③的最高价氧化物的水化物
(3)⑥和⑦两种元素的气态氢化物中稳定性较强的是
(4)②和④两种元素形成的常见气态化合物中化学键类型为
(5)⑦的单质与⑤的最高价氧化物对应水化物反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】现有A、B、C、D四种短周期元素,A元素形成的-2价阴离子比氦原子的核外电子数多8个,B元素与A元素可组成一种化合物E,为淡黄色固体,该固体遇到潮湿的空气能生成A的单质;A、C元素原子最外层电子数相同;D元素原子的M层上有7个电子。
(1)写出D元素在周期表中的位置_______ 。
(2)A、C两种元素的简单气态氢化物的稳定性由强到弱为_______ 。(用化学式表示)
(3)写出淡黄色固体E的电子式_______ 。
(4)A2和A3互为_______ 。(填字母代号)
A.同位素 B.同素异形体
(5)B、C、D三种元素的简单离子半径从大到小的顺序是_______ 。(用离子符号表示)
(6)D的单质与B的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(1)写出D元素在周期表中的位置
(2)A、C两种元素的简单气态氢化物的稳定性由强到弱为
(3)写出淡黄色固体E的电子式
(4)A2和A3互为
A.同位素 B.同素异形体
(5)B、C、D三种元素的简单离子半径从大到小的顺序是
(6)D的单质与B的最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】如图是部分短周期元素的常见化合价与原子序数的关系:
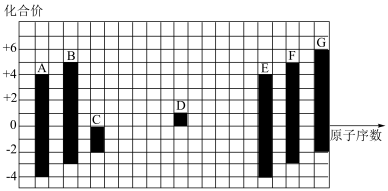
回答下列问题:
(1)E元素为__________ (填元素符号,下同);F元素为__________ 。
(2)C、D、G的离子半径由大到小的顺序是__________ (用元素符号表示)。
(3)最简单氢化物的热稳定性:B__________ (填“>”或“<”)C。
(4)C与D形成的具有强氧化性的化合物为__________ ,该化合物与 反应的化学方程式为
反应的化学方程式为________________________________________ ,其中氧化剂与还原剂的物质的量之比为__________ 。

回答下列问题:
(1)E元素为
(2)C、D、G的离子半径由大到小的顺序是
(3)最简单氢化物的热稳定性:B
(4)C与D形成的具有强氧化性的化合物为
 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】下表是元素周期表的一部分,回答下列有关问题:
(1)h的原子结构示意图是_______ 。
(2)c、d、e的简单离子半径由大到小的顺序是_______ (填离子符号)。
(3)d、f、g的气态氢化物的稳定性由强到弱的顺序_______ (填化学式)。
(4)a、c和e三种元素形成化合物含_______ (填化学键类型),它的电子式为_______ 。
(5)用电子式表示由a、g两元素组成的化合物的形成过程:_______ 。
| 周期 | IA | |||||||
| 1 | a | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | b | c | d | |||||
| 3 | e | f | g | |||||
| 4 | h |
(2)c、d、e的简单离子半径由大到小的顺序是
(3)d、f、g的气态氢化物的稳定性由强到弱的顺序
(4)a、c和e三种元素形成化合物含
(5)用电子式表示由a、g两元素组成的化合物的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】A、B、C、D、E、F是原子序数依次增大的6种短周期主族元素。A元素是动植物生长不可缺少的元素,其单质在空气中含量最高;B元素的最外层电子数是其电子层数的3倍;短周期主族元素中C原子半径最大;C、D、E的最高价氧化物对应水化物两两之间都能反应,元素E最高正化合价与最低负化合价的代数和为4。回答下列问题:
(1)A元素组成单质的电子式_____________ 。E和F的最高价氧化物对应水化物酸性更强的是_____________ (填化学式)。
(2)B、C、D、E四种元素简单离子的离子半径由大到小 的顺序是(填具体的离子符号):______________________ ;
(3)C和B能形成C2B和C2B2两种化合物,用电子式请写出C2B2的形成过程:
_________________________________ 。
(4)已知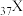 和
和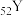 都位于第五周期,分别与C和E同一主族。下列有关说法正确的是_____________(填字母序号);
都位于第五周期,分别与C和E同一主族。下列有关说法正确的是_____________(填字母序号);
(5)下列物质的变化中未发生化学键破坏的是_____________ (填序号,下同),仅发生离子键破坏的是_____________ ,仅发生共价键破坏的是_____________ ,既发生离子键破坏,又发生共价键破坏的是________________________ .
①氯化钠溶于水、②氯化氢溶于水、③乙醇溶于水、④过氧化钠与水反应、⑤碘升华.
(6)A、B组成的一种无色气体遇空气变为红棕色。将标准状况下40 L该无色气体与15 L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐和水。请写出该反应的离子方程式_____________ 。
(1)A元素组成单质的电子式
(2)B、C、D、E四种元素简单离子的离子半径
(3)C和B能形成C2B和C2B2两种化合物,用电子式请写出C2B2的形成过程:
(4)已知
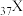 和
和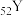 都位于第五周期,分别与C和E同一主族。下列有关说法正确的是_____________(填字母序号);
都位于第五周期,分别与C和E同一主族。下列有关说法正确的是_____________(填字母序号);| A.原子半径:X>Y | B.最高价氧化物对应水化物的碱性强弱:X>C |
| C.气态氢化物稳定性强弱:E>Y | D.B与C形成的化合物中不可能含有共价键 |
①氯化钠溶于水、②氯化氢溶于水、③乙醇溶于水、④过氧化钠与水反应、⑤碘升华.
(6)A、B组成的一种无色气体遇空气变为红棕色。将标准状况下40 L该无色气体与15 L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐和水。请写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表列出9种元素在元素周期表(元素周期表只给出部分)中的位置
请回答下列问题:
(1)考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的元素符号是_____ 。
(2)写出由元素②和元素④形成原子个数比为1∶2的化合物的电子式_____ 。某短周期元素的最高正化合价与最低负化合价的代数和为4,该元素在周期表的位置为_____ 。
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物反应的离子方程式为_____ 。
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是_____ (填化学式;用“>”连接)。元素④、⑤、⑧所形成的简单离子半径由大到小的顺序是_____ (用化学符号表示)。
(5)由①、③、⑧三种元素以原子个数比4∶1∶1形成的化合物中含有的化学键类型是_____ (选填“离子键”“极性键”“非极性键”)
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | |||||
| 4 | ⑨ |
(1)考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的元素符号是
(2)写出由元素②和元素④形成原子个数比为1∶2的化合物的电子式
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物反应的离子方程式为
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是
(5)由①、③、⑧三种元素以原子个数比4∶1∶1形成的化合物中含有的化学键类型是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是: (填具体元素符号或化学式,下同),非金属性最强的元素是: 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是:_______,碱性最强的化合物的化学式是:_____________。
(3)最高价氧化物是两性氧化物的元素是:_________;写出它的最高价氧化物与氢氧化钠反应的离子方程式:____________________________________。
(4)④与⑧形成的化合物的电子式是: ,该化合物所含化学键类型是: (填“共价键”或“离子键”)。
(5)试设计实验方案比较④与⑤的化学性质(金属性),有关实验步骤、现象和结论填入下表
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是:_______,碱性最强的化合物的化学式是:_____________。
(3)最高价氧化物是两性氧化物的元素是:_________;写出它的最高价氧化物与氢氧化钠反应的离子方程式:____________________________________。
(4)④与⑧形成的化合物的电子式是: ,该化合物所含化学键类型是: (填“共价键”或“离子键”)。
(5)试设计实验方案比较④与⑤的化学性质(金属性),有关实验步骤、现象和结论填入下表
| 实验步骤 | 实验现象与结论 |
您最近一年使用:0次
【推荐1】元素周期表中前四周期几种主族元素的位置关系如图所示(过渡元素已忽略)。
请回答下列问题。
(1)①和②能形成简单化合物,该物质的化学式为_______ ,已知该物质为离子化合物,两种离子半径①_______ ②(填“>”“<”或“=”)。
(2)④、⑤、⑥三种元素的第一电离能由大到小的顺序为_______ (用元素符号表示,下同),电负性由大到小的顺序为_______ 。
(3)③、⑨、⑪分别与①形成简单二元化合物,三种物质的热稳定性从强到弱的顺序为_______ (用化学式表示)。
(4)元素⑦的基态原子的电子排布式为_______ ,其电子占据的最高能级的轨道形状为_______ 。
(5)元素⑩的焰色为紫色,从微观角度解释元素产生焰色反应的原因_______ 。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||||||||||||
| ⑩ | ⑾ |
(1)①和②能形成简单化合物,该物质的化学式为
(2)④、⑤、⑥三种元素的第一电离能由大到小的顺序为
(3)③、⑨、⑪分别与①形成简单二元化合物,三种物质的热稳定性从强到弱的顺序为
(4)元素⑦的基态原子的电子排布式为
(5)元素⑩的焰色为紫色,从微观角度解释元素产生焰色反应的原因
您最近一年使用:0次
【推荐2】下表为元素周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)表中属于d区的元素是________ (填编号),其原子结构示意图是 ________________ 。
(2)写出元素⑩的基态原子的简化电子排布式:________________________________ 。
(3)某元素的特征电子排布式为 ,该元素是
,该元素是 ________ (填名称),原子的最外层电子的成对电子为 ________ 对。
(4)③和④的简单气态氢化物最稳定的是________ (填化学式,下同),⑦的最强含氧酸为 ________ 。
(5)⑦和③形成的化合物的电子式是________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | |||||||||||||||
| ⑧ | ⑨ | ⑩ |
(1)表中属于d区的元素是
(2)写出元素⑩的基态原子的简化电子排布式:
(3)某元素的特征电子排布式为
 ,该元素是
,该元素是 (4)③和④的简单气态氢化物最稳定的是
(5)⑦和③形成的化合物的电子式是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】按下列要求填空。
(1)基态某原子的最外层电子排布式是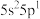 ,推断该元素位于第五周期第
,推断该元素位于第五周期第___________ 族,该元素的最高正化合价为___________ ,在元素周期表中属于___________ 区。
(2)基态某原子的价层电子排布式为 ,推断该元素位于第五周期第
,推断该元素位于第五周期第___________ 族,在元素周期表中属于___________ 区。
(3)比较大小(填“>”或“<”)。
①键长:
___________ 
②键能:
___________ 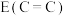
③键角:
___________ 
④键的极性:
___________ 
⑤沸点:
___________ CO
⑥酸性:HCOOH___________ 
(4)HCN中心原子“C”的杂化类型为___________ ,VSEPR模型为___________ ,分子空间构型为___________ 。
(1)基态某原子的最外层电子排布式是
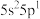 ,推断该元素位于第五周期第
,推断该元素位于第五周期第(2)基态某原子的价层电子排布式为
 ,推断该元素位于第五周期第
,推断该元素位于第五周期第(3)比较大小(填“>”或“<”)。
①键长:


②键能:

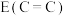
③键角:


④键的极性:


⑤沸点:

⑥酸性:HCOOH

(4)HCN中心原子“C”的杂化类型为
您最近一年使用:0次



