ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过如图装置(夹持装置略)对制备ClO2、并在吸收、释放和应用进行了研究。

(1)仪器B的名称是___________ 。安装F中导管时,应选用如图中的___________ 。

(2)打开B的活塞,A中发生反应生成ClO2和Cl2,其氧化产物和还原产物的物质的量之比为___________ ,为使产生的ClO2气流稳定,在D中被充分吸收,应___________ 。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是___________ 。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为___________ ,在ClO2释放实验中,打开E中的活塞,D中发生反应,则装置F的作用是___________ 。
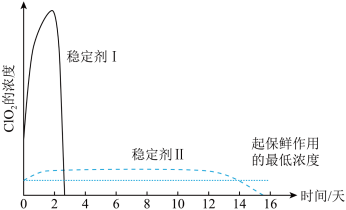
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图所示。若将其用于水果保鲜,你认为效果较好的稳定剂是___________ ,原因是___________ 。

(1)仪器B的名称是

(2)打开B的活塞,A中发生反应生成ClO2和Cl2,其氧化产物和还原产物的物质的量之比为
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图所示。若将其用于水果保鲜,你认为效果较好的稳定剂是

更新时间:2023-11-30 08:46:23
|
相似题推荐
【推荐1】“雾霾”成为人们越来越关心的环境问题。雾霾中含有二氧化硫、氮氧化物和可吸入颗粒物等污染性物质。请回答下列问题:
(1)汽车尾气是雾霾形成的原因之一。尾气治理可用汽油中挥发出来的烃类物质(CxHy)催化还原尾气中的NO气体,该过程的化学方程式为___ 。
(2)冬季燃煤供暖产生的废气也是雾霾的主要来源之一。发现将煤炭在O2/CO2的气氛下燃烧,能够降低燃煤时NO的排放,主要反应为:2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH
N2(g)+2CO2(g) ΔH
已知:①N2(g)+O2(g) 2NO(g) ΔH1=+180.5kJ·mol-1
2NO(g) ΔH1=+180.5kJ·mol-1
②2CO(g) 2C(s)+O2(g) ΔH2=+221kJ·mol-1
2C(s)+O2(g) ΔH2=+221kJ·mol-1
③C(s)+O2(g) CO2(g) ΔH3=-393.5kJ·mol-1
CO2(g) ΔH3=-393.5kJ·mol-1
则ΔH=___ 。
(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图所示,电极材料为石墨。
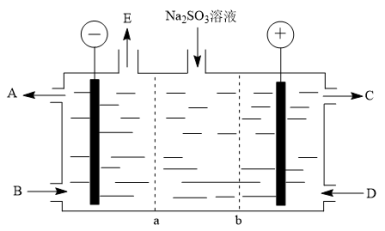
①a表示___ 离子交换膜(填“阴”或“阳”)。A~E分别代表生产中的原料或产品,其中C为硫酸,则A表示___ ,E表示___ 。
②生成C时,阳极的电极反应式为___ 。
(1)汽车尾气是雾霾形成的原因之一。尾气治理可用汽油中挥发出来的烃类物质(CxHy)催化还原尾气中的NO气体,该过程的化学方程式为
(2)冬季燃煤供暖产生的废气也是雾霾的主要来源之一。发现将煤炭在O2/CO2的气氛下燃烧,能够降低燃煤时NO的排放,主要反应为:2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH
N2(g)+2CO2(g) ΔH已知:①N2(g)+O2(g)
 2NO(g) ΔH1=+180.5kJ·mol-1
2NO(g) ΔH1=+180.5kJ·mol-1②2CO(g)
 2C(s)+O2(g) ΔH2=+221kJ·mol-1
2C(s)+O2(g) ΔH2=+221kJ·mol-1③C(s)+O2(g)
 CO2(g) ΔH3=-393.5kJ·mol-1
CO2(g) ΔH3=-393.5kJ·mol-1则ΔH=
(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图所示,电极材料为石墨。

①a表示
②生成C时,阳极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】工业上以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3)。其工业流程如下图所示:

(1)“过滤Ⅰ”所得“滤渣Ⅰ”的主要成分为_________ (填化学式)。
(2)“氧化”过程中除了发生MnO2与SO2的反应外,还发生另一氧化还原反应,写出该反应的离子方程式______________________________________________________________ 。
(3)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少MnS2O6的生成,“浸锰”的适宜温度是____________________________________ 。

(4)向“过滤Ⅱ”所得的滤液中加入NH4HCO3溶液时温度控制在30~35 ℃,温度不宜太高的原因是_________________________________________________________________ 。
(5)加入NH4HCO3溶液后,生成MnCO3沉淀,同时还有CO2气体生成,写出反应的离子方程式:_____________________________________________________________________ 。
(6)生成的MnCO3沉淀需经充分洗涤,检验沉淀是否洗涤干净的方法是___________________________________________________________________________ 。

(1)“过滤Ⅰ”所得“滤渣Ⅰ”的主要成分为
(2)“氧化”过程中除了发生MnO2与SO2的反应外,还发生另一氧化还原反应,写出该反应的离子方程式
(3)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少MnS2O6的生成,“浸锰”的适宜温度是

(4)向“过滤Ⅱ”所得的滤液中加入NH4HCO3溶液时温度控制在30~35 ℃,温度不宜太高的原因是
(5)加入NH4HCO3溶液后,生成MnCO3沉淀,同时还有CO2气体生成,写出反应的离子方程式:
(6)生成的MnCO3沉淀需经充分洗涤,检验沉淀是否洗涤干净的方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下列各物质是中学化学中常见的物质,甲为常见金属单质,乙、丙、丁是非金属单质,其它为化合物,B、D分别为黑色粉末和黑色晶体,G为淡黄色固体,J为生活中常见的调味品,I为红褐色固体,①是实验室制取丁的反应之一,F为棕黄色溶液。各物质间的转化如下图所示,回答下列各问题(部分生成物未列出):
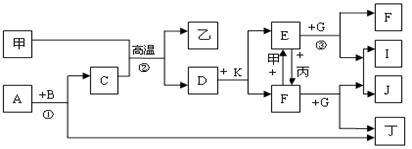
(1)写出乙的化学式_______ 、A的电子式_________ 、甲在周期表中位置是__________ ;
(2)写出G的一种用途____________________ ;
(3)写出B与K的浓溶液反应的化学方程式:_______________________________ ;
(4)整个转换过程中属于氧化还原反应的数目有__________ 个;
(5)写出反应③E与A按物质的量之比2:1的反应的离子方程式___ 。

(1)写出乙的化学式
(2)写出G的一种用途
(3)写出B与K的浓溶液反应的化学方程式:
(4)整个转换过程中属于氧化还原反应的数目有
(5)写出反应③E与A按物质的量之比2:1的反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】磺酰氯(SO2Cl2)可用于制造锂电池正极活性物质。实验室可利用SO2和Cl2在活性炭催化下反应制取少量SO2Cl2,装置如图(部分夹持装置已省略)。
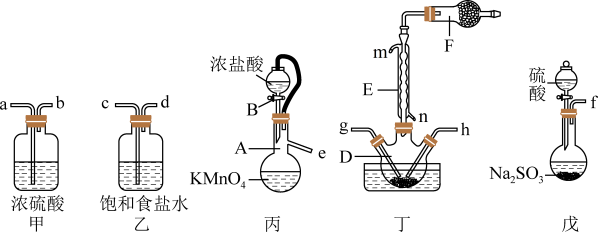
已知:①SO2(g)+Cl2(g)=SO2Cl2(l);伴随反应进行,过程中会放出热量;
②SO2Cl2熔点为-54.1℃,沸点69.1℃,常温较稳定。遇水剧烈反应,100℃以上易分解;
③装置丙中利用KMnO4与浓盐酸的反应产生出Cl2;
装置戊中反应方程式为: 。
。
④
回答下列问题:
(1)仪器E的名称是___________ ,水从___________ 口进入(选填“m”或“n”):仪器F中盛放的固体的成分可以是___________ 。
(2)装置乙的作用是___________ 。去除装置甲可能会降低SO2Cl2的产量,原因可能是___________ 。
(3)配平下列氧化还原反应方程式,并用单线桥法标出电子转移的方向和数目___________ 。

(4)装置丁中三颈烧瓶置于冷水浴中,其原因是___________ 。
(5)某实验小组利用该装置消耗了标准状况下氯气1120 mL(SO2足量),最后得到纯净的磺酰氯4.0 g,则磺酰氯的产率为___________ 。

已知:①SO2(g)+Cl2(g)=SO2Cl2(l);伴随反应进行,过程中会放出热量;
②SO2Cl2熔点为-54.1℃,沸点69.1℃,常温较稳定。遇水剧烈反应,100℃以上易分解;
③装置丙中利用KMnO4与浓盐酸的反应产生出Cl2;
装置戊中反应方程式为:
 。
。④

回答下列问题:
(1)仪器E的名称是
(2)装置乙的作用是
(3)配平下列氧化还原反应方程式,并用单线桥法标出电子转移的方向和数目

(4)装置丁中三颈烧瓶置于冷水浴中,其原因是
(5)某实验小组利用该装置消耗了标准状况下氯气1120 mL(SO2足量),最后得到纯净的磺酰氯4.0 g,则磺酰氯的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室用如图装置制取SnCl4,SnCl4遇水强烈水解,产生大量白烟。回答下列问题:
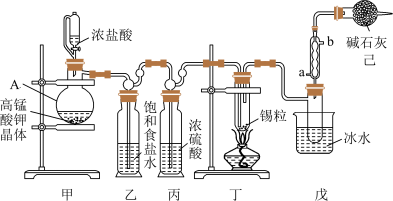
(1)甲装置中盛放浓盐酸的仪器名称________ ,其中导管的作用是________________
(2)装置乙、丙中球泡的作用是________________
(3)装置己的作用是____________________________________________________

(1)甲装置中盛放浓盐酸的仪器名称
(2)装置乙、丙中球泡的作用是
(3)装置己的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】高铁酸盐是优良的多功能水处理剂。K2FeO4为紫色固体,可溶于水,微溶于浓 KOH溶液,难溶于有机物;在0~5℃、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O2,现某实验小组制备高铁酸钾(K2FeO4)装置如图所示,夹持、加热等装置略。回答下列问题:
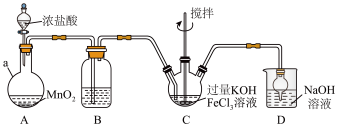
(1)仪器a的名称是_______ ,装置 B中除杂质所用试剂是_______ 、装置D的作用是_______ 。
(2)装置C反应中 KOH必须过量的原因是_______ 。
(3)C中制备高铁酸钾的化学反应:3Cl2+2FeCl3+16KOH = 2K2FeO4+12KCl+8H2O,写出该反应的离子方程式:_______ ,该反应中还原剂是_______ 。C中混合物经过重结晶、有机物洗涤纯化、真空干燥,得到高铁酸钾晶体。若反应过程中转移了0.6mol电子,则氧化产物的物质的量为_______ mol。

(1)仪器a的名称是
(2)装置C反应中 KOH必须过量的原因是
(3)C中制备高铁酸钾的化学反应:3Cl2+2FeCl3+16KOH = 2K2FeO4+12KCl+8H2O,写出该反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】为探究氯气与KI溶液的反应,某课外小组用下图装置进行实验(夹持仪器已略去,气密性已检验),装置A中发生反应的化学方程式为KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。

(1)盛KClO3的装置名称_______ ,KClO3的氧化性比MnO2_______ (填“强”、“弱”)。
(2)并用单线桥标出A中反应电子转移方向和数目_______ 。
(3)装置C中NaOH的作用是_______ 。
(4)为探究B中溶液颜色变化的原因,小组同学查阅资料并进行实验。
查阅资料:I2和I-在溶液中发生反应: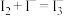 ,
, 显棕黄色且遇淀粉溶液变蓝;I2可被氯气氧化为
显棕黄色且遇淀粉溶液变蓝;I2可被氯气氧化为 (红色)和
(红色)和 (黄色),两种离子可继续被氧化成
(黄色),两种离子可继续被氧化成 (无色)。
(无色)。
进行实验:
①操作Ⅰ的实验目的是证明反应后的B溶液中有淀粉,无_______ ,说明溶液的浅棕色不是_______ 造成的。
②写出 在水溶液中与氯气反应生成
在水溶液中与氯气反应生成 的离子方程式
的离子方程式_______ 。
③由以上实验可推断B中溶液颜色变成浅棕色的原因是I-先被氯气氧化为I2,_______ 。

| 实验操作 | 实验现象 |
| 打开A中分液漏斗活塞,放下部分浓盐酸 | 装置B中溶液变蓝色,随后蓝色褪去,溶液显浅棕色 |
(2)并用单线桥标出A中反应电子转移方向和数目
(3)装置C中NaOH的作用是
(4)为探究B中溶液颜色变化的原因,小组同学查阅资料并进行实验。
查阅资料:I2和I-在溶液中发生反应:
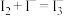 ,
, 显棕黄色且遇淀粉溶液变蓝;I2可被氯气氧化为
显棕黄色且遇淀粉溶液变蓝;I2可被氯气氧化为 (红色)和
(红色)和 (黄色),两种离子可继续被氧化成
(黄色),两种离子可继续被氧化成 (无色)。
(无色)。进行实验:
| 实验操作 | 实验现象 |
| Ⅰ.取反应后B中的溶液4mL分成两等份,第一份滴入1滴碘水;第二份滴入1滴淀粉溶液 | 第一份溶液变蓝色 第二份溶液颜色没有变化 |
| Ⅱ.将I2溶于KI溶液中配制得碘总浓度为0.1mol/L的溶液,取上述溶液2mL,滴加1滴淀粉溶液,再通入氯气 | 加淀粉溶液后变蓝,通氯气后蓝色褪去,溶液显浅棕色 |
| Ⅲ.向所得溶液继续通入氯气 | 溶液几乎变为无色 |
②写出
 在水溶液中与氯气反应生成
在水溶液中与氯气反应生成 的离子方程式
的离子方程式③由以上实验可推断B中溶液颜色变成浅棕色的原因是I-先被氯气氧化为I2,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】NaClO2是一种高效氧化剂漂白剂,某种利用 ClO2生产 NaClO2并进行尾气处理的工艺如图:
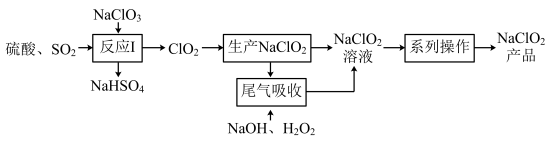
(1)写出“反应 I”中生成 ClO2的化学方程式:______ 。
(2)“尾气吸收”是为吸收未反应的 ClO2,除减少污染外,还能______ 。
(3)实验室用如图所示装置模拟“尾气吸收”过程,发现温度较低时吸收效果好,但该反应放热。在不改变吸收液浓度和体积的条件下,欲使反应在 0~5℃下进行,实验中可采取 的措施有______ 、______ 。

(4)上述流程中由NaClO2溶液 制取干燥的NaClO2产品所进行的系列操作,包括:______ 、______ 。(已知温度对 NaClO2的溶解度影响不大)

(1)写出“反应 I”中生成 ClO2的化学方程式:
(2)“尾气吸收”是为吸收未反应的 ClO2,除减少污染外,还能
(3)实验室用如图所示装置模拟“尾气吸收”过程,发现温度较低时吸收效果好,但该反应放热。在不改变吸收液浓度和体积的条件下,欲使反应在 0~5℃下进行,实验中可采取 的措施有

(4)上述流程中由NaClO2溶液 制取干燥的NaClO2产品所进行的系列操作,包括:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】I.治疗胃酸过多的药物达喜(其式量不超过 700)由五种短周期元素组成,按如下流程进行实验以确定其组成。
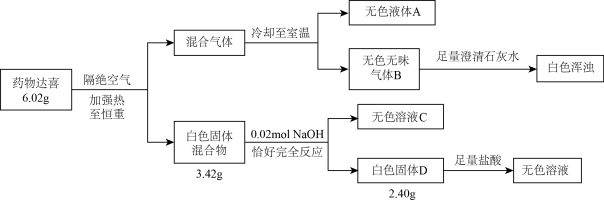
请回答:
(1)达喜的化学式是_____________ 。
(2)达喜与胃酸(含稀盐酸)反应的化学方程式是____________ 。
(3)气体 B 与环氧丙烷( )可制得一种可降解高聚物,该反应的化学方程式是
)可制得一种可降解高聚物,该反应的化学方程式是_____________________ (有机物用结构简式表示)。
II.将 NaClO3溶液逐滴加入到碘单质和过量盐酸的混合液中可制备液态 ICl,实验装置如下图:

请回答:
(1)圆底烧瓶中发生的化学反应是______________ ( 用化学方程式表示)。
(2)若加入的 NaClO3溶液已足量,请设计实验方案证明该反应已完全:_______ 。

请回答:
(1)达喜的化学式是
(2)达喜与胃酸(含稀盐酸)反应的化学方程式是
(3)气体 B 与环氧丙烷(
 )可制得一种可降解高聚物,该反应的化学方程式是
)可制得一种可降解高聚物,该反应的化学方程式是II.将 NaClO3溶液逐滴加入到碘单质和过量盐酸的混合液中可制备液态 ICl,实验装置如下图:

请回答:
(1)圆底烧瓶中发生的化学反应是
(2)若加入的 NaClO3溶液已足量,请设计实验方案证明该反应已完全:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】草酸是一种酸,草酸晶体(H2C2O4•2H2O)易溶于水,熔点较低,加热会熔化、气化和分解。草酸(H2C2O4)与氢氧化钙的反应:H2C2O4+Ca(OH)2=CaC2O4↓(白色)+2H2O。
(1)草酸的水溶液的pH___ 7(填“>”、“=”、“<”)
(2)实验室可用加热草酸晶体分解的方法获得CO。
①先加热草酸晶体生成CO、CO2和H2O,其化学方程式是____ ;
②最后用图1装置收集CO,气体应从___ 端进入(选填“a”或“b”)。

(3)实验图2中观察到澄清石灰水变浑浊,乙认为一定是由草酸晶体受热分解产生的CO2所导致,丙认为乙的结论不严密,理由是___ 。
按图3装置将草酸钙晶体(H2C2O4•xH2O)样品高温加热,使其完全分解。
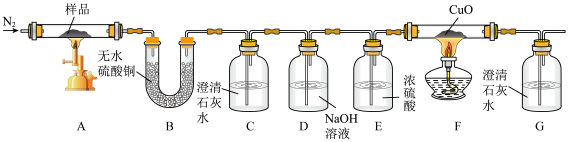
(4)B中观察到硫酸铜变蓝,说明反应生成了_____ ;
(5)C、G中澄清石灰水均变浑浊,说明反应还生成___ 和___ 气体。
(6)反应开始前通入氮气的目的是____ 。
(1)草酸的水溶液的pH
(2)实验室可用加热草酸晶体分解的方法获得CO。
①先加热草酸晶体生成CO、CO2和H2O,其化学方程式是
②最后用图1装置收集CO,气体应从

(3)实验图2中观察到澄清石灰水变浑浊,乙认为一定是由草酸晶体受热分解产生的CO2所导致,丙认为乙的结论不严密,理由是
按图3装置将草酸钙晶体(H2C2O4•xH2O)样品高温加热,使其完全分解。

(4)B中观察到硫酸铜变蓝,说明反应生成了
(5)C、G中澄清石灰水均变浑浊,说明反应还生成
(6)反应开始前通入氮气的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室里常用Na2O2与H2O反应快速制取少量的O2,下面装置用来制取O2并演示Na在O2中的燃烧实验。

(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴。判断A装置是否漏气(填“漏气”“不漏气”或“无法确定”)____ ,判断理由是____ 。
(2)写出A装置中反应的化学方程式____ 。
(3)B装置中盛放的试剂是____ ,作用是____ 。
(4)D装置中盛放的试剂是____ ,作用是____ 。

(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴。判断A装置是否漏气(填“漏气”“不漏气”或“无法确定”)
(2)写出A装置中反应的化学方程式
(3)B装置中盛放的试剂是
(4)D装置中盛放的试剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】AgNO3是中学化学常用试剂,某兴趣小组设计如下实验探究其性质。
Ⅰ.AgNO3的热稳定性
AgNO3受热易分解,用下图装置加热AgNO3固体,试管内有红棕色气体生成,一段时间后,在末端导管口可收集到无色气体a。

(1)实验室检验气体a的方法为______ 。
(2)已知B中只生成一种盐,据此判断AgNO3受热分解的化学方程式为______ 。
(3)从安全角度考虑,上述实验装置存在一处明显缺陷,改进措施为______ 。
Ⅱ.AgNO3与盐溶液的反应
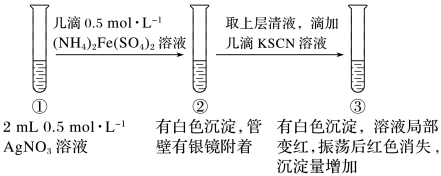
(4)甲同学认为试管②中产生银镜是Fe2+所致,其离子方程式为___ ;
(5)已知:AgSCN为白色沉淀。试管③中红色褪去的原因为___ (请从平衡移动的角度解释)。
Ⅰ.AgNO3的热稳定性
AgNO3受热易分解,用下图装置加热AgNO3固体,试管内有红棕色气体生成,一段时间后,在末端导管口可收集到无色气体a。

(1)实验室检验气体a的方法为
(2)已知B中只生成一种盐,据此判断AgNO3受热分解的化学方程式为
(3)从安全角度考虑,上述实验装置存在一处明显缺陷,改进措施为
Ⅱ.AgNO3与盐溶液的反应

(4)甲同学认为试管②中产生银镜是Fe2+所致,其离子方程式为
(5)已知:AgSCN为白色沉淀。试管③中红色褪去的原因为
您最近一年使用:0次



