| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ⑧ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 4 | ⑨ | ⑩ |
(1)在这些元素中,化学性质
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)⑩简单氢化物的VSEPR构型是
(4)用电子式表示元素④与⑥的化合物的形成过程:
(5)表示①与⑦的化合物的电子式
(6)试用一个离子方程式说明②和③的简单氢化物结合Cu2+的能力
相似题推荐
(1)单质A有两种同素异形体,其中沸点高的是
(2)C和D反应可生成组成比为1∶3的化合物E,E的空间结构为
(3)单质D与湿润的碳酸钠反应可制备D2A,其化学方程式为
(4)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566 nm,F的化学式为
(1)卤素互化物如IBr、ICl等与卤素单质结构相似、性质相近。Cl2、IBr、ICl沸点由高到低的顺序为
(2)碘原子价电子的电子排布图为
(3)I3+属于多卤素阳离子,推测I3+的空间构型为
(4)请推测①HClO4、②HIO4、③H5IO6[可写成(HO)5IO]三种物质的酸性由强到弱的顺序为
(5)离子化合物RbICl2存在复合阴离子,且晶体结构与NaCl相似,晶胞边长为685.5pm(1pm=10-12m),RbICl2晶胞中含有
(6)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为
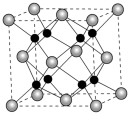
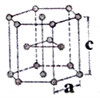
(7)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为

(1)基态铜原子价电子排布式为
(2)在Cu(NO3)2溶液中加入氨水至过量,生成[Cu(NH3)4]2+。
①
 中N原子的杂化类型是
中N原子的杂化类型是②[Cu(NH3)4]2+中提供孤对电子的基态原子有
③NH3能与Cu2+形成[Cu(NH3)4]2+,而NF3不能,其原因是
(3)黄铜合金采取面心立方堆积,其晶胞结构如图所示:
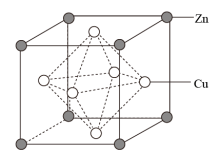
已知:晶胞参数为a nm。
①合金中粒子间作用力类型是
②与Cu原子等距离且最近的Cu原子有
③黄铜合金晶体密度为
(1)T在周期表中的位置是
(2)Y、Z、R的第一电离能由大到小的顺序为
(3)根据等电子体原理,Y2Z分子的结构式为
(4)YZ能被TRZ4溶液吸收生成配合物[T(YZ)(X2Z)5]RZ4,该配合物中含有的化学键类型有
(5)由Q与Z、R可形成多种化合物,写出Q2Z2的电子式:
Q2Z熔点比Q2R高,其原因是
(6)QX晶体的结构与NaCl相同,若Q+与最邻近X-的核间距离为a pm,阿伏伽德罗常数为NA,则QX晶体的密度为
【推荐2】铁系元素是人体必需的微量元素, Fe3+可以与KSCN溶液、苯酚等发生显色作用。镁元素也是人体所必需的阳离子元素之一,它能够维持核酸结构的稳定性,调节机体免疫功能,对人体抵抗新冠病毒等病毒侵袭起着重要作用。
(1)Fe3+的基态核外电子排布式为
(2)与SCN−互为等电子体且为非极性分子的化学式为
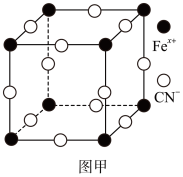
(3)普鲁士蓝俗称铁蓝,晶胞如图甲所示(K+未画出),平均每两个晶胞立方体中含有一个K+,又知该晶体中铁元素有+2价和+3价两种,则Fe3+与Fe2+的个数比为
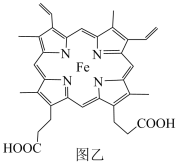
(4)血红素铁(图乙)用作铁强化剂,其吸收率比一般铁剂高3倍,在图乙中画出Fe2+与N原子间的化学键(若是配位键,需要用箭头加以表示)
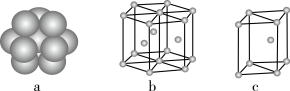
(5)镁单质晶体中原子的堆积模型如图,它的堆积模型名称为
(1)在基态Ti原子中,核外存在
(2)南京理工大学团队成功合成了能在室温稳定存在的五氮阴离子盐(N5)6(H3O)3(NH4)4Cl,五氮阴离子N5-是制备全氮类物质N5+N5-的重要中间体,下列说法不正确的是
A. (N5)6(H3O)3(NH4)4Cl中含四种离子 B. N5+N5-属于共价化合物
C. 每个N5-中含有36个电子 D. N5+N5-中既含极性键又含非极性键
(3)NH3分子空间结构为
(4)六氟合钛酸钾(K2TiF6)中存在[TiF6]2-离子,则钛元素的化合价是
(5)碳酸盐的热分解是由于晶体中阳离子结合碳酸根离子中的氧离子,使碳酸根离子分解为二氧化碳分子的结果。已知
| 碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
| 热分解温度/℃ | 402 | 900 | 1172 | 1360 |
| 阳离子半径/ pm | 66 | 99 | 112 | 135 |
请解释碱土金属元素碳酸盐热分解温度的变化规律:
(6)金属钛有两种同素异形体,常温下是六方堆积,高温下是体心立方堆积。如图所示是钛晶体的一种晶胞,晶胞参数a = 0.295nm,c=0.469nm,则该钛晶体的密度为
(1)有下列物质:①HF、②Cl2、③H2O、④CCl4、⑤BF3、⑥CO2,其中属于极性分子的是
 键又有
键又有 键的是
键的是(2)下列分子中,空间构型为正四面体且键角为
 的是
的是a.
 b.
b. c.
c.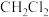 d.
d. e.
e. f.
f.
(3)H2O、
 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是(4)丙烯晴分子(
 )中碳原子杂化轨道类型为
)中碳原子杂化轨道类型为(5)VIA族元素氧、硫、硒(
 )的化合物在研究和生产中有许多重要用途。
)的化合物在研究和生产中有许多重要用途。①
 离子的空间构型为
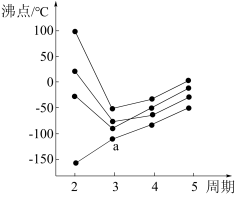
离子的空间构型为②如图所示,每条折线表示周期表IVA—VIIA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是
(1)已知:
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点/K | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度/K | 873 | 773 | 1073 | 713.2 |
分析表中四种物质的相关数据,请回答:
①CH4和SiH4比较,NH3和PH3比较,沸点高低的各自原因是
②结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时
(2)SO2与CO2分子的空间结构分别是
(3)醋酸的球棍模型如图1所示。
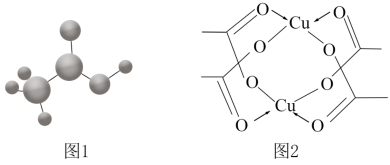
①在醋酸中,碳原子的轨道杂化类型有
②Cu的水合醋酸盐晶体局部结构如图2所示,该晶体中含有的化学键是
A.极性键 B.非极性键 C.金属键 D.配位键
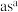 、
、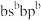 、
、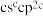 ,D与B同主族,E位于C的下一周期,且E是同周期元素中电负性最大的。试回答下列问题:
,D与B同主族,E位于C的下一周期,且E是同周期元素中电负性最大的。试回答下列问题:(1)由A、B、C、D、E五种元素中的两种或三种元素可组成多种物质,分子①
 、②
、②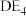 、③
、③ 、④
、④ 中,属于极性分子的是
中,属于极性分子的是 杂化的是
杂化的是(2)A、B两元素能组成一种分子中原子个数比为1:1的常见溶剂,其分子式为
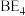 中的溶解度
中的溶解度 中的溶解度。
中的溶解度。



