有以下多种物质,请回答相关问题:
①硫酸钠②氢氧化钡③醋酸④一水合氨⑤次氯酸钠⑦乙醇
(1)上述物质的水溶液显碱性的是___________ 。(填序号)
(2)从显碱性的溶液中任选一种,用化学用语说明其显碱性的原因___________ 。(写表达式)
(3)室温下,配制浓度均为0.1 的下列五种溶液,请回答问题。
的下列五种溶液,请回答问题。
① ②
② ③
③ ④
④ ⑤
⑤
资料:某些弱酸在25℃时的电离常数如下:
①写出碳酸的第一级电离平衡常数 的计算公式
的计算公式___________ 。
②上述酸中酸性最强的是___________ 。(填化学式)
③25℃时,若次氯酸中初始 的物质的量浓度为0.01
的物质的量浓度为0.01 ,达到电离平衡时溶液中。
,达到电离平衡时溶液中。
___________ (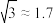 )
)
④下列反应可以发生的是___________ (填字母)。
A.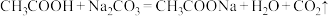
B.
C.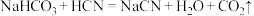
①硫酸钠②氢氧化钡③醋酸④一水合氨⑤次氯酸钠⑦乙醇
(1)上述物质的水溶液显碱性的是
(2)从显碱性的溶液中任选一种,用化学用语说明其显碱性的原因
(3)室温下,配制浓度均为0.1
 的下列五种溶液,请回答问题。
的下列五种溶液,请回答问题。①
 ②
② ③
③ ④
④ ⑤
⑤
资料:某些弱酸在25℃时的电离常数如下:
| 化学式 |  |  |  |  |  |
| 电离常数 |  | 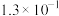 |  |  | 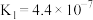  |
 的计算公式
的计算公式②上述酸中酸性最强的是
③25℃时,若次氯酸中初始
 的物质的量浓度为0.01
的物质的量浓度为0.01 ,达到电离平衡时溶液中。
,达到电离平衡时溶液中。
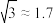 )
)④下列反应可以发生的是
A.
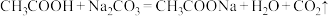
B.

C.
更新时间:2023-12-23 00:12:50
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
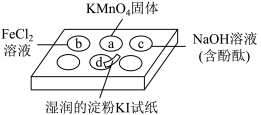
【推荐1】某学习小组利用点滴板探究氯气的性质,实验装置如图所示。
(1)可用于替代a中 的物质是___________。
的物质是___________。
(2)d中的现象是___________ ,b中离子反应方程式是___________ 。
(3)c中红色褪去,可能原因有:①氯气与氢氧化钠反应生成两种盐,溶液碱性减弱;②___________ 。请设计实验验证上述猜测___________ 。
(4)相同温度和压强下,研究 在不同溶液中的溶解度(用溶解
在不同溶液中的溶解度(用溶解 的物质的量浓度表示)随溶液浓度变化。图1为不同浓度NaCl溶液中
的物质的量浓度表示)随溶液浓度变化。图1为不同浓度NaCl溶液中 的溶解度以及其他含氯微粒(HClO、
的溶解度以及其他含氯微粒(HClO、 )浓度的变化曲线。在饱和食盐水中加入不同浓度盐酸溶液时
)浓度的变化曲线。在饱和食盐水中加入不同浓度盐酸溶液时 溶解度的变化曲线如图2所示。
溶解度的变化曲线如图2所示。 的溶解度先减小后增大。请结合图1信息,分析出现增大的可能原因为
的溶解度先减小后增大。请结合图1信息,分析出现增大的可能原因为___________ 。
(1)可用于替代a中
 的物质是___________。
的物质是___________。A. | B. | C. | D.浓硫酸 |
(3)c中红色褪去,可能原因有:①氯气与氢氧化钠反应生成两种盐,溶液碱性减弱;②
(4)相同温度和压强下,研究
 在不同溶液中的溶解度(用溶解
在不同溶液中的溶解度(用溶解 的物质的量浓度表示)随溶液浓度变化。图1为不同浓度NaCl溶液中
的物质的量浓度表示)随溶液浓度变化。图1为不同浓度NaCl溶液中 的溶解度以及其他含氯微粒(HClO、
的溶解度以及其他含氯微粒(HClO、 )浓度的变化曲线。在饱和食盐水中加入不同浓度盐酸溶液时
)浓度的变化曲线。在饱和食盐水中加入不同浓度盐酸溶液时 溶解度的变化曲线如图2所示。
溶解度的变化曲线如图2所示。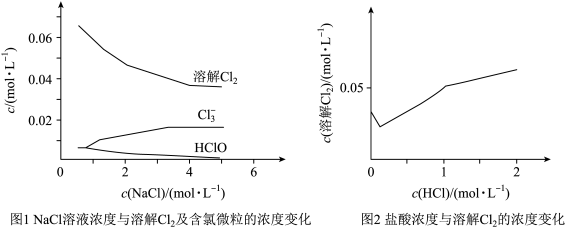
 的溶解度先减小后增大。请结合图1信息,分析出现增大的可能原因为
的溶解度先减小后增大。请结合图1信息,分析出现增大的可能原因为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】纳米 在生物医学等方面具有广泛的用途。利用废旧镀锌铁皮(含
在生物医学等方面具有广泛的用途。利用废旧镀锌铁皮(含 、
、 、
、 、
、 )制备纳米
)制备纳米 及副产物
及副产物 的流程如下:
的流程如下:
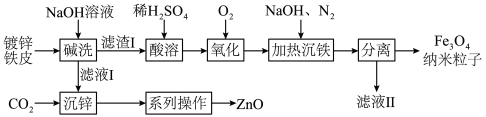
查阅资料: 、
、 、
、 的化学性质与铝及其化合物类似。
的化学性质与铝及其化合物类似。
回答下列问题:
(1)“碱洗”时, 溶液的作用是
溶液的作用是___________________ 。
(2)“沉锌”时,选用 而不用盐酸的依据是
而不用盐酸的依据是___________________ ,该反应的离子方程式为__________________________ 。
(3)“系列操作”包括过滤、____________ 。
(4)“氧化”后的溶液中所含金属阳离子有________________________ (填离子符号)。
(5)文献表明,若“氧化”时,溶液 过低,
过低, 容易转化为
容易转化为 ,该反应的化学方程式为
,该反应的化学方程式为_______________________ 。
(6)检验“分离”得到的 是否洗净的操作为
是否洗净的操作为______________________ 。
(7)某化学兴趣小组用 废旧镀锌铁皮(
废旧镀锌铁皮( 元素的质量分数为
元素的质量分数为 )制备纳米
)制备纳米 ,最终得到
,最终得到 产品,则产率为
产品,则产率为______ (保留三位有效数字)。
 在生物医学等方面具有广泛的用途。利用废旧镀锌铁皮(含
在生物医学等方面具有广泛的用途。利用废旧镀锌铁皮(含 、
、 、
、 、
、 )制备纳米
)制备纳米 及副产物
及副产物 的流程如下:
的流程如下:
查阅资料:
 、
、 、
、 的化学性质与铝及其化合物类似。
的化学性质与铝及其化合物类似。回答下列问题:
(1)“碱洗”时,
 溶液的作用是
溶液的作用是(2)“沉锌”时,选用
 而不用盐酸的依据是
而不用盐酸的依据是(3)“系列操作”包括过滤、
(4)“氧化”后的溶液中所含金属阳离子有
(5)文献表明,若“氧化”时,溶液
 过低,
过低, 容易转化为
容易转化为 ,该反应的化学方程式为
,该反应的化学方程式为(6)检验“分离”得到的
 是否洗净的操作为
是否洗净的操作为(7)某化学兴趣小组用
 废旧镀锌铁皮(
废旧镀锌铁皮( 元素的质量分数为
元素的质量分数为 )制备纳米
)制备纳米 ,最终得到
,最终得到 产品,则产率为
产品,则产率为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】某化工厂的废液中,含有大量 溶液,但当中掺杂有一些
溶液,但当中掺杂有一些 、
、 ,为实现变废为宝,选择适当的试剂设计实验除去杂质,从而得到纯净的
,为实现变废为宝,选择适当的试剂设计实验除去杂质,从而得到纯净的 晶体,相应的实验流程如图所示。
晶体,相应的实验流程如图所示。
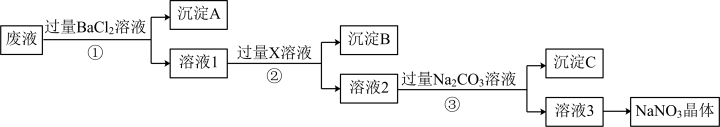
请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X_______ 。
(2)上述实验流程中加入过量 溶液后发生反应的离子方程式:
溶液后发生反应的离子方程式: _______ 、_______ 。
(3)按此实验方案得到的溶液3中肯定含有_______ 杂质。(填化学式,下同)为了解决这个问题,可以向溶液3中加入适量的_______ 。
(4)在①步操作中如何证明加的 溶液已过量?
溶液已过量? _______ 。
 溶液,但当中掺杂有一些
溶液,但当中掺杂有一些 、
、 ,为实现变废为宝,选择适当的试剂设计实验除去杂质,从而得到纯净的
,为实现变废为宝,选择适当的试剂设计实验除去杂质,从而得到纯净的 晶体,相应的实验流程如图所示。
晶体,相应的实验流程如图所示。
请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X
(2)上述实验流程中加入过量
 溶液后发生反应的离子方程式:
溶液后发生反应的离子方程式: (3)按此实验方案得到的溶液3中肯定含有
(4)在①步操作中如何证明加的
 溶液已过量?
溶液已过量?
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作分解为如下几步:
A.用蒸馏水洗干净滴定管
B.用待测定的溶液润洗酸式滴定管
C.用酸式滴定管取稀盐酸20. 00mL,注入锥形瓶中,加入酚酞
D.另取锥形瓶,再重复操作一次
E.检查滴定管是否漏水
F.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2~3 cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
(1)正确操作的顺序是(用序号字母填写)______ 。
(2)判断滴定终点的现是______ 。
(3)下列操作使得待测液浓度偏低的是______
A.碱式滴定管在装液前未用标准NaOH溶液润洗2~3次
B.滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C.达到滴定终点时,仰视溶液凹液面最低点读数
D.滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(4)常温下,已知0.1 mol·L-1一元酸HA溶液中c(OH-) / c(H+)=1×10-8。
①常温下,0.1 mol·L-1 HA溶液的pH=______ ;写出该酸(HA)与NaOH溶液反应的离子方程式:______ ;
②pH=3的HA与pH=11的NaOH溶液等体积混合后,溶液中4种离子物质的量浓度大小关系是:______ ;
A.用蒸馏水洗干净滴定管
B.用待测定的溶液润洗酸式滴定管
C.用酸式滴定管取稀盐酸20. 00mL,注入锥形瓶中,加入酚酞
D.另取锥形瓶,再重复操作一次
E.检查滴定管是否漏水
F.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2~3 cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
(1)正确操作的顺序是(用序号字母填写)
(2)判断滴定终点的现是
(3)下列操作使得待测液浓度偏低的是
A.碱式滴定管在装液前未用标准NaOH溶液润洗2~3次
B.滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C.达到滴定终点时,仰视溶液凹液面最低点读数
D.滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(4)常温下,已知0.1 mol·L-1一元酸HA溶液中c(OH-) / c(H+)=1×10-8。
①常温下,0.1 mol·L-1 HA溶液的pH=
②pH=3的HA与pH=11的NaOH溶液等体积混合后,溶液中4种离子物质的量浓度大小关系是:
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】化学上的缓冲溶液就是外加少量酸、碱后而pH值基本不变的溶液。
I.CH3COOH和CH3COONa的缓冲溶液
1.现有25℃时浓度均为0.10mol/L的CH3COOH和CH3COONa的缓冲溶液,pH=4.76。写出该缓冲溶液中存在的电离平衡方程式___________ 、___________ 。
2.向1.0L上述0.10mol/L的CH3COOH和CH3COONa的缓冲溶液中滴加几滴NaOH稀溶液(忽略溶液体积的变化),发生反应的离子方程式为___________ ,反应后溶液中c(H+)=___________ mol/L。
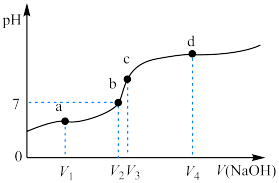
3.向CH3COOH溶液中逐滴加入NaOH溶液,溶液pH与加入NaOH溶液的关系如图所示,a点为反应一半点,a点离子浓度关系由大到小为___________ ;c点恰好完全反应,该处溶液呈碱性的原因为___________ 。
4.CO2的电子式为___________ ,其分子极性为___________ ;电负性C___________ Si(填“>”“=”或者“<”)。
5.人体血液存在H2CO3(CO2)和NaHCO3的缓冲体系,下列说法不正确的是___________ 。
a.代谢产生的H+被 结合形成H2CO3
结合形成H2CO3
b.代谢产生的碱被H+中和,H+又由H2CO3电离
c.血液中的缓冲体系可抵抗大量酸、碱的影响
d.能有效除掉人体正常代谢产生的酸、碱,保持pH的稳定
I.CH3COOH和CH3COONa的缓冲溶液
1.现有25℃时浓度均为0.10mol/L的CH3COOH和CH3COONa的缓冲溶液,pH=4.76。写出该缓冲溶液中存在的电离平衡方程式
2.向1.0L上述0.10mol/L的CH3COOH和CH3COONa的缓冲溶液中滴加几滴NaOH稀溶液(忽略溶液体积的变化),发生反应的离子方程式为
3.向CH3COOH溶液中逐滴加入NaOH溶液,溶液pH与加入NaOH溶液的关系如图所示,a点为反应一半点,a点离子浓度关系由大到小为
4.CO2的电子式为
5.人体血液存在H2CO3(CO2)和NaHCO3的缓冲体系,下列说法不正确的是
a.代谢产生的H+被
 结合形成H2CO3
结合形成H2CO3b.代谢产生的碱被H+中和,H+又由H2CO3电离
c.血液中的缓冲体系可抵抗大量酸、碱的影响
d.能有效除掉人体正常代谢产生的酸、碱,保持pH的稳定
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】Na2S俗名叫“臭碱”,是重要的化工产品。
某学习小组设计如下实验:
Ⅰ.探究Na2S的还原性
甲取少量硫化钠溶液于试管,滴加2滴酚酞溶液,再滴加溴水溶液,观察到溶液颜色变浅。
(1)酚酞的作用是____________ ;写出该实验的离子方程式____________________________
(2)乙认为甲方案不严密。他设计方案:取少量硫化钠溶液于试管,滴加适量苯,再加入溴水。加入“苯”的目的是_________________________________________________________
Ⅱ.探究氧化还原反应和沉淀反应的竞争
丙设计两组实验:
实验Ⅰ:①在10mL2 mol·L-1FeCl3溶液中滴加2mL 1 mol·L-1Na2S溶液,观察到有浅黄色沉淀生成,溶液黄色变浅。②在10mL 2 mol·L-1Na2S溶液中滴加2ml 1 mol·L-1FeCl3溶液。观察到先产生浅黄色固体,随后生成黑色固体,溶液黄色变无色。
实验2:在2 mol·L-1Na2S溶液中滴加少量AgNO3溶液,立即产生大量黑色沉淀,没有浅黄色沉淀。
(3)实验I①中产生的浅黄色固体是___________________ (填化学式)。写出实验I②中产生黑色沉淀的离子方程式_________________________________________
(4)已知:氧化性有Ag+>Fe3+。实验2中,发生复分解反应,未发生氧化还原反应,其主要原因可能是_____________________________________________________________________
某学习小组设计如下实验:
Ⅰ.探究Na2S的还原性
甲取少量硫化钠溶液于试管,滴加2滴酚酞溶液,再滴加溴水溶液,观察到溶液颜色变浅。
(1)酚酞的作用是
(2)乙认为甲方案不严密。他设计方案:取少量硫化钠溶液于试管,滴加适量苯,再加入溴水。加入“苯”的目的是
Ⅱ.探究氧化还原反应和沉淀反应的竞争
丙设计两组实验:
实验Ⅰ:①在10mL2 mol·L-1FeCl3溶液中滴加2mL 1 mol·L-1Na2S溶液,观察到有浅黄色沉淀生成,溶液黄色变浅。②在10mL 2 mol·L-1Na2S溶液中滴加2ml 1 mol·L-1FeCl3溶液。观察到先产生浅黄色固体,随后生成黑色固体,溶液黄色变无色。
实验2:在2 mol·L-1Na2S溶液中滴加少量AgNO3溶液,立即产生大量黑色沉淀,没有浅黄色沉淀。
(3)实验I①中产生的浅黄色固体是
(4)已知:氧化性有Ag+>Fe3+。实验2中,发生复分解反应,未发生氧化还原反应,其主要原因可能是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐1】弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡。
(1)常温下,将0.1mol/L HCl溶液与0.1 mol/L MOH溶液等体积混合,测得混合后溶液的pH=5,则MOH在水中的电离方程式为_______ 。
(2)已知常温时CH3COOH CH3COO– + H+,Ka=2×10–5,则反应CH3COO– + H2O
CH3COO– + H+,Ka=2×10–5,则反应CH3COO– + H2O CH3COOH + OH–的平衡常数Kh=
CH3COOH + OH–的平衡常数Kh=___________ 。
(3)已知H2A在水中发生电离:H2A=H++HA–,HA– H++A2–。
H++A2–。
①Na2A的水解方程式为_______ , 等物质的量浓度的两种溶液:NaHA溶液的pH_______ (填“>”、“=”或“<”)Na2A溶液的pH。
② 已知0.1 mol·L-1 NaHA溶液的pH=2,该溶液中各种离子浓度由大到小的顺序是_______ 。
③某温度下,若向0.1 mol·L–1的NaHA溶液中逐滴滴加0.1 mol·L–1 NaOH溶液至溶液呈中性 。对该混合溶液,下列说法一定正确的是_______ (填序号)。
A.c(H+)·c(OH–)=1×10–14 B.c(Na+)=c(HA–)+2c(A2–)
C.溶液中水的电离程度逐渐减小 D.c(Na+)=c(HA–)+c(A2–)
(4)根据甲醇在酸性(H2SO4)电解质溶液中与氧气生成二氧化碳和水的反应,设计一种燃料电池。该燃料电池工作时,正极的电极反应式为___________ 。
(1)常温下,将0.1mol/L HCl溶液与0.1 mol/L MOH溶液等体积混合,测得混合后溶液的pH=5,则MOH在水中的电离方程式为
(2)已知常温时CH3COOH
 CH3COO– + H+,Ka=2×10–5,则反应CH3COO– + H2O
CH3COO– + H+,Ka=2×10–5,则反应CH3COO– + H2O CH3COOH + OH–的平衡常数Kh=
CH3COOH + OH–的平衡常数Kh=(3)已知H2A在水中发生电离:H2A=H++HA–,HA–
 H++A2–。
H++A2–。①Na2A的水解方程式为
② 已知0.1 mol·L-1 NaHA溶液的pH=2,该溶液中各种离子浓度由大到小的顺序是
③某温度下,若向0.1 mol·L–1的NaHA溶液中逐滴滴加0.1 mol·L–1 NaOH溶液至溶液
A.c(H+)·c(OH–)=1×10–14 B.c(Na+)=c(HA–)+2c(A2–)
C.溶液中水的电离程度逐渐减小 D.c(Na+)=c(HA–)+c(A2–)
(4)根据甲醇在酸性(H2SO4)电解质溶液中与氧气生成二氧化碳和水的反应,设计一种燃料电池。该燃料电池工作时,正极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐2】回答下列问题:
(1)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图I中数据,试填写下列空白:

①该反应的化学方程式为______ 。
②反应开始至2min,气体Y的平均反应速率为_____ 。
(2)如图II是一个电化学过程的示意图,其中B电极的电极材料为碳。请填空:
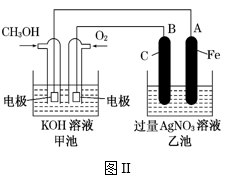
①甲池中,通入甲醇电极反应式为_____ 。
②乙池中,总反应离子方程式为_____ 。
③在此过程中若完全反应,乙池中A极的质量增加648g,则甲池中理论上消耗O2_____ L(标准状况下)。
(3)①下列不能说明HNO2是弱电解质的是_____ (填字母)。
a.常温下0.1 mol∙L−1NaNO2溶液的pH>7
b.用一定浓度HNO2溶液做导电实验,灯泡很暗
c.0.1 mol∙L−1HNO2溶液与等体积0.1 mol∙L−1NaOH溶液恰好反应
d.常温下,0.1 mol∙L−1HNO2溶液的pH=2.3
②体积相同、c(H+)相同的三种酸溶液a.HCOOH;b.HCN;c.HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)_____ 。(已知25℃时,HCOOH的Ka=1.7710−4,HCN的Ka=5.010−10)
③25℃时,0.1 mol∙L−1的某一元酸(HA)溶液中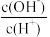 =1×10−8,0.1 mol∙L−1HA溶液的pH=
=1×10−8,0.1 mol∙L−1HA溶液的pH=_____ ,Ka=_____ 。
(1)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图I中数据,试填写下列空白:

①该反应的化学方程式为
②反应开始至2min,气体Y的平均反应速率为
(2)如图II是一个电化学过程的示意图,其中B电极的电极材料为碳。请填空:

①甲池中,通入甲醇电极反应式为
②乙池中,总反应离子方程式为
③在此过程中若完全反应,乙池中A极的质量增加648g,则甲池中理论上消耗O2
(3)①下列不能说明HNO2是弱电解质的是
a.常温下0.1 mol∙L−1NaNO2溶液的pH>7
b.用一定浓度HNO2溶液做导电实验,灯泡很暗
c.0.1 mol∙L−1HNO2溶液与等体积0.1 mol∙L−1NaOH溶液恰好反应
d.常温下,0.1 mol∙L−1HNO2溶液的pH=2.3
②体积相同、c(H+)相同的三种酸溶液a.HCOOH;b.HCN;c.HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)
③25℃时,0.1 mol∙L−1的某一元酸(HA)溶液中
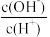 =1×10−8,0.1 mol∙L−1HA溶液的pH=
=1×10−8,0.1 mol∙L−1HA溶液的pH=
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】Ⅰ.25℃时,部分弱酸的电离平衡常数如下表:
(1)H2S的二级电离平衡常数的表达式为_________ 。
(2)相同c(H+)浓度的HCOOH和HClO溶液中:c(HCOOH)______ c(HClO) (填“>”、“<”或“=”)。
Ⅱ.现将pH=3,体积均为V0的盐酸和醋酸溶液分别加水稀释至体积V,pH随lg( )的变化如图所示。
)的变化如图所示。

(3)醋酸的电离平衡常数表达式为Ka=________ ;加水稀释过程中,醋酸的电离平衡向______ (填“正”或“逆”)反应方向移动,Ka______ 填“增大”“减小”或“不变”)。
(4)比较b、c两点溶液的导电能力强弱:b_______ c(填大于、小于、等于)。
(5)已知HA的电离常数Ka1=4.9×10-10,H2B的电离常数Ka1=4.3×10-7,Ka2=5.6×10-12,试写出NaA与少量H2B反应的离子方程式___________ 。
| 弱酸 | HCOOH | H2S | H2CO3 | HClO |
| 电离平衡常数(25℃) | Ka=1.77×10-4 | Ka1=1.3×10-7 Ka2=7.1×10-15 | Ka1=4.4×10-7 Ka2=4.7×10-11 | Ka=3.0×10-8 |
(2)相同c(H+)浓度的HCOOH和HClO溶液中:c(HCOOH)
Ⅱ.现将pH=3,体积均为V0的盐酸和醋酸溶液分别加水稀释至体积V,pH随lg(
 )的变化如图所示。
)的变化如图所示。
(3)醋酸的电离平衡常数表达式为Ka=
(4)比较b、c两点溶液的导电能力强弱:b
(5)已知HA的电离常数Ka1=4.9×10-10,H2B的电离常数Ka1=4.3×10-7,Ka2=5.6×10-12,试写出NaA与少量H2B反应的离子方程式
您最近一年使用:0次



