世界卫生组织公布镍金属和镍合金是致癌物。请结合所学知识完成问题:
(1)镍原子在周期表中的位置_______ ,其电子排布式为_______ 。
(2) 溶液与丁二酮肟的反应如下图,该反应可以用来鉴别
溶液与丁二酮肟的反应如下图,该反应可以用来鉴别 。
。
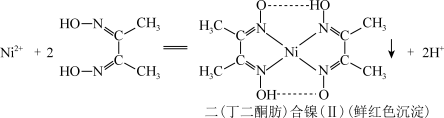
①丁二酮肟中同周期元素的第一电离能由大到小的顺序为_______ 。
②二(丁二酮肟)合镍(Ⅱ)中存在的化学键类型有_______ (填标号)。
A.极性键 B.非极性键 C.氢键 D.配位键
(3)可以用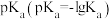 来衡量酸的强弱。下表是部分酸的
来衡量酸的强弱。下表是部分酸的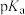 数据:
数据:
从表中数据可知,酸性: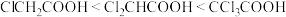 ,请从物质结构角度解释原因
,请从物质结构角度解释原因_______ 。
(4)某种镁、镍和碳三种元素形成的晶体具有超导性。该晶体可看作是镁原子位于顶点,镍原子位于面心的面心立方堆积(晶胞结构如图,未标出碳原子位置),碳原子只填充在由镍构成的八面体空隙。
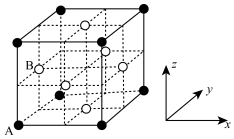
①填充在八面体空隙的碳原子位于该晶胞的_______ 位置。
②原子的分数坐标:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,若A点原子分数坐标 ,B点原子分数坐标
,B点原子分数坐标 ,则碳原子的分数坐标为
,则碳原子的分数坐标为_______ 。
③已知晶胞中相邻且最近的镁、碳原子间核间距为 ,
, 为阿伏加德罗常数的值,其密度为
为阿伏加德罗常数的值,其密度为_______  (列出计算式即可)。
(列出计算式即可)。
(1)镍原子在周期表中的位置
(2)
 溶液与丁二酮肟的反应如下图,该反应可以用来鉴别
溶液与丁二酮肟的反应如下图,该反应可以用来鉴别 。
。
①丁二酮肟中同周期元素的第一电离能由大到小的顺序为
②二(丁二酮肟)合镍(Ⅱ)中存在的化学键类型有
A.极性键 B.非极性键 C.氢键 D.配位键
(3)可以用
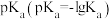 来衡量酸的强弱。下表是部分酸的
来衡量酸的强弱。下表是部分酸的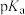 数据:
数据:| 物质 |  |  |  |
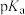 (室温) (室温) | 2.86 | 1.29 | 0.65 |
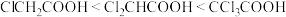 ,请从物质结构角度解释原因
,请从物质结构角度解释原因(4)某种镁、镍和碳三种元素形成的晶体具有超导性。该晶体可看作是镁原子位于顶点,镍原子位于面心的面心立方堆积(晶胞结构如图,未标出碳原子位置),碳原子只填充在由镍构成的八面体空隙。

①填充在八面体空隙的碳原子位于该晶胞的
②原子的分数坐标:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,若A点原子分数坐标
 ,B点原子分数坐标
,B点原子分数坐标 ,则碳原子的分数坐标为
,则碳原子的分数坐标为③已知晶胞中相邻且最近的镁、碳原子间核间距为
 ,
, 为阿伏加德罗常数的值,其密度为
为阿伏加德罗常数的值,其密度为 (列出计算式即可)。
(列出计算式即可)。
更新时间:2023-12-27 10:21:13
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、V、M、W为五种短周期元素,其中X是短周期元素中金属性最强的元素;Y与X同周期,是同周期简单离子中半径最小的;Z原子基态时2p原子轨道上有3个未成对的电子;V原子的核外电子排布式为1s22s22p63s2;M处于第三周期,其单质为淡黄色固体;W的一种同位素原子无中子。回答下列问题:
(1)M与W形成的分子是___ (填“极性分子”或“非极性分子”);与该分子互为等电子体的一种阴离子为(写化学式)___ 。
(2)元素X、Y、V第一电离能由小到大的顺序是___ (用元素符号表示)。
(3)ZW3气体易溶于水的原因是___ 。(写两点)
(4)M8是___ 晶体,该晶体中微粒间的作用力为___ ;
(5)X的最高价氧化物的水化物和Y的最高价氧化物相互反应的离子方程式___ 。
(1)M与W形成的分子是
(2)元素X、Y、V第一电离能由小到大的顺序是
(3)ZW3气体易溶于水的原因是
(4)M8是
(5)X的最高价氧化物的水化物和Y的最高价氧化物相互反应的离子方程式
您最近一年使用:0次
【推荐2】Y、Z、W、R、M五种元素,位于元素周期表的前四周期,它们的核电荷数依次增大,有如下信息:
请回答下列问题(Y、Z、W、R、M用所对应的元素符号表示):
(1)Z、W元素相比,第一电离能较大的是____ ,M2+的核外电子排布式为_______ 。
(2)M2Z的熔点比M2W的______ (填“高”或“低”),请解释原因:_____________ 。
(3)WZ2的VSEPR模型名称为______ ;WZ3气态为单分子,该分子中W原子的杂化轨道类型为____ ;WZ3的三聚体环状结构如图(a)所示,该结构的分子中含有____ 个σ键;写出一种与WZ3互为等电子体的分子的化学式_____ 。
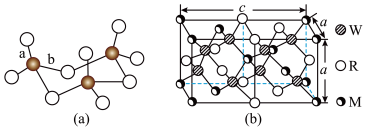
(4)MRW2的晶胞如图(b)所示,晶胞参数a=0.524 nm、c=1.032 nm;MRW2的晶胞中,晶体密度ρ=____ g/cm3(只要求列算式,不必计算出数值,阿伏加 德罗常数为NA=6.02×1023 mol-1)。
| 元素 | 相关信息 |
| Y | 原子核外有6个不同运动状态的电子 |
| Z | 非金属元素,基态原子的s轨道的电子总数与p轨道的电子总数相同 |
| W | 主族元素,与Z原子的价电子数相同 |
| R | 价层电子排布式为3d64s2 |
| M | 位于第ⅠB族,其被称作“电器工业的主角” |
请回答下列问题(Y、Z、W、R、M用所对应的元素符号表示):
(1)Z、W元素相比,第一电离能较大的是
(2)M2Z的熔点比M2W的
(3)WZ2的VSEPR模型名称为

(4)MRW2的晶胞如图(b)所示,晶胞参数a=0.524 nm、c=1.032 nm;MRW2的晶胞中,晶体密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】已知可以由下列反应合成三聚氰胺:CaO+3C CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2 CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:_____ 。
CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和___ (填化学式),由此可以推知CN22-的空间构型为___ 。
(2)尿素分子中C原子采取____ 杂化。尿素分子的结构简式是____ 。
(3)三聚氰胺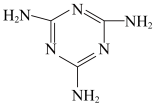 俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸
俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸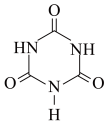 后,三聚氰酸与三聚氰胺分子相互之间通过
后,三聚氰酸与三聚氰胺分子相互之间通过____ 结合,在肾脏内易形成结石。
(4)H2与O2发生反应的过程用模型图示如下(“—”表示化学键):
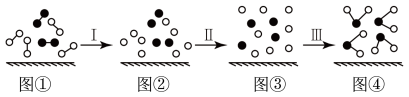
其中过程Ⅰ是___ 过程(填“吸热”、“放热”或“没有能量变化”)。图④中产生了由极性键构成的_______ 分子(填“极性”或“非极性”)。
(5)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为_____ 。
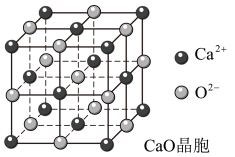
已知CaO晶体的密度为ρ,求晶胞中距离最近的两个钙离子之间的距离_____ (列出计算式)CaO晶体和NaCl晶体的晶格能分别为:CaO3401kJ·mol-1、NaCl786kJ·mol-1。导致两者晶格能差异的主要原因是________ 。
 CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2 CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:
CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和
(2)尿素分子中C原子采取
(3)三聚氰胺
 俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸
俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸 后,三聚氰酸与三聚氰胺分子相互之间通过
后,三聚氰酸与三聚氰胺分子相互之间通过(4)H2与O2发生反应的过程用模型图示如下(“—”表示化学键):

其中过程Ⅰ是
(5)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为

已知CaO晶体的密度为ρ,求晶胞中距离最近的两个钙离子之间的距离
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】中国古代陶瓷烧制工艺的珍品“唐三彩”中的蓝色,其釉料的着色剂是一种含钴矿物。钴在制取颜料和制备合金方面有着重要的应用,回答下列问题。
(1)基态Co2+的核外电子排布式为__________ ,基态Co原子中空间运动状态不同的电子数为___ 种。
(2)配合物[Co(NH3)5Br](NO3)2中存在的化学键类型有__________ ,配体NH3中配位原子的杂化轨道类型为__________ ,NO3-的空间构型是__________ ,第一电离能N__________ (填“大于”或“小于”)O。
(3)CoO2具有如图所示的层状结构(小球表示Co,大球表示O)。下列用粗实线画出的结构单元不能描述其化学组成的是__________ (填字时代号)。________ nm(结果保留三位小数,下同)。CoO也属于NaCl型结构,晶胞参数为a'=0.488 nm,则r(Co2+)为________ nm
(1)基态Co2+的核外电子排布式为
(2)配合物[Co(NH3)5Br](NO3)2中存在的化学键类型有
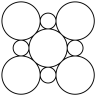
(3)CoO2具有如图所示的层状结构(小球表示Co,大球表示O)。下列用粗实线画出的结构单元不能描述其化学组成的是
A.  B.
B. 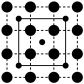 C.
C. 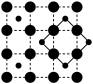 D.
D. 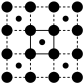
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】长征五号B运载火箭中使用了耐热性佳,导热性好的氮化铝陶瓷。已知:Al4C3+4NH3=4AlN+3CH4。回答下列问题:
(1)碳原子核外电子中未成对电子数是_____ ,氨气的电子式是_____ 。
(2)AlN是由共价键直接形成的晶体,硬度大、熔点高,它是_____ 晶体。上述反应中形成相同电子层结构离子的元素,其简单离子半径由大到小的顺序是_____ 。
(3)比较非金属性N>C正确的是_____
a.HNO3酸性大于H2CO3
b.N最高价为+5,C最高价为+4
c.HNO3氧化性大于H2CO3
d.H3C﹣NH2中C﹣N共用电子对偏向N
(4)AlN遇水会发生水解,反应的化学方程式为:_____ ,AlN在80℃和90℃水中完全水解,测得水解后溶液的pH(80℃)>pH(90℃),试从平衡移动角度解释其原因:_____ 。 (不考虑水的离子积变化和Al(OH)3电离)。
(5)向Al(OH)3悬浊液中加入NaOH溶液至沉淀恰好完全溶解,写出反应的离子方程式:_____ 。溶液中c(Na+)_____ c(AlO ) (填“>”或“<”),欲使c(Na+):c(AlO
) (填“>”或“<”),欲使c(Na+):c(AlO )=1:1,可加入
)=1:1,可加入_____ 。
(1)碳原子核外电子中未成对电子数是
(2)AlN是由共价键直接形成的晶体,硬度大、熔点高,它是
(3)比较非金属性N>C正确的是
a.HNO3酸性大于H2CO3
b.N最高价为+5,C最高价为+4
c.HNO3氧化性大于H2CO3
d.H3C﹣NH2中C﹣N共用电子对偏向N
(4)AlN遇水会发生水解,反应的化学方程式为:
(5)向Al(OH)3悬浊液中加入NaOH溶液至沉淀恰好完全溶解,写出反应的离子方程式:
 ) (填“>”或“<”),欲使c(Na+):c(AlO
) (填“>”或“<”),欲使c(Na+):c(AlO )=1:1,可加入
)=1:1,可加入
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
⑴A、B、C原子的第一电离能由小到大的顺序是__________ (用元素符号表示);
Q元素基态原子电子排布式为_____________________________ 。
⑵写出BC2+的电子式___________ ,1mol BC2+中含有的π键数目为____________ 。
⑶化合物甲由B、D两元素组成,已知甲是一种重要的结构材料,硬度大,耐磨损,晶胞如图1所示甲的晶体中B、D两种元素原子的杂化方式均为__________ 。
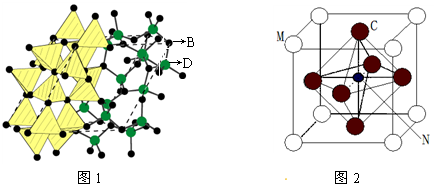
⑷法国科学家阿尔贝·费尔和德国科学家彼得·格林贝格尔因在巨磁电阻效应(CMR效应)研究方面的成就而获得诺贝尔物理学奖。如图2的化合物具有CMR效应,则该化合物的化学式为________________ 。
| A | B | C | |||||||||||||||
| D | E | ||||||||||||||||
| N | M | Q | |||||||||||||||
⑴A、B、C原子的第一电离能由小到大的顺序是
Q元素基态原子电子排布式为
⑵写出BC2+的电子式
⑶化合物甲由B、D两元素组成,已知甲是一种重要的结构材料,硬度大,耐磨损,晶胞如图1所示甲的晶体中B、D两种元素原子的杂化方式均为

⑷法国科学家阿尔贝·费尔和德国科学家彼得·格林贝格尔因在巨磁电阻效应(CMR效应)研究方面的成就而获得诺贝尔物理学奖。如图2的化合物具有CMR效应,则该化合物的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】磷的单质及其化合物用途非常广泛,回答下列问题:
(1)基态磷原子价电子排布式为_______ ,第一电离能:磷_______ (填“>”或“<”)硫。
(2)磷的常见单质如图所示。
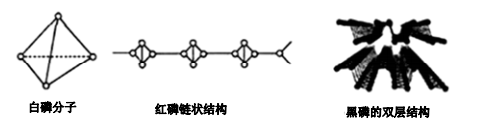
①白磷分子中磷原子的杂化轨道类型为_______ ,每个白磷分子中有_______ 对孤对电子。
②黑磷是一种有金属光泽的晶体,能够导电的原因是_______ 。
(3)砷为磷的下一周期同族元素,酸性:H3PO4_______ (填“>”或“<”)H3AsO4。
(4)一种发光二极管的半导体材料为GaAsxP1-x,该化合物中Ga、As及P的电负性从大到小的顺序为_______ 。
(5)磷化硼(BP)是一种半导体材料,熔点为1000℃。其晶胞结构如图所示。
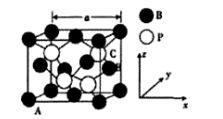
①磷化硼属于_______ (填“分子”“原子”“离子”或“金属”)晶体。
②原子坐标参数,可表示晶胞内部各原子的相对位置,上图中原子坐标参数A为(0,0,0),B为(1, ,
, )。则C原子的坐标参数为
)。则C原子的坐标参数为_______ 。
③晶胞参数是用来描述晶胞的大小和形状,已知BP晶胞参数α≈478 pm,则其密度为_______ (设NA为阿伏加德罗常数的数值,列出计算式即可)g·cm-3。
(1)基态磷原子价电子排布式为
(2)磷的常见单质如图所示。

①白磷分子中磷原子的杂化轨道类型为
②黑磷是一种有金属光泽的晶体,能够导电的原因是
(3)砷为磷的下一周期同族元素,酸性:H3PO4
(4)一种发光二极管的半导体材料为GaAsxP1-x,该化合物中Ga、As及P的电负性从大到小的顺序为
(5)磷化硼(BP)是一种半导体材料,熔点为1000℃。其晶胞结构如图所示。

①磷化硼属于
②原子坐标参数,可表示晶胞内部各原子的相对位置,上图中原子坐标参数A为(0,0,0),B为(1,
 ,
, )。则C原子的坐标参数为
)。则C原子的坐标参数为③晶胞参数是用来描述晶胞的大小和形状,已知BP晶胞参数α≈478 pm,则其密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
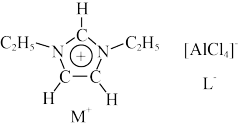
【推荐2】离子液体是一种由离子构成的很有研究价值的溶剂。某离子液体由如图所示正离子 和负离子
和负离子 构成,已知
构成,已知 中的五元环为平面形结构,该离子有较强的稳定性。
中的五元环为平面形结构,该离子有较强的稳定性。
(1)基态N原子中共有___________ 种空间状态不同的电子,其中占据最高能级的电子云轮廓图为___________ 形。原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为___________ 。
(2) 中的各种元素的电负性由小到大的顺序为
中的各种元素的电负性由小到大的顺序为___________ , 中N原子的杂化方式为
中N原子的杂化方式为___________ 。
(3)负离子 的空间构型为
的空间构型为___________ 形。
(4)分子中的大 键可用符号
键可用符号 表示,其中m代表形成大
表示,其中m代表形成大 键的原子数,n代表形成大
键的原子数,n代表形成大 键的电子数。如苯(
键的电子数。如苯(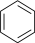 )中的大
)中的大 键可表示为
键可表示为 ,则
,则 中的大
中的大 键可表示为
键可表示为___________ 。
(5)碳原子与氮原子还可形成六元环状化合物吡啶( ),其分子中也含有与苯类似的
),其分子中也含有与苯类似的 大
大 键,则吡啶中N原子的孤电子对占据的轨道为___________。
键,则吡啶中N原子的孤电子对占据的轨道为___________。
(6)吡啶在水中的溶解度远大于苯,主要原因是①___________ ,②___________ 。
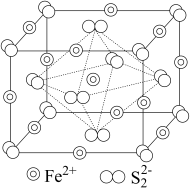
(7)黄铁矿是工业生产硫酸的原料,其晶胞结构如图所示,晶胞参数为anm,该晶体的电子式为___________ , 的配位数为
的配位数为___________ ,晶体的密度为___________  。
。
 和负离子
和负离子 构成,已知
构成,已知 中的五元环为平面形结构,该离子有较强的稳定性。
中的五元环为平面形结构,该离子有较强的稳定性。
(1)基态N原子中共有
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的氮原子,其价电子自旋磁量子数的代数和为(2)
 中的各种元素的电负性由小到大的顺序为
中的各种元素的电负性由小到大的顺序为 中N原子的杂化方式为
中N原子的杂化方式为(3)负离子
 的空间构型为
的空间构型为(4)分子中的大
 键可用符号
键可用符号 表示,其中m代表形成大
表示,其中m代表形成大 键的原子数,n代表形成大
键的原子数,n代表形成大 键的电子数。如苯(
键的电子数。如苯( )中的大
)中的大 键可表示为
键可表示为 ,则
,则 中的大
中的大 键可表示为
键可表示为(5)碳原子与氮原子还可形成六元环状化合物吡啶(
 ),其分子中也含有与苯类似的
),其分子中也含有与苯类似的 大
大 键,则吡啶中N原子的孤电子对占据的轨道为___________。
键,则吡啶中N原子的孤电子对占据的轨道为___________。| A.2s轨道 | B.2p轨道 | C.sp杂化轨道 | D. 杂化轨道 杂化轨道 |
(7)黄铁矿是工业生产硫酸的原料,其晶胞结构如图所示,晶胞参数为anm,该晶体的电子式为
 的配位数为
的配位数为 。
。
您最近一年使用:0次
【推荐3】镍铜合金是由60%镍、33%铜、7%铁三种金属组成的合金材料。镍铜合金有较好的室温力学性能和高温强度,耐蚀性强,耐磨性好,可作为航空发动机的结构材料。回答下列问题:
(1)基态Cu2+的价电子排布式为___________ 。
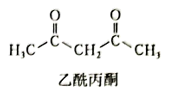
(2)乙酰丙酮(结构如下图)中碳原子的杂化类型为___________ ,乙酰丙酮中σ键与π键数目之比为___________ 。乙酰丙酮中三种元素C、H、O的电负性大小关系:___________ 。
(3)Cu与Fe的第二电离能分别为I2(Cu)=1958 kJ·mol-1 ,I2(Fe)=1561 kJ·mol-1,I2 (Cu)大于I2 (Fe)的主要原因是___________ 。
(4)已知Cu2O的立方晶胞结构如下图所示。
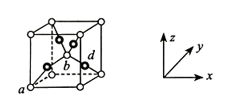
①已知a、b的坐标参数依次为(0,0,0)、( ,
, ,
, ),则d的坐标参数为
),则d的坐标参数为___________ 。
②晶胞边长为c pm,该晶体的密度为___________ g·cm-3.(列出计算式,设NA为阿伏加德罗常数的数值)
(1)基态Cu2+的价电子排布式为
(2)乙酰丙酮(结构如下图)中碳原子的杂化类型为

(3)Cu与Fe的第二电离能分别为I2(Cu)=1958 kJ·mol-1 ,I2(Fe)=1561 kJ·mol-1,I2 (Cu)大于I2 (Fe)的主要原因是
(4)已知Cu2O的立方晶胞结构如下图所示。

①已知a、b的坐标参数依次为(0,0,0)、(
 ,
, ,
, ),则d的坐标参数为
),则d的坐标参数为②晶胞边长为c pm,该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】盐酸阿比多尔是一种盐酸盐,其主要作用是通过抑制流感病毒脂膜与宿主细胞的融合而阻断病毒的复制,结构如图。回答下列问题:
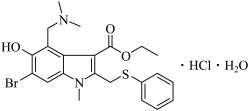
(1)盐酸阿比多尔中所含N、O、S三种元素第一电离能由大到小的顺序为___ 。O原子核外有___ 种不同运动状态的电子,基态S原子的价电子排布图不是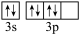 ,是因为该排布方式违背了
,是因为该排布方式违背了___ 。
(2)该结构中N原子的杂化方式是___ 。已知在氨分子中,H—N—H键角为107.3°,但是在[Zn(NH3)6]2+离子中H—N—H键角变为109.5°,分析原因为___ 。
(3)盐酸阿比多尔中不含有的化学键类型为___ (填选项字母)。
A.离子键 B.配位键 C.金属键 D.σ键 E.π键 F.极性键 G.非极性键
(4)以氮化镓(GaN)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点。GaN晶胞如图1所示,图2为晶胞沿y轴的投影1∶1平面图。
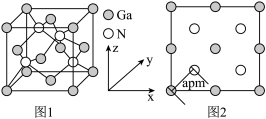
①氮化硼与氮化镓的结构类似,氮化硼熔点3000℃,氮化镓熔点1700℃,分析它们熔点不同的原因____ 。
②晶胞中与一个Ga原子距离最近且相等的N原子有____ 个。
③设阿伏加 德罗常数的值为NA,则该晶胞的密度是___ g·cm−3(列出计算表达式)。

(1)盐酸阿比多尔中所含N、O、S三种元素第一电离能由大到小的顺序为
 ,是因为该排布方式违背了
,是因为该排布方式违背了(2)该结构中N原子的杂化方式是
(3)盐酸阿比多尔中不含有的化学键类型为
A.离子键 B.配位键 C.金属键 D.σ键 E.π键 F.极性键 G.非极性键
(4)以氮化镓(GaN)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点。GaN晶胞如图1所示,图2为晶胞沿y轴的投影1∶1平面图。

①氮化硼与氮化镓的结构类似,氮化硼熔点3000℃,氮化镓熔点1700℃,分析它们熔点不同的原因
②晶胞中与一个Ga原子距离最近且相等的N原子有
③设阿伏加 德罗常数的值为NA,则该晶胞的密度是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】锂电池正极材料NCA,极大地改善了锂电池的性能(注明:NCA指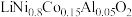 )。请回答下列问题:
)。请回答下列问题:
(1)基态铝原子的价层电子排布式为_______ 。基态钴原子核外有_______ 种能量不同的电子。
(2)钠、镁、铝的第一电离能由大到小排序为_______ (填元素符号)。
(3)氧化锂(Li2O)的熔点为1567℃,氧化镁(MgO)的熔点为2853℃。Li+、Mg2+的离子半径依次为0.076nm、0.072nm。它们的熔点差异除离子半径因素外,还与_______ 有关。
(4)螯合物又称内络合物。 、
、 都能与乙二胺(
都能与乙二胺(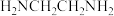 )形成螯合物,其配位原子是
)形成螯合物,其配位原子是_______ (填元素符号)。
(5) 是有机合成的常用还原剂。
是有机合成的常用还原剂。 的空间结构是
的空间结构是_______ 。
(6)NiO晶胞与NaCl晶胞相似,如下图所示:
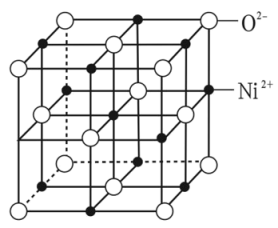
①连接面心上6个 构成
构成_______ (填标号)。
A.正四边形 B.正四面体 C.正八面体 D.立方体
②在NiO晶胞中,每个氧离子周围与它最近且相等距离的氧离子有_______ 个;每个镍离子周围与它最近且相等距离的氧离子有_______ 个。
③已知NiO晶胞边长为a cm,NA为阿伏加德罗常数的值,则NiO晶体的密度为_______  (只列出计算式)。(NiO的摩尔质量用M(g·mol-1)表示)
(只列出计算式)。(NiO的摩尔质量用M(g·mol-1)表示)
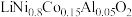 )。请回答下列问题:
)。请回答下列问题:(1)基态铝原子的价层电子排布式为
(2)钠、镁、铝的第一电离能由大到小排序为
(3)氧化锂(Li2O)的熔点为1567℃,氧化镁(MgO)的熔点为2853℃。Li+、Mg2+的离子半径依次为0.076nm、0.072nm。它们的熔点差异除离子半径因素外,还与
(4)螯合物又称内络合物。
 、
、 都能与乙二胺(
都能与乙二胺(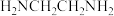 )形成螯合物,其配位原子是
)形成螯合物,其配位原子是(5)
 是有机合成的常用还原剂。
是有机合成的常用还原剂。 的空间结构是
的空间结构是(6)NiO晶胞与NaCl晶胞相似,如下图所示:

①连接面心上6个
 构成
构成A.正四边形 B.正四面体 C.正八面体 D.立方体
②在NiO晶胞中,每个氧离子周围与它最近且相等距离的氧离子有
③已知NiO晶胞边长为a cm,NA为阿伏加德罗常数的值,则NiO晶体的密度为
 (只列出计算式)。(NiO的摩尔质量用M(g·mol-1)表示)
(只列出计算式)。(NiO的摩尔质量用M(g·mol-1)表示)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】云南省曲靖市物华天宝,资源丰富,煤炭、磷、铅、锌、锑等资源储量位居全省前列,会泽县“斑铜”技艺更是闻名全国。2021年12月,中国有色金属工业协会授予曲靖市“绿色晶硅光伏之都”称号。
(1)晶体硅中Si原子的杂化方式是____ ,基态Zn原子核外电子排布式为____ ,基态Cu原子核外有____ 种能量不同的电子。
(2)磷化亚铜(Cu3P)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化亚铜与水反应产生有毒的磷化氢(PH3)气体,PH3分子的空间构型为____ ;Si、P、S的第一电离能(I1)由大到小的顺序为____ 。
(3)一种铜金合金具有储氢功能。其晶体为面心立方最密堆积结构,晶胞中Cu原子处于面心,Au原子处于顶点,则Au原子的配位数为____ 。该储氢材料储氢时,氢分子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与ZnS的结构相似(如图1),该晶体储氢后的化学式为____ 。
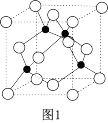
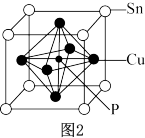
(4)磷青铜晶体的晶胞结构如图2所示,该晶体中P原子位于由铜原子形成的____ 的空隙中。若晶体密度为ag·cm-3,P与最近的Cu原子的核间距为____ nm(用含NA的代数式表示)。
(1)晶体硅中Si原子的杂化方式是
(2)磷化亚铜(Cu3P)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化亚铜与水反应产生有毒的磷化氢(PH3)气体,PH3分子的空间构型为
(3)一种铜金合金具有储氢功能。其晶体为面心立方最密堆积结构,晶胞中Cu原子处于面心,Au原子处于顶点,则Au原子的配位数为

(4)磷青铜晶体的晶胞结构如图2所示,该晶体中P原子位于由铜原子形成的

您最近一年使用:0次



