金属元素及其化合物在生活生产中应用十分广泛。
(1)磷酸亚铁锂(LiFePO4)和锰酸锂(LiMn2O4)均可用作锂离子电池正极材料。在周期表中,与Li化学性质最相似的邻族元素是______ ,基态Fe原子的最外层电子的轨道表示式为______ 。
(2)原子核外电子有两种相反的自旋状态,分别用+ 和﹣
和﹣ 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为______ 。
(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下:
锰元素位于第______ 周期______ 族______ 区;比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,解释原因______ 。
(4)铍由于重量轻、弹性模数高和热稳定性好,已成为引人注目的飞机和导弹结构材料。铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的是______(填选项字母)。
(5)写出氧化铍和NaOH溶液反应生成Na2BeO2,写出该反应的离子方程式______ 。
(6)下列事实能说明氯与氧两元素非金属性相对强弱的有______(填选项字母)。
(7)下列分子或离子:①BCl3、②NH3、③H2O、④CH4、⑤BeCl2中,键角由大到小排列顺序的是______ (用序号表示)。
(1)磷酸亚铁锂(LiFePO4)和锰酸锂(LiMn2O4)均可用作锂离子电池正极材料。在周期表中,与Li化学性质最相似的邻族元素是
(2)原子核外电子有两种相反的自旋状态,分别用+
 和﹣
和﹣ 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下:
| 元素 | Mn | Fe | |
电离能/kJ•mol﹣1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(4)铍由于重量轻、弹性模数高和热稳定性好,已成为引人注目的飞机和导弹结构材料。铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的是______(填选项字母)。
| A.都属于轻金属 | B.失电子的能力都比镁弱 |
| C.原子核外电子云形状都是2种 | D.氯化物的水溶液pH均小于7 |
(6)下列事实能说明氯与氧两元素非金属性相对强弱的有______(填选项字母)。
| A.Cl原子最外层电子数比O多 | B.酸性:HCl>H2O |
| C.ClO2中氯元素为+4价,氧元素为﹣2价 | D.沸点:H2O>HCl |
更新时间:2023-12-21 12:14:51
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】比较微粒半径: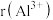
_______ 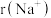 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
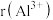
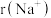 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】科学家们用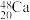 原子轰击某种铬原子,得到了
原子轰击某种铬原子,得到了 原子。
原子。
(1)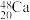 原子的核外电子数是
原子的核外电子数是_______ ,中子数是_______ 。
(2) 的原子结构示意图是
的原子结构示意图是 ,其中的x=
,其中的x=_______ ,y=_______ 。 位于元素周期表的第
位于元素周期表的第_______ 周期,第_______ 族,与它属于同族的一种元素是_______ 。
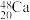 原子轰击某种铬原子,得到了
原子轰击某种铬原子,得到了 原子。
原子。(1)
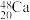 原子的核外电子数是
原子的核外电子数是(2)
 的原子结构示意图是
的原子结构示意图是 ,其中的x=
,其中的x= 位于元素周期表的第
位于元素周期表的第
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下面为元素周期表的一部分,根据元素①~⑧在表中的位置回答下列问题。
(1)①的元素名称为:___________ ,元素④的原子结构示意图为___________ 。
(2)②的最高价氧化物对应水化物酸性比③的最高价氧化物对应水化物酸性弱的原因是___________(填字母)。
(3)②、④组成的能引起温室效应的化合物的电子式为___________ ,其中含有的化学键为___________ 。
(4)②、⑧的最高价氧化物对应水化物的酸性从强到弱的顺序为___________ (用化学式表示)。
(5)③、⑤、⑦三种元素的离子半径从大到小顺序为___________ (用元素符号表示)。
(6)写出元素⑤⑥对应的最高价氧化物的水化物相互之间发生反应的化学方程式___________ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)②的最高价氧化物对应水化物酸性比③的最高价氧化物对应水化物酸性弱的原因是___________(填字母)。
| A.②的单质为固体,而③的单质为气体 |
| B.原子半径②比③大 |
| C.②的非金属性比③弱 |
| D.原子序数③比②大 |
(4)②、⑧的最高价氧化物对应水化物的酸性从强到弱的顺序为
(5)③、⑤、⑦三种元素的离子半径从大到小顺序为
(6)写出元素⑤⑥对应的最高价氧化物的水化物相互之间发生反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】某微粒的结构示意图为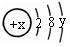 试回答:
试回答:
(1)当x-y=10时,该粒子为_____ (选填“原子”或“阳离子”、“阴离子”);
(2)当y=8时,该粒子可能是(用化学式表示,任填3种)_______ 、_______ 、_______ ;
(3)请写出工业上制取y=7元素对应单质时的离子方程式:_____________ 。
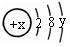 试回答:
试回答:(1)当x-y=10时,该粒子为
(2)当y=8时,该粒子可能是(用化学式表示,任填3种)
(3)请写出工业上制取y=7元素对应单质时的离子方程式:
您最近一年使用:0次
【推荐2】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)B的基态原子中能量最高的电子,其电子云在空间有___ 个方向,原子轨道呈____ 形。
(2)某同学根据上述信息,推断C基态原子的核外电子排布图为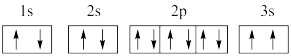 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了_____________________ 。
(3)G位于______ 族______ 区。
(4)检验F元素的实验方法是_________________ 。
(5)BA3中心原子杂化轨道类型为___________ ;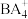 VSEPR模型为
VSEPR模型为___________ ;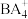 空间结构为
空间结构为_______________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1个 |
| C元素原子的第一至第四电离能分别是: I1=738 kJ·mol-1;I2=1 451 kJ·mol-1;I3=7 733 kJ·mol-1;I4=10 540 kJ·mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)B的基态原子中能量最高的电子,其电子云在空间有
(2)某同学根据上述信息,推断C基态原子的核外电子排布图为
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(3)G位于
(4)检验F元素的实验方法是
(5)BA3中心原子杂化轨道类型为
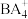 VSEPR模型为
VSEPR模型为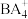 空间结构为
空间结构为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】短周期元素A、B、C、D原子序数依次增大,A的单质是最轻的气体,A、C同主族,只有C是金属元素,B的最外层电子数是次外层电子数的3倍,B、C的最外层电子数之和与D的最外层电子数相等。
(1)C的原子结构示意图为_________________ ;
(2)化合物C2B2中阴、阳离子个数比为___________ ;
(3)化合物CDB是家用消毒剂的主要成分,其物质名称为___________ 。
(4)往CD溶液中滴加硝酸银溶液,可观察到的现象是_________________ ,其反应的离子方程式为________________________________ 。
(1)C的原子结构示意图为
(2)化合物C2B2中阴、阳离子个数比为
(3)化合物CDB是家用消毒剂的主要成分,其物质名称为
(4)往CD溶液中滴加硝酸银溶液,可观察到的现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】比较键角大小:气态SeO3分子_________ SeO 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是_______ 。
 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知有关氮、磷的单键和三键的键能( )如下表:
)如下表:
从能量角度看,氮以N2、而白磷以P4(结构式可表示为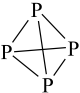 )形式存在的原因是
)形式存在的原因是_______ 。
 )如下表:
)如下表:| N-N | N≡N | P-P | P≡P |
| 193 | 946 | 197 | 489 |
 )形式存在的原因是
)形式存在的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】羰基铁[Fe(CO)5]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为-20℃,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。
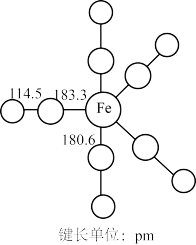
(1)Fe(CO)5晶体类型为___________ 。(填“离子晶体”或“分子晶体”)
(2)下列说法正确的是___________。

(1)Fe(CO)5晶体类型为
(2)下列说法正确的是___________。
| A.中心Fe原子可能采取sp3杂化 | B.配体与Fe原子所形成的配位键的键能相同 |
| C.Fe在周期表中位于Ⅷ族,属于d区元素 | D.制备Fe(CO)5应在隔绝空气的条件下进行 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】硫代硫酸盐是一类具有应用前景的浸金试剂。硫代硫酸根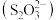 可看作是
可看作是 中的一个
中的一个 原子被
原子被 原子取代的产物。
原子取代的产物。
(1)基态 原子价层电子排布式是
原子价层电子排布式是___________ 。
(2)比较 原子和O原子的第一电离能大小,从原子结构的角度说明理由:
原子和O原子的第一电离能大小,从原子结构的角度说明理由:___________ 。
(3) 的空间结构是
的空间结构是___________ 。
(4)同位素示踪实验可证实 中两个
中两个 原子的化学环境不同,实验过程为
原子的化学环境不同,实验过程为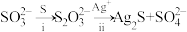 。过程ⅱ中,
。过程ⅱ中, 断裂的只有硫硫键,若过程ⅰ所用试剂是
断裂的只有硫硫键,若过程ⅰ所用试剂是 和
和 ,过程ⅱ含硫产物是
,过程ⅱ含硫产物是___________ 。
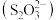 可看作是
可看作是 中的一个
中的一个 原子被
原子被 原子取代的产物。
原子取代的产物。(1)基态
 原子价层电子排布式是
原子价层电子排布式是(2)比较
 原子和O原子的第一电离能大小,从原子结构的角度说明理由:
原子和O原子的第一电离能大小,从原子结构的角度说明理由:(3)
 的空间结构是
的空间结构是(4)同位素示踪实验可证实
 中两个
中两个 原子的化学环境不同,实验过程为
原子的化学环境不同,实验过程为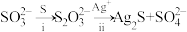 。过程ⅱ中,
。过程ⅱ中, 断裂的只有硫硫键,若过程ⅰ所用试剂是
断裂的只有硫硫键,若过程ⅰ所用试剂是 和
和 ,过程ⅱ含硫产物是
,过程ⅱ含硫产物是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题。
(1) 中的化学键属于
中的化学键属于___________ (填“σ”或“π”)键。
(2) 分子中,中心原子上的σ键电子对数为
分子中,中心原子上的σ键电子对数为___________ ,孤电子对数为___________ ,价层电子对数为___________ ,中心原子的杂化方式为___________ ,VSEPR模型为___________ ,分子的空间结构为___________ 。
(3)下列分子中若有手性分子,请用“*”标出其手性碳原子;若无手性分子,此小题不必作答。
(1)
 中的化学键属于
中的化学键属于(2)
 分子中,中心原子上的σ键电子对数为
分子中,中心原子上的σ键电子对数为(3)下列分子中若有手性分子,请用“*”标出其手性碳原子;若无手性分子,此小题不必作答。

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】在HF、H2O、NH3、CH4、N2、CO2、HI分子中:
(1)以非极性键结合的非极性分子是________________________________ 。
(2)以极性键相结合,具有正四面体结构的非极性分子是______________ 。
(3)以极性键相结合,具有三角锥结构的极性分子是__________________ 。
(4)以极性键相结合,具有V结构的极性分子是______________________ 。
(5)以极性键相结合,而且分子极性最大的是________________ 。
(1)以非极性键结合的非极性分子是
(2)以极性键相结合,具有正四面体结构的非极性分子是
(3)以极性键相结合,具有三角锥结构的极性分子是
(4)以极性键相结合,具有V结构的极性分子是
(5)以极性键相结合,而且分子极性最大的是
您最近一年使用:0次



