在HF、H2O、NH3、CH4、N2、CO2、HI分子中:
(1)以非极性键结合的非极性分子是________________________________ 。
(2)以极性键相结合,具有正四面体结构的非极性分子是______________ 。
(3)以极性键相结合,具有三角锥结构的极性分子是__________________ 。
(4)以极性键相结合,具有V结构的极性分子是______________________ 。
(5)以极性键相结合,而且分子极性最大的是________________ 。
(1)以非极性键结合的非极性分子是
(2)以极性键相结合,具有正四面体结构的非极性分子是
(3)以极性键相结合,具有三角锥结构的极性分子是
(4)以极性键相结合,具有V结构的极性分子是
(5)以极性键相结合,而且分子极性最大的是
9-10高二下·吉林·期中 查看更多[3]
河北省石家庄市鹿泉一中2017-2018学年高二3月月考化学试题(已下线)2009一2010年度吉林一中下学期高二期中考试化学卷(已下线)2011-2012学年吉林省汪清六中高二下学期期中考试化学试卷
更新时间:2018-03-29 01:51:06
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】根据所学知识填空:
(1)三原子分子常见的空间结构有__________ 形(如 )和
)和__________ 形(如 )。
)。
(2)四原子分子常见的空间结构有___________ 形和___________ 形,如甲醛( )分子呈
)分子呈___________ 形,键角约为___________ ;氨分子呈___________ 形,键角为___________ ;需要注意的是白磷分子呈___________ 形,键角为___________ 。
(3)五原子分子最常见的空间结构为___________ 形,如常见的 键角是
键角是___________ 。
(1)三原子分子常见的空间结构有
 )和
)和 )。
)。(2)四原子分子常见的空间结构有
 )分子呈
)分子呈(3)五原子分子最常见的空间结构为
 键角是
键角是
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】磷酸根离子的空间构型为___________ ,其中P的价层电子对数为___________ 、杂化轨道类型为___________ 。
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】如图是甲醛分子的模型,根据该图和所学化学知识回答下列问题:
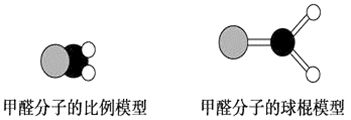
(1)甲醛分子中碳原子的杂化方式是__________ ,作出该判断的主要理由是__________________________ 。
(2)下列是对甲醛分子中碳氧键的判断,其中正确的是________ (填序号)。
①单键 ②双键 ③σ键 ④π键 ⑤σ键和π键
(3)甲醛分子中C—H键与C—H键间的夹角________ (填“=”、“>”或“<”)120°,出现该现象的主要原因是____________________________________________ 。

(1)甲醛分子中碳原子的杂化方式是
(2)下列是对甲醛分子中碳氧键的判断,其中正确的是
①单键 ②双键 ③σ键 ④π键 ⑤σ键和π键
(3)甲醛分子中C—H键与C—H键间的夹角
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】钛能与卤素单质发生反应,生成用途多样的卤化钛。
(1)卤族元素(F、Cl、Br、I)随着原子序数的递增,相关性质逐渐增强或变大的是___________。
(2) 易与
易与 结合,下列关于
结合,下列关于 分子说法错误的是___________。
分子说法错误的是___________。
(1)卤族元素(F、Cl、Br、I)随着原子序数的递增,相关性质逐渐增强或变大的是___________。
| A.元素的电负性 | B.简单离子的还原性 |
| C.气态氢化物的热稳定性 | D.最高价氧化物对应水化物的酸性 |
 易与
易与 结合,下列关于
结合,下列关于 分子说法错误的是___________。
分子说法错误的是___________。A.键角为 | B.是极性分子 |
C.含有 键 键 | D.中心原子采取 杂化 杂化 |
您最近半年使用:0次
【推荐2】CuSCN是一种生物防腐涂料,可用CuSO4、NaSCN、Na2SO3作原料,并用乙二醇或DMF作分散剂进行制备。
(1) Cu+基态核外电子排布式为____________ 。
(2) NaSCN中元素S、C、N的第一电离能由大到小的顺序为____________ ;Na2SO3中SO32-的空间构型为____________ (用文字描述)。
(3) 乙二醇(HOCH2CH2OH)与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为____________________ 。
(4) DMF(OHCNCH3CH3)分子中碳原子的轨道杂化类型为____________ ;1 mol DMF分子中含有σ键的数目为____________ 。
(1) Cu+基态核外电子排布式为
(2) NaSCN中元素S、C、N的第一电离能由大到小的顺序为
(3) 乙二醇(HOCH2CH2OH)与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为
(4) DMF(OHCNCH3CH3)分子中碳原子的轨道杂化类型为
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】有下列微粒:CH4 CO2 NH3 BF3 H2O HF填写下列空白:
(1)呈正四面体的是________ 。
(2)中心原子的轨道杂化类型为sp杂化的是________ ,为sp2杂化的是________ 。
(3)以极性键结合,而且分子极性最大的是________ 。
(4)以极性键结合,具有三角锥结构的极性分子是________ ,具有V形结构的极性分子是________ 。
(1)呈正四面体的是
(2)中心原子的轨道杂化类型为sp杂化的是
(3)以极性键结合,而且分子极性最大的是
(4)以极性键结合,具有三角锥结构的极性分子是
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在水中的溶解度,吡啶( )远大于苯,主要原因是①
)远大于苯,主要原因是①_______ ,②_______ 。
 )远大于苯,主要原因是①
)远大于苯,主要原因是①
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为原料,经过一系列反应可以得到 和
和 ,流程如图所示。请回答下列问题:
,流程如图所示。请回答下列问题: 分子为
分子为__________ (填“极性”或“非极性”)分子,该分子中F—B—F键角是______ 。
(2) 和过量NaF作用可生成
和过量NaF作用可生成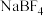 ,
, 的空间结构为
的空间结构为_________ ,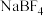 中
中______ (填“含有”或“不含”)配位键。
(3)与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为_________ ,层间作用力为________ 。
 和
和 ,流程如图所示。请回答下列问题:
,流程如图所示。请回答下列问题:
 分子为
分子为(2)
 和过量NaF作用可生成
和过量NaF作用可生成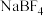 ,
, 的空间结构为
的空间结构为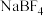 中
中(3)与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为
您最近半年使用:0次




