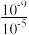常温下,相同体积的CH3COOH、HClO两种酸的稀溶液分别稀释时,溶液pH随加水量的变化如下图。下列说法正确的是
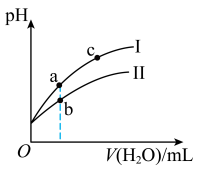

| A.图像中a点酸的总浓度等于b点酸的总浓度 |
| B.曲线Ⅰ表示HClO溶液稀释过程中pH的变化 |
C.图像中a、c两点处的溶液中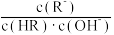 相等(HR代表CH3COOH或HClO) 相等(HR代表CH3COOH或HClO) |
| D.用0.1mol/L的NaOH溶液分别中和两种酸,CH3COOH溶液消耗碱的体积更多 |
更新时间:2023-12-25 10:38:19
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验能达到预期目的是
| 编号 | 实验内容 | 实验目的 |
| A | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| B | 室温下,用pH试纸测定浓度为0.1mol·L−1NaClO溶液和0.1mol·L−1 溶液的pH 溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| C | 等体积pH=2的HX和HY两种酸分别与足量的锌粒反应,排水法收集气体,HX放出的氢气多且反应速率快 | 证明HX酸性比HY强 |
| D | 制备无水 | 将氯化铁溶液在盐酸中蒸发结晶 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时,下列事实中能说明HA为弱电解质的是( )
① NaA溶液的pH>7 ②用HA溶液做导电实验时灯泡很暗
③ pH=2的HA溶液稀释至100倍,pH 约为3.1 ④HA的溶解度比HCl的小
⑤ 用HA溶液浸泡水壶中的水垢,可将其清除
① NaA溶液的pH>7 ②用HA溶液做导电实验时灯泡很暗
③ pH=2的HA溶液稀释至100倍,pH 约为3.1 ④HA的溶解度比HCl的小
⑤ 用HA溶液浸泡水壶中的水垢,可将其清除
| A.①②③ | B.①②⑤ | C.①③④ | D.①③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.一定温度下,将氨水稀释,NH3∙H2O的电离度增大,H2O的电离度也增大 |
| B.水中加酸加碱都会阻碍水的电离,所以c(H+)∙c(OH-)<10-14 |
| C.水中加酸,阻碍水的电离,所以c(H+)=c(OH-)<10-7mol∙L-1 |
| D.醋酸溶液加水稀释,溶液中所有微粒的浓度都会降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】使用如图装置探究溶液离子浓度变化,电导率不会出现“先减小后增大”现象的是
| A | B | C | D |  | |
| 试剂a | 稀硫酸 | 硫酸铁 | 醋酸 | 碳酸氢铵 | |
| 试剂b | 碳酸钠 | 氢氧化钡 | 氨水 | 氢氧化钙 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】乙二胺(H2NCH2CH2NH2)是二元弱碱(已知:25℃时,Kb1=10-4,Kb2=10-7),其水溶液与NH3水溶液的电离方式相似。现用锥形瓶装10 mL0.1 mol·L-1乙二胺溶液,用0.1 mol·L-1盐酸滴定。下列叙述错误 的是
| A.乙二胺在水溶液中的第一步电离方程式H2NCH2CH2NH2+H2O⇌[H2NCH2CH2NH3]++OH- |
| B.选用甲基橙作指示剂,可以很好地判断滴定终点 |
| C.滴入10.00 mL盐酸时,溶液呈碱性 |
| D.滴入20.00 mL盐酸时,混合溶液中有c(H2NCH2CH2NH2)+c([H2NCH2CH2NH3]+)+c([H3NCH2CH2NH3]2+)=c(Cl-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】草酸H2C2O4是二元弱酸。向100 mL 0.40 mol·L-1 H2C2O4溶液中加入1.0 mol·L-1NaOH或HCl溶液调节pH,加水控制溶液体积为200 mL。测得溶液中微粒的δ(x)随pH变化如图所示,其中δ(x)=
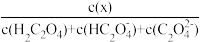 ,x代表微粒H2C2O4、
,x代表微粒H2C2O4、 或
或 。下列叙述正确的是
。下列叙述正确的是

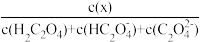 ,x代表微粒H2C2O4、
,x代表微粒H2C2O4、 或
或 。下列叙述正确的是
。下列叙述正确的是
A.曲线I是 的变化曲线 的变化曲线 |
B.pH=4时, |
C.c(H2C2O4)+c( )+c( )+c( )=0.40 mol·L-1 )=0.40 mol·L-1 |
D.c( )+c(OH-)= c(H2C2O4)+c(H+) )+c(OH-)= c(H2C2O4)+c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列溶液中微粒的物质的量浓度关系正确的是
| A.25℃时,向0.1mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) |
| B.25℃时,NaB溶液的pH=8,c(Na+)- c(B-)=9.9×10-7 mol·L-1 |
| C.0.1 mol·L-1NaHCO3溶液:c(Na+)>c(oH-)>c(HCO3-)>c(H+) |
| D.相同物质的量浓度的CH3COONa和NaClO的混合液中,各离子浓度的大小关系是:c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】运动员在剧烈运动后产生的乳酸会使肌肉麻痹疼痛,故常用液氮降温减少炎症和乳酸。已知乳酸(表示为HL,L-为乳酸根)是一元弱酸。25℃时,下列有关叙述不正确的是
| A.0.1mol/LHL溶液的pH>1 |
| B.0.1mol/LHL溶液加水稀释时,溶液中水电离出的c(H+)增大 |
C.0.1mol/LNaL溶液中: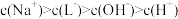 |
D.在HL和NaL组成的缓冲溶液中: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
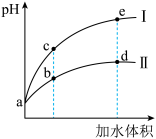
【推荐2】某温度下,将pH和体积均相同的HCl和 溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述不正确的是
溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述不正确的是
 溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述不正确的是
溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述不正确的是
A.稀释前溶液的浓度: |
| B.溶液中水的电离程度:b点<c点 |
C.从b点到d点,溶液中 逐渐增大 逐渐增大 |
D.在d点和e点均存在: (酸根阴离子) (酸根阴离子) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列叙述正确的是

A.将稀氨水逐滴加入稀硫酸中,当溶液的 时, 时,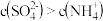 |
B.两种醋酸溶液的物质的量浓度分别为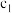 和 和 ,pH分别为a和 ,pH分别为a和 ,则 ,则 |
C. 的NaOH溶液与 的NaOH溶液与 的醋酸溶液等体积混合,滴入石蕊溶液呈红色 的醋酸溶液等体积混合,滴入石蕊溶液呈红色 |
D.向 的氨水中加入少量硫酸铵固体,则溶液中 的氨水中加入少量硫酸铵固体,则溶液中 增大 增大 |
您最近一年使用:0次