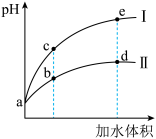
某温度下,将pH和体积均相同的HCl和 溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述不正确的是
溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述不正确的是
 溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述不正确的是
溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述不正确的是
A.稀释前溶液的浓度: |
| B.溶液中水的电离程度:b点<c点 |
C.从b点到d点,溶液中 逐渐增大 逐渐增大 |
D.在d点和e点均存在: (酸根阴离子) (酸根阴离子) |
2023·北京房山·一模 查看更多[10]
四川省宜宾市兴文第二中学校2023-2024学年高二下学期开学化学试题吉林省辽源市田家炳高中友好学校七十六届期末联考2023-2024学年高二上学期1月期末化学试题江西省宜丰中学创新部2023-2024学年高一上学期10月月考化学试题【定心卷】3.1.2 弱电解质的电离平衡随堂练习-人教版2023-2024学年选择性必修1(已下线)考点1 电离平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)第29讲弱电解质的电离江西省丰城中学2022-2023学年高一下学期4月期中考试化学试题(已下线)专题16 水溶液中的离子平衡四川省凉山州宁南中学2022-2023学年高二下学期第一次月考化学试题北京市房山区2023届高三一模考试化学试题
更新时间:2023-03-30 15:09:24
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】为了探究强弱电解质对反应速率的影响,分别向试管1和试管2中加入等浓度、等体积的盐酸和醋酸溶液,再同时加入相同质量的锌粉(不足),下列说法正确的是(不考虑酸的挥发)
| A.反应刚开始时,试管2中反应更剧烈 |
| B.反应结束后,试管1中产生的气体更多 |
C.反应结束后,试管2中溶液含有的 浓度更小 浓度更小 |
D.生成相同体积(相同条件下)的 时,试管1消耗的时间更长 时,试管1消耗的时间更长 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列关于电解质溶液的叙述正确的是
| A.常温下物质的量浓度相等①NH4HSO4、②(NH4)2SO4、③(NH4)2CO3三种溶液中c(NH4+) ①<②<③ |
| B.在纯水中加入少量硫酸或硫酸铵,均可抑制水的电离 |
| C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,向10mL0.1mol/L的某一元酸HR溶液中逐滴加入0.1mol/L氨水,所得溶液pH及导电能力变化如图。下列分析不正确的是( )
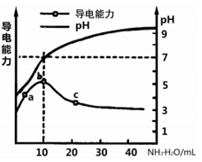
| A.a~b点导电能力增强说明HR为弱酸 |
| B.a、b点所示溶液中水的电离程度不相同 |
| C.b恰好完全中和,pH=7说明NH4R没有水解 |
| D.c 点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,向0.1 mol/L H3AsO4和0.1 mol/L H3AsO3溶液中分别逐滴加入0.1 mol/L NaOH溶液,溶液中含砷微粒的物质的量分数与溶液pH的关系分别如图1和图2所示。下列说法不正确的是

A.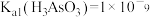 |
| B.相同条件下,酸性H3AsO4>H3AsO3 |
C.b点溶液中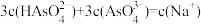 |
D.Na3AsO4溶液中,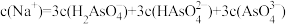 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定温度下, 溶液中存在如下平衡:
溶液中存在如下平衡: ,下列有关说法正确的是
,下列有关说法正确的是
 溶液中存在如下平衡:
溶液中存在如下平衡: ,下列有关说法正确的是
,下列有关说法正确的是| A.加水稀释,溶液中所有离子浓度都减小 |
B.与等体积等浓度的醋酸混合后的溶液中: |
C.若通入适量的HCl后溶液呈中性,则溶液中: |
D.升高温度后, 变大 变大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
名校
【推荐2】醋酸溶液中存在电离平衡CH3COOH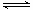 H++CH3COO-,不正确的是
H++CH3COO-,不正确的是
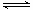 H++CH3COO-,不正确的是
H++CH3COO-,不正确的是| A.醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) |
| B.常温下0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)减小 |
| C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动 |
| D.常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】醋酸铅因有甜味而被称为“铅糖”,它有毒但能入药,又知(CH3COO)2Pb可溶于水,硝酸铅与醋酸钠溶液反应的离子方程式为Pb2++2CH3COO-=(CH3COO)2Pb。下列有关说法正确的是
| A.0.1mol·L-1的醋酸铅溶液与0.1mol·L-1的醋酸钠溶液相比,c(Pb2+)=c(Na+) |
| B.0.1mol·L-1的醋酸铅溶液与0.1mol·L-1的醋酸钠溶液相比,c(CH3COO-)之比等于2∶1 |
| C.将0.1mol·L-1的醋酸铅溶液加水稀释10倍,c(Pb2+)∶c(CH3COO-)=2∶1 |
| D.醋酸铅是共价化合物,溶液可能导电性很弱 |
您最近一年使用:0次




