 、
、 、
、 和
和 都是强酸,它们的酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:
都是强酸,它们的酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:| 酸 |  |  |  |  |
 |  | 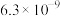 |  | 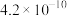 |
| A.在冰醋酸中这四种酸都没有完全电离 |
B.在冰醋酸中 是这四种酸中最强的酸 是这四种酸中最强的酸 |
| C.水不能区分这四种酸的强弱,但冰醋酸可以区分这四种酸的强弱 |
D.在冰醋酸中的电离方程式为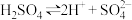 |
23-24高二·全国·假期作业 查看更多[3]
(已下线)寒假作业05 电离平衡及溶液的酸碱性-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)(已下线)专题04 电离平衡 水的电离和溶液的pH-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)安徽省马鞍山市当涂第一中学2023-2024学年高二上学期1月期末化学试题
更新时间:2024-01-04 09:50:15
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】已知 的电离平衡常数:
的电离平衡常数: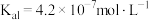 和
和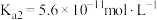 ,
, 的电离平衡常数:
的电离平衡常数: 。在反应
。在反应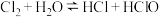 达到平衡后,要使
达到平衡后,要使 的浓度增大可加入
的浓度增大可加入
 的电离平衡常数:
的电离平衡常数: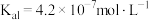 和
和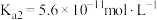 ,
, 的电离平衡常数:
的电离平衡常数: 。在反应
。在反应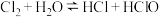 达到平衡后,要使
达到平衡后,要使 的浓度增大可加入
的浓度增大可加入A. | B. | C. | D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列物质在水溶液中的电离方程式书写正确的是
| A.AlCl3=Al3++3Cl- | B.NaHCO3=Na++H++ |
| C.KClO3=K++Cl-+3O2- | D.HClO=H++ClO- |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列叙述正确的是( )
①0.1mol•L﹣1氨水中,c(OH﹣)=c(NH4+)
②10mL 0.02 mol•L﹣1 HCl溶液与10mL 0.02 mol•L﹣1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=12
③在0.1 mol•L﹣1CH3COONa溶液中,c(OH﹣)=c(CH3COOH)+c(H+)
④0.1 mol•L﹣1某二元弱酸的强碱盐NaHA溶液中,c(Na+)=2c(A2﹣)+c(HA﹣)+c(H2A)
①0.1mol•L﹣1氨水中,c(OH﹣)=c(NH4+)
②10mL 0.02 mol•L﹣1 HCl溶液与10mL 0.02 mol•L﹣1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=12
③在0.1 mol•L﹣1CH3COONa溶液中,c(OH﹣)=c(CH3COOH)+c(H+)
④0.1 mol•L﹣1某二元弱酸的强碱盐NaHA溶液中,c(Na+)=2c(A2﹣)+c(HA﹣)+c(H2A)
| A.①②③ | B.②③ | C.②③④ | D.①④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】室温下,向10 mL pH=11的氨水中加水稀释后,下列说法正确的是
| A.溶液中导电粒子的数目减少 |
| B.将10 mL pH=11的氨水与10 mL pH=3的盐酸混合,所得溶液的pH=7 |
C.溶液中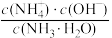 不变 不变 |
| D.一水合氨的电离程度增大,c(OH-)亦增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】常温下,向10mL  草酸
草酸 溶液中逐滴加入等浓度的NaOH溶液。有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是
溶液中逐滴加入等浓度的NaOH溶液。有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是

 草酸
草酸 溶液中逐滴加入等浓度的NaOH溶液。有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是
溶液中逐滴加入等浓度的NaOH溶液。有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是
| A.在溶液中水解程度大于电离程度 |
B.当V(NaOH) = 10 mL时溶液中存在: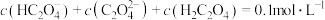 |
C.当V(NaOH) = 15 mL时,溶液中存在: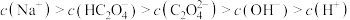 |
D.当V(NaOH) = 20 mL时,溶液中存在: |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】下列关于电解质溶液的叙述正确的是
| A.pH均为4的H2SO4、NH4Cl溶液中,水的电离程度相同 |
B.等pH的NaOH溶液与NH3•H2O 稀释后pH的变化如右图所示,则曲线I表示的是NaOH溶液的稀释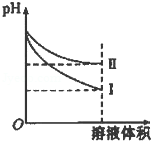 |
| C.1mol/LNa2CO3溶液中存在:c(Na+)=2c(CO32﹣ )+2c(HCO3﹣) |
| D.向某温度的氨水中通入盐酸,则氨水的电离常数增大 |
您最近一年使用:0次



