羟基自由基(·OH,电中性)是一种活性含氧粒子。常温下,利用·OH 处理含苯酚(C6H6O)废水, 可将其转化为无毒的氧化物。
(1)·OH 中氧元素的化合价为___________ 。
(2)pH=3时Fe2+催化H2O2的分解过程中产生·OH中间体,催化循环反应如下。将ii补充完整。
i.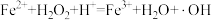
ii. ,
,__________________ 。
(3)已知:羟基自由基容易发生猝灭2·OH=H2O2。用H2O2分解产生的·OH脱除苯酚,当其他条件不变时,不同温度下,苯酚的浓度随时间的变化如图1所示。0~20min 时, 温度从40℃上升到50℃,反应速率基本不变的原因是___________ 。
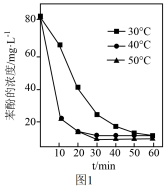
(4)利用电化学高级氧化技术可以在电解槽中持续产生·OH,使处理含苯酚废水更加高效,装置如图2所示。已知 a 极主要发生的反应是(O2生成H2O2,然后在电解液中产生·OH,并迅速与苯酚(C6H6O)反应。

①b极连接电源的___________ 极。
②a极的电极反应式为___________ 。
③电解液中发生的主要反应的方程式是___________ 、___________ 。
(1)·OH 中氧元素的化合价为
(2)pH=3时Fe2+催化H2O2的分解过程中产生·OH中间体,催化循环反应如下。将ii补充完整。
i.
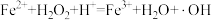
ii.
 ,
,(3)已知:羟基自由基容易发生猝灭2·OH=H2O2。用H2O2分解产生的·OH脱除苯酚,当其他条件不变时,不同温度下,苯酚的浓度随时间的变化如图1所示。0~20min 时, 温度从40℃上升到50℃,反应速率基本不变的原因是

(4)利用电化学高级氧化技术可以在电解槽中持续产生·OH,使处理含苯酚废水更加高效,装置如图2所示。已知 a 极主要发生的反应是(O2生成H2O2,然后在电解液中产生·OH,并迅速与苯酚(C6H6O)反应。

①b极连接电源的
②a极的电极反应式为
③电解液中发生的主要反应的方程式是
更新时间:2024-01-09 11:48:10
|
相似题推荐
【推荐1】(1)工业生产甲醇的常用方法是:
CO(g)+2H2(g) CH3OH(g)△H=-90.8kJ/mol。
CH3OH(g)△H=-90.8kJ/mol。
已知:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol
H2(g)+1/2O2(g)=H2O(g)△H=-241.8kJ/mol
①H2的燃烧热为______ kJ/mol。
②CH3OH(g)+O2(g) CO(g)+2H2O(g)的反应热△H=
CO(g)+2H2O(g)的反应热△H=_____________ 。
(2)N2、H2合成氨气为放热反应。800K时向下列起始体积相同的密闭容器中充入2molN2、3molH2H2,甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙是绝热容器,三容器各自建立化学平衡。
①达到平衡时,平衡常数K甲________ K乙________ K丙。
②达到平衡时N2的浓度c甲(N2)________ c乙(N2),c乙(N2)________ c丙(N2)。
③对甲、乙、丙三容器的描述,以下说法正确的是________ 。
A.乙容器气体密度不再变化时,说明此反应已达到平衡状态
B.在甲中充入稀有气体He,化学反应速率增大
C.向甲容器中充入氨气,正向速率减小,逆向速率增大
D.丙容器温度不再变化时说明已达平衡状态
CO(g)+2H2(g)
 CH3OH(g)△H=-90.8kJ/mol。
CH3OH(g)△H=-90.8kJ/mol。已知:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol
H2(g)+1/2O2(g)=H2O(g)△H=-241.8kJ/mol
①H2的燃烧热为
②CH3OH(g)+O2(g)
 CO(g)+2H2O(g)的反应热△H=
CO(g)+2H2O(g)的反应热△H=(2)N2、H2合成氨气为放热反应。800K时向下列起始体积相同的密闭容器中充入2molN2、3molH2H2,甲容器在反应过程中保持压强不变,乙容器保持体积不变,丙是绝热容器,三容器各自建立化学平衡。
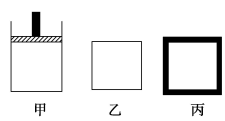
①达到平衡时,平衡常数K甲
②达到平衡时N2的浓度c甲(N2)
③对甲、乙、丙三容器的描述,以下说法正确的是
A.乙容器气体密度不再变化时,说明此反应已达到平衡状态
B.在甲中充入稀有气体He,化学反应速率增大
C.向甲容器中充入氨气,正向速率减小,逆向速率增大
D.丙容器温度不再变化时说明已达平衡状态
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上可通过煤的液化合成甲醇,主反应为:CO(g)+2H2(g)=CH3OH(l) △H=x
(1)已知常温下CH3OH、H2和CO的燃烧热分别为726.5kl/mol、285.5kJ/mol、283.0kJ/mol,则x=_______ ;为提高合成甲醇反应的选择性,关键因素是___________ 。
(2)TK下,在容积为1.00 L的某密闭容器中进行上述反应(CH3OH为气体),相关数据如图。
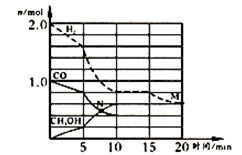
①该反应0-10min的平均速率v(H2)=_______ ;M和N点的逆反应速率较大的是______ (填“v逆(M)”、“v逆(N)”或“不能确定”) 。
②10min时容器内CO的体积分数为_______ 。相同条件下,若起始投料加倍,达平衡时,CO的体积分数将________ (填“增大”、“减小”或“不变”)
③对于气相反应,常用某组分(B)的平衡压强(PB)代替物质的量浓度(CB)表示平衡常数(以Kp表示),其中,PB=P总×B的体积分数;若在TK下平衡气体总压强xatm,则该反应Kp=____ (计算表达式)。实验测得不同温度下的lnK(化学平衡常数K的自然对数)如图,请分析lnK随T呈现上述变化趋势的原因是:____________ 。

(1)已知常温下CH3OH、H2和CO的燃烧热分别为726.5kl/mol、285.5kJ/mol、283.0kJ/mol,则x=
(2)TK下,在容积为1.00 L的某密闭容器中进行上述反应(CH3OH为气体),相关数据如图。

①该反应0-10min的平均速率v(H2)=
②10min时容器内CO的体积分数为
③对于气相反应,常用某组分(B)的平衡压强(PB)代替物质的量浓度(CB)表示平衡常数(以Kp表示),其中,PB=P总×B的体积分数;若在TK下平衡气体总压强xatm,则该反应Kp=

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】低碳经济成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。结合下列有关图示和所学知识回答:

(1)用 催化加氢可以制取乙烯:
催化加氢可以制取乙烯: 。若该反应体系的能量随反应过程变化关系如上图所示,则该反应属于
。若该反应体系的能量随反应过程变化关系如上图所示,则该反应属于_______ 反应(填“吸热”或“放热”),该反应的
______ (用含a、b的式子表示)。又知:相关化学键的键能如下表所示,实验测得上述反应的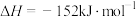 ,则表中的
,则表中的
______ 。
注:乙烯结构如图:
(2)在 完全燃烧生成
完全燃烧生成 和液态水的反应中,每有5mol电子转移时,放出650kJ的热量,其燃烧热的热化学方程式为
和液态水的反应中,每有5mol电子转移时,放出650kJ的热量,其燃烧热的热化学方程式为_________________________________ 。
(3)工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:

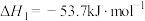 ,
,

 ,
,
则

______  。为提高该反应中
。为提高该反应中 的转化率,可采用的方式有
的转化率,可采用的方式有_______ 。
A加入合适的催化剂 B.升高温度 C.增大 浓度 D.减小压强
浓度 D.减小压强

(1)用
 催化加氢可以制取乙烯:
催化加氢可以制取乙烯: 。若该反应体系的能量随反应过程变化关系如上图所示,则该反应属于
。若该反应体系的能量随反应过程变化关系如上图所示,则该反应属于
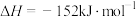 ,则表中的
,则表中的
化学键 |
| H-H |
| C-H | H-O |
健能 | 803 | 436 | x | 414 | 464 |

(2)在
 完全燃烧生成
完全燃烧生成 和液态水的反应中,每有5mol电子转移时,放出650kJ的热量,其燃烧热的热化学方程式为
和液态水的反应中,每有5mol电子转移时,放出650kJ的热量,其燃烧热的热化学方程式为(3)工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:
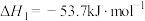 ,
,
 ,
,则


 。为提高该反应中
。为提高该反应中 的转化率,可采用的方式有
的转化率,可采用的方式有A加入合适的催化剂 B.升高温度 C.增大
 浓度 D.减小压强
浓度 D.减小压强
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】(1)一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示:
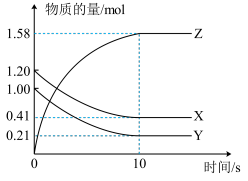
①该反应的化学方程式为_______ 。
②10 s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示:

则下列说法符合该图像的是_______ 。
A.t1时刻,增大了X的浓度
B.t1时刻,升高了体系温度
C.t1时刻,缩小了容器体积
D.t1时刻,使用了催化剂
(2)在一个恒温恒容的密闭容器中发生反应2CO(g)+2NO(g) N2(g) +2CO2(g),能表明已达到平衡状态的标志有
N2(g) +2CO2(g),能表明已达到平衡状态的标志有 ( )
A.混合气体的压强保持不变 B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变 D.气体的总质量
E.2v正(CO)=v逆(N2) F.t min内生成2molN2同时消耗1molCO2
(3)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g) N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
①0∼5min内,以表示的该反应速率v(CO2)=_______ ,最终达平衡时NO的转化率a=_______ ,该温度T℃下的平衡常数K=_______ 。
②保持温度T℃不变,向该2L密闭容器中加入该四种反应混合物各2mol,则此时反应_______ 移动(填“正向”、“逆向”或“不”);最终达平衡时容器中气体的平均摩尔质量为_______ g·mol-1。

①该反应的化学方程式为
②10 s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示:

则下列说法符合该图像的是
A.t1时刻,增大了X的浓度
B.t1时刻,升高了体系温度
C.t1时刻,缩小了容器体积
D.t1时刻,使用了催化剂
(2)在一个恒温恒容的密闭容器中发生反应2CO(g)+2NO(g)
 N2(g) +2CO2(g),能表明已达到平衡状态的标志有
N2(g) +2CO2(g),能表明已达到平衡状态的标志有 A.混合气体的压强保持不变 B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变 D.气体的总质量
E.2v正(CO)=v逆(N2) F.t min内生成2molN2同时消耗1molCO2
(3)向容积为2L的密闭容器中加入活性炭(足量)和NO,发生反应C(s)+2NO(g)
 N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。
N2(g)+CO2(g),NO和N2的物质的量变化如下表所示。| 条件 | 保持温度为T/℃ | ||||||
| 时间 | 0 | 5min | 10min | 15min | 20min | 25min | 30min |
| NO物质的量/mol | 2.0 | 1.4 | 1.0 | 0.70 | 0.50 | 0.40 | 0.40 |
| N2物质的量/mol | 0 | 0.3 | 0.50 | 0.65 | 0.75 | 0.80 | 0.80 |
①0∼5min内,以表示的该反应速率v(CO2)=
②保持温度T℃不变,向该2L密闭容器中加入该四种反应混合物各2mol,则此时反应
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】 在工业生产中具有重要作用。回答下列问题:
在工业生产中具有重要作用。回答下列问题:
Ⅰ.已知 ,在
,在 的密闭容器中充入
的密闭容器中充入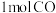 和
和 ,5分钟后气体压强减小10%。
,5分钟后气体压强减小10%。
(1)以 表示的反应速率为
表示的反应速率为_______ 。
(2)能说明该反应已达平衡的是_______ 。(填编号)
a. b.
b.
c.混合气体的密度不变 d.混合气体的平均相对分子质量不变
Ⅱ.工业以 为原料合成
为原料合成 的反应为:
的反应为: 。
。
(3)在一定温度和压强下,以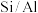 混合物作为催化剂,向反应炉中匀速通入
混合物作为催化剂,向反应炉中匀速通入 ,不同硅铝比(Ⅰ、Ⅱ)与生成
,不同硅铝比(Ⅰ、Ⅱ)与生成 的速率关系如图所示。下列说法正确的是
的速率关系如图所示。下列说法正确的是_______ 。(填编号)

a.合适的硅铝比为0.15
b.温度越低越有利于工业合成
c.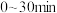 内,
内, 的产量I>II
的产量I>II
d.在原料气 中混入适量的惰性气体对
中混入适量的惰性气体对 的生成速率无影响
的生成速率无影响
(4)若在恒温恒容密闭容器中通入一定量的 ,达平衡时
,达平衡时 ,再充入少量
,再充入少量 重新达平衡时
重新达平衡时 ,则m
,则m_______ n(选填“<”、“>”或“=”),理由是_______ 。
(5)反应相同时间测得 的转化率随反应温度变化情况如图所示。在图中画出,其他条件不变,增大压强(催化剂不失活)情况下,
的转化率随反应温度变化情况如图所示。在图中画出,其他条件不变,增大压强(催化剂不失活)情况下, 的转化率随温度变化图
的转化率随温度变化图_______ 。

Ⅲ.实验室模拟反应 ,再将混合气体通入稀
,再将混合气体通入稀 溶液洗气制
溶液洗气制 。(忽略溶液体积变化)
。(忽略溶液体积变化)
(6)洗气过程中溶液
_______ ,水的电离程度_______ 。(均填变化情况)
 在工业生产中具有重要作用。回答下列问题:
在工业生产中具有重要作用。回答下列问题:Ⅰ.已知
 ,在
,在 的密闭容器中充入
的密闭容器中充入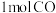 和
和 ,5分钟后气体压强减小10%。
,5分钟后气体压强减小10%。(1)以
 表示的反应速率为
表示的反应速率为(2)能说明该反应已达平衡的是
a.
 b.
b.
c.混合气体的密度不变 d.混合气体的平均相对分子质量不变
Ⅱ.工业以
 为原料合成
为原料合成 的反应为:
的反应为: 。
。(3)在一定温度和压强下,以
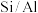 混合物作为催化剂,向反应炉中匀速通入
混合物作为催化剂,向反应炉中匀速通入 ,不同硅铝比(Ⅰ、Ⅱ)与生成
,不同硅铝比(Ⅰ、Ⅱ)与生成 的速率关系如图所示。下列说法正确的是
的速率关系如图所示。下列说法正确的是
a.合适的硅铝比为0.15
b.温度越低越有利于工业合成

c.
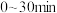 内,
内, 的产量I>II
的产量I>IId.在原料气
 中混入适量的惰性气体对
中混入适量的惰性气体对 的生成速率无影响
的生成速率无影响(4)若在恒温恒容密闭容器中通入一定量的
 ,达平衡时
,达平衡时 ,再充入少量
,再充入少量 重新达平衡时
重新达平衡时 ,则m
,则m(5)反应相同时间测得
 的转化率随反应温度变化情况如图所示。在图中画出,其他条件不变,增大压强(催化剂不失活)情况下,
的转化率随反应温度变化情况如图所示。在图中画出,其他条件不变,增大压强(催化剂不失活)情况下, 的转化率随温度变化图
的转化率随温度变化图
Ⅲ.实验室模拟反应
 ,再将混合气体通入稀
,再将混合气体通入稀 溶液洗气制
溶液洗气制 。(忽略溶液体积变化)
。(忽略溶液体积变化)(6)洗气过程中溶液

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】甲醇是重要的有机化工原料,目前世界甲醇年产量超过2.1×107吨,在能源紧张的今天,甲醇的需求也在增大。
甲醇的合成方法是:(ⅰ)CO(g)+2H2(g) CH3OH(g) ΔH=-90.1kJ·mol-1
CH3OH(g) ΔH=-90.1kJ·mol-1
另外:(ⅱ)2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ·mol-1
(ⅲ)2H2(g)+O2(g)=2H2O(l) ΔH=-572.0kJ·mol-1
若混合气体中有二氧化碳存在时,还发生下列反应:
(ⅳ)CO2(g)+H2(g) CO(g)+H2O(g) ΔH=+41.1kJ·mol-1
CO(g)+H2O(g) ΔH=+41.1kJ·mol-1
(1)甲醇的燃烧热为____ kJ·mol-1。
(2)在碱性条件下利用一氯甲烷(CH3Cl)水解也可制备少量的甲醇,该反应的化学方程式为___ 。
(3)若反应在密闭恒容绝热容器中进行,反应(ⅳ)对合成甲醇反应中CO的转化率的影响是___ 。
a.增大 b.减小 c.无影响 d.无法判断
(4)在恒温恒容的密闭容器中发生反应(ⅰ),各物质的浓度如表:
①x=___ 。
②该温度下,反应(ⅰ)的平衡常数K=___ 。
③反应进行到第2min时,改变了反应条件,改变的这个条件可能是___ (填序号)。
a.使用催化剂 b.降低温度 c.增加H2的浓度
(5)如图是温度、压强与反应(ⅰ)中CO转化率的关系:

①由图像可知,较低温度时,CO转化率对___ (选填“温度”或“压强”)敏感。
②由图像可知,温度越低,压强越大,CO转化率越高,但实际生产往往采用300~400℃和10MPa的条件,其原因是___ 。
(6)在一容积为2L的密闭容器内加入2mol的CO和6mol的H2,在一定条件下发生反应(ⅰ)。该反应的逆反应速率与时间的关系如图所示:

①由图可知反应在t1、t3、t7时都达到了平衡,而在t2、t8时都改变了条件,试判断t8时改变的条件可能是___ 。
②若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线___ 。
甲醇的合成方法是:(ⅰ)CO(g)+2H2(g)
 CH3OH(g) ΔH=-90.1kJ·mol-1
CH3OH(g) ΔH=-90.1kJ·mol-1另外:(ⅱ)2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ·mol-1
(ⅲ)2H2(g)+O2(g)=2H2O(l) ΔH=-572.0kJ·mol-1
若混合气体中有二氧化碳存在时,还发生下列反应:
(ⅳ)CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=+41.1kJ·mol-1
CO(g)+H2O(g) ΔH=+41.1kJ·mol-1(1)甲醇的燃烧热为
(2)在碱性条件下利用一氯甲烷(CH3Cl)水解也可制备少量的甲醇,该反应的化学方程式为
(3)若反应在密闭恒容绝热容器中进行,反应(ⅳ)对合成甲醇反应中CO的转化率的影响是
a.增大 b.减小 c.无影响 d.无法判断
(4)在恒温恒容的密闭容器中发生反应(ⅰ),各物质的浓度如表:
| 时间/min 浓度/mol·L-1 | c(CO) | c(H2) | c(CH3OH) |
| 0 | 0.8 | 1.6 | 0 |
| 2 | 0.6 | x | 0.2 |
| 4 | 0.3 | 0.6 | 0.5 |
| 6 | 0.3 | 0.6 | 0.5 |
①x=
②该温度下,反应(ⅰ)的平衡常数K=
③反应进行到第2min时,改变了反应条件,改变的这个条件可能是
a.使用催化剂 b.降低温度 c.增加H2的浓度
(5)如图是温度、压强与反应(ⅰ)中CO转化率的关系:

①由图像可知,较低温度时,CO转化率对
②由图像可知,温度越低,压强越大,CO转化率越高,但实际生产往往采用300~400℃和10MPa的条件,其原因是
(6)在一容积为2L的密闭容器内加入2mol的CO和6mol的H2,在一定条件下发生反应(ⅰ)。该反应的逆反应速率与时间的关系如图所示:

①由图可知反应在t1、t3、t7时都达到了平衡,而在t2、t8时都改变了条件,试判断t8时改变的条件可能是
②若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】MnO2是重要化工原料,由软锰矿制备MnO2的一种工艺流程如下:

资料:①软锰矿的主要成分为MnO2,主要杂质有 和
和
②金属离子沉淀的pH
③该工艺条件下,MnO2与 不反应。
不反应。
(1)溶出
①溶出前,软锰矿需研磨。目的是_______ 。
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示。

i.II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是_______ 。
ii.若Fe2+全部来自于反应 ,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2。而实际比值(0.9)小于2,原因是
,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2。而实际比值(0.9)小于2,原因是_______ 。
(2)纯化
已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2,后加入 ,调溶液
,调溶液 ,说明试剂加入顺序及调节pH的原因:
,说明试剂加入顺序及调节pH的原因:_______ 。
(3)电解
Mn2+纯化液经电解得MnO2。生成MnO2的电极反应式是_______ 。

资料:①软锰矿的主要成分为MnO2,主要杂质有
 和
和
②金属离子沉淀的pH
 | 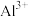 | 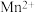 |  | |
| 开始沉淀时 | 1.5 | 3.4 | 5.8 | 6.3 |
| 完全沉淀时 | 2.8 | 4.7 | 7.8 | 8.3 |
 不反应。
不反应。(1)溶出
①溶出前,软锰矿需研磨。目的是
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示。

i.II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是
ii.若Fe2+全部来自于反应
 ,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2。而实际比值(0.9)小于2,原因是
,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2。而实际比值(0.9)小于2,原因是(2)纯化
已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2,后加入
 ,调溶液
,调溶液 ,说明试剂加入顺序及调节pH的原因:
,说明试剂加入顺序及调节pH的原因:(3)电解
Mn2+纯化液经电解得MnO2。生成MnO2的电极反应式是
您最近一年使用:0次
【推荐2】LiMn2O4作为一种新型锂电池正极材料受到广泛关注。由菱锰矿(MnCO3,含有少量Si、Fe、Ni、Al等元素)制备LiMn2O4的流程如下:
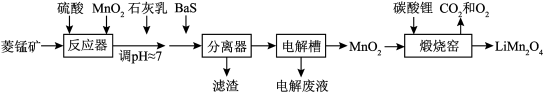
已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为___________ 。
(2)加入MnO2的作用是___________ 。
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=___________ mol·L-1;用石灰乳调节至pH≈7,除去的金属离子是___________ 。
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有NiS和___________ 。
(5)在电解槽中,发生电解反应的离子方程式为___________ 。随着电解反应进行,为保持电解液成分稳定,应不断___________ 。电解废液可在反应器中循环利用。
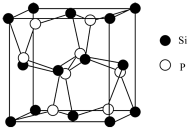
(6)Si与P形成的某化合物晶体的晶胞如图。该晶体类型是___________ ,该化合物的化学式为___________ 。

已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为
(2)加入MnO2的作用是
(3)溶矿反应完成后,反应器中溶液pH=4,此时c(Fe3+)=
(4)加入少量BaS溶液除去Ni2+,生成的沉淀有NiS和
(5)在电解槽中,发生电解反应的离子方程式为
(6)Si与P形成的某化合物晶体的晶胞如图。该晶体类型是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】一定条件下,二氧化碳可合成低碳烯烃,缓解温室效应、充分利用碳资源。
(1)已知:①C2H4(g)+2O2(g)=2CO2(g)+2H2(g) △H1
②2H2(g)+O2(g)=2H2O(l) △H2
③H2O(l)=H2O(g) △H3
④2CO2(g)+6H2(g) C2H4(g)+4H2O(g) △H4
C2H4(g)+4H2O(g) △H4
则△H4=______ (用△H1、△H2、△H3表示)。
(2)反应④的反应温度、投料比[ =x]对CO2平衡转化率的影响如图所示:
=x]对CO2平衡转化率的影响如图所示:
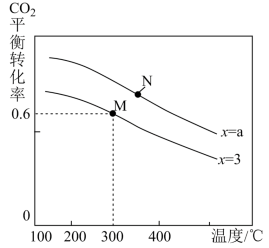
图1
①a______ 3(填“>”“<”或“=”,下同);M、N两点反应的平衡常数KM_____ KN。
②300℃,往6L反应容器中加入3molH2、1molCO2,反应10min达到平衡。求0到10min氢气的平均反应速率为_____ 。
(3)中科院兰州化学物理研究所用Fe3(CO)12/ZSM-5催化CO2加氢合成低碳烯烃反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图:
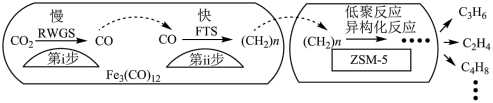
催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如表:
①欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM-5中添加_____ 助剂效果最好。
②下列说法正确的是______ (填标号)。
a.第i步反应为CO2+H2 CO+H2O
CO+H2O
b.第i步反应的活化能低于第ⅱ步
c.催化剂助剂生要在低聚反应、异构化反应环节起作用
d.Fe3(CO)12/ZSM-5使CO2加氢合成低碳烯烃的△H减小
e.添加不同助剂后,反应的平衡常数各不相同
(4)2018年,强碱性电催化还原CO2制乙烯研究取得突破进展,原理如图所示:
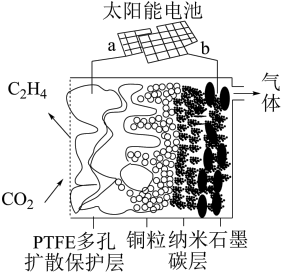
已知PTFE浸泡了饱和KCl溶液,请写出阴极的电极反应:_____ 。
(1)已知:①C2H4(g)+2O2(g)=2CO2(g)+2H2(g) △H1
②2H2(g)+O2(g)=2H2O(l) △H2
③H2O(l)=H2O(g) △H3
④2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g) △H4
C2H4(g)+4H2O(g) △H4则△H4=
(2)反应④的反应温度、投料比[
 =x]对CO2平衡转化率的影响如图所示:
=x]对CO2平衡转化率的影响如图所示:
图1
①a
②300℃,往6L反应容器中加入3molH2、1molCO2,反应10min达到平衡。求0到10min氢气的平均反应速率为
(3)中科院兰州化学物理研究所用Fe3(CO)12/ZSM-5催化CO2加氢合成低碳烯烃反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图:

催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如表:
| 助剂 | CO2转化率(%) | 各产物在所有产物中的占比(%) | ||
| C2H4 | C3H6 | 其他 | ||
| Na | 42.5 | 35.9 | 39.6 | 24.5 |
| K | 27.2 | 75.6 | 22.8 | 1.6 |
| Cu | 9.8 | 80.7 | 12.5 | 6.8 |
②下列说法正确的是
a.第i步反应为CO2+H2
 CO+H2O
CO+H2Ob.第i步反应的活化能低于第ⅱ步
c.催化剂助剂生要在低聚反应、异构化反应环节起作用
d.Fe3(CO)12/ZSM-5使CO2加氢合成低碳烯烃的△H减小
e.添加不同助剂后,反应的平衡常数各不相同
(4)2018年,强碱性电催化还原CO2制乙烯研究取得突破进展,原理如图所示:

已知PTFE浸泡了饱和KCl溶液,请写出阴极的电极反应:
您最近一年使用:0次






