 是一种强温室气体,且易形成颗粒性污染物,研究
是一种强温室气体,且易形成颗粒性污染物,研究 的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高
的分解对环境保护有重要意义。碘蒸气的存在能大幅度提高 的分解速率,反应历程如下:
的分解速率,反应历程如下:第一步
 (快反应)
(快反应)第二步
 (慢反应)
(慢反应)第三步
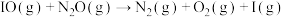 (快反应)
(快反应)实验表明,含碘时
 的分解速率方程
的分解速率方程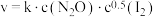 (k为速率常数)。下列表述正确的是
(k为速率常数)。下列表述正确的是| A.IO为反应的中间产物 | B.第一步对总反应速率起决定作用 |
C. 浓度与 浓度与 分解速率无关 分解速率无关 | D.第二步活化能比第三步小 |
更新时间:2024-01-14 21:55:32
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】丙烯与HBr发生加成反应的机理及反应体系中的能量变化如图所示,下列说法错误的是
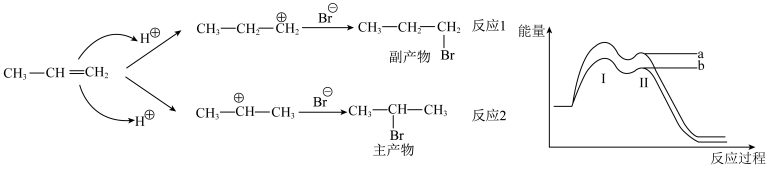

| A.反应2放出热量更多 |
| B.相同条件下反应2的速率比反应1大 |
| C.对于反应1和反应2,第Ⅰ步都是反应的决速步骤 |
| D.曲线a表示的是反应2的能量变化图 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是( )
| A.化学反应速率只能加快不能减慢 |
| B.增加反应物的用量一定能增大反应速率 |
| C.同质量的镁和铝分别与同浓度盐酸反应剧烈程度相同 |
| D.反应物的性质是决定化学反应速率的主要因素 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】某探究性学习小组利用 溶液和酸性
溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。
溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。
(1)通过实验A、B可探究_______ (填外部因素)的改变对反应速率的影响,其中 =
=_______ ;通过实验_______ 可探究温度变化对化学反应速率的影响。
(2)若 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是_______ ;利用实验B中数据计算,用 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为_______ 。
 溶液和酸性
溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。
溶液之间的反应来探究外界条件改变对化学反应速率的影响,实验如下。| 实验序号 | 实验温度/K |  溶液(含硫酸) 溶液(含硫酸) |  溶液 溶液 |  | 溶液颜色褪至无色时 所需时间/s | ||
| V/mL | 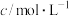 | V/mL | 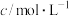 | V/mL | |||
| A | 293 | 2 | 0.02 | 5 | 0.1 | 5 |  |
| B |  | 2 | 0.02 | 4 | 0.1 |  | 8 |
| C | 313 | 2 | 0.02 |  | 0.1 | 6 |  |
 =
=(2)若
 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为
您最近一年使用:0次
【推荐1】研究表明N2O与CO在Fe+的作用下会发生如下反应:① ,②
,② 。其能量变化示意图如下所示。下列说法不正确的是
。其能量变化示意图如下所示。下列说法不正确的是
 ,②
,② 。其能量变化示意图如下所示。下列说法不正确的是
。其能量变化示意图如下所示。下列说法不正确的是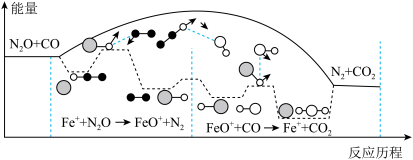
A. 使反应的活化能变小 使反应的活化能变小 |
| B.该催化剂不能有效提高反应物的平衡转化率 |
C. 与CO在不同催化剂表面上转化成 与CO在不同催化剂表面上转化成 与 与 的反应历程完全相同 的反应历程完全相同 |
D.反应①过程中, 中的极性键发生了断裂 中的极性键发生了断裂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】任何有机化合物的分子都是由特定碳骨架构成的,构建碳骨架是合成有机化合物的重要任务。某构建碳骨架的反应历程如图所示,下列关于该反应的说法错误 的是
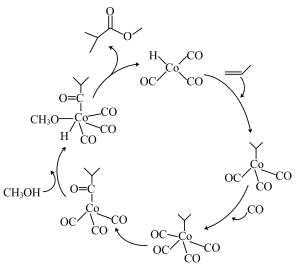

| A.反应过程中Co的成键数目发生改变 |
| B.图中所示物质间的转化有非极性键的断裂和形成 |
| C.CH3OH分子中采用sp3杂化的仅有C原子 |
D.该构建碳骨架的总反应为:CH3CH=CH2+CO+CH3OH (CH3)2CHCOOCH3,原子利用率为100% (CH3)2CHCOOCH3,原子利用率为100% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】燃油汽车尾气含有大量的NO,用活化后的 作催化剂,在有氧条件下氨气将NO还原成
作催化剂,在有氧条件下氨气将NO还原成 的一种反应历程如图所示,下列叙述错误的是
的一种反应历程如图所示,下列叙述错误的是
 作催化剂,在有氧条件下氨气将NO还原成
作催化剂,在有氧条件下氨气将NO还原成 的一种反应历程如图所示,下列叙述错误的是
的一种反应历程如图所示,下列叙述错误的是
A.汽车尾气中含有的 来源是空气中 来源是空气中 和 和 在气缸内反应生成 在气缸内反应生成 |
| B.反应③涉及π键的断裂和形成 |
C.总反应的化学方程式为 |
D. 不能改变反应热,但可以改变反应历程,从而降低活化能 不能改变反应热,但可以改变反应历程,从而降低活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关说法正确的是
| A.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
B. ,升高温度,反应速率 ,升高温度,反应速率 和氢气的平衡转化率均增大 和氢气的平衡转化率均增大 |
| C.升高温度通过降低活化能而加快化学反应速率 |
D.常温下,反应 不能自发进行,则该反应的 不能自发进行,则该反应的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列各表述与示意图一致的是


| A.图①表示25℃时,等物质的量浓度的盐酸和醋酸溶液中加水,溶液的pH随加入水体积的变化 |
B.图②表示2SO2(g)+O2(g) 2SO3(g)△H<0,正、逆反应的平衡常数随温度的变化 2SO3(g)△H<0,正、逆反应的平衡常数随温度的变化 |
| C.图③表示10mL0.01mol•L-1的酸性KMnO4溶液与过量的0.1mol•L-1的H2C2O4溶液混合时,n(Mn2+)随时间的变化 |
| D.图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0,使用和未使用催化剂时,反应过程中的能量变化 |
您最近一年使用:0次
【推荐2】为研究反应 (aq)+2I-(aq)=2
(aq)+2I-(aq)=2 (aq)+I2(aq)的反应进程中的能量变化,在
(aq)+I2(aq)的反应进程中的能量变化,在 和I-的混合溶液中加入Fe3+,过程变化如下:
和I-的混合溶液中加入Fe3+,过程变化如下:
第一步:2Fe3+(aq)+2I-(aq)= I2(aq) + 2Fe2+(aq)
第二步:2Fe2+(aq)+ (aq)=2Fe3+(aq)+2
(aq)=2Fe3+(aq)+2 (aq)
(aq)
下列有关该反应的说法正确的是
 (aq)+2I-(aq)=2
(aq)+2I-(aq)=2 (aq)+I2(aq)的反应进程中的能量变化,在
(aq)+I2(aq)的反应进程中的能量变化,在 和I-的混合溶液中加入Fe3+,过程变化如下:
和I-的混合溶液中加入Fe3+,过程变化如下: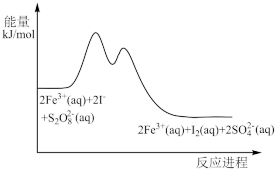
第一步:2Fe3+(aq)+2I-(aq)= I2(aq) + 2Fe2+(aq)
第二步:2Fe2+(aq)+
 (aq)=2Fe3+(aq)+2
(aq)=2Fe3+(aq)+2 (aq)
(aq) 下列有关该反应的说法正确的是
A. (已知其中有1个-O-O-结构)中S元素化合价为+7 (已知其中有1个-O-O-结构)中S元素化合价为+7 |
| B.总反应是吸热反应 |
| C.第一步基元反应是该反应的决速步骤 |
| D.Fe3+改变了总反应的反应历程和焓变 |
您最近一年使用:0次

 。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物质用·标注。下列说法正确的是
。我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物质用·标注。下列说法正确的是

 键形成
键形成

 NaCl(l)+K(g),选取适宜的温度,使K变成蒸气从反应混合物中分离出来
NaCl(l)+K(g),选取适宜的温度,使K变成蒸气从反应混合物中分离出来

