(1)受热分解法。将H2S和CH4混合气导入热解器,反应分两步进行。
反应Ⅰ:2H2S(g)=2H2(g)+S2(g)
 =169.8kJ/mol
=169.8kJ/mol反应Ⅱ:CH4(g)+S2(g)=CS2(g)+2H2(g)
 =63.7kJ/mol
=63.7kJ/mol现将硫化氢和甲烷按照2:1体积比投料,并用N2稀释,常压和不同温度下反应,反应相同时间后,H2、S2和CS2体积分数如图所示。

 =
=②1050℃时,H2的体积分数为
③在950℃~1150℃范围内,其他条件不变,随着温度的升高,S2(g)的体积分数先增大而后减小,其原因可能是
(2)光电催化法。某光电催化法脱除H2S的原理如图所示。
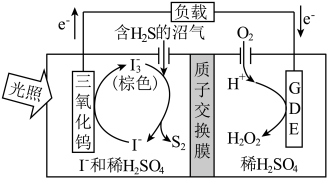
②与受热分解法相比,光电催化法的优点是
(3)催化重整法。Fe2O3可以用作脱除H2S的催化剂,脱除过程如图所示。
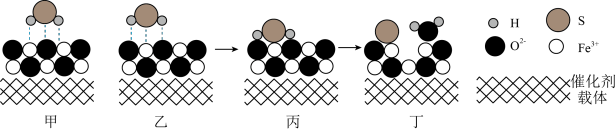
②脱除一段时间后,催化剂的活性降低,原因是
相似题推荐
2H2(g)+CO(g)=CH3OH(g) ΔH=-90.8 kJ·mol-1
2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41.3 kJ·mol-1
请回答下列问题。
(1)由 H2和CO直接制备二甲醚的总反应:3H2(g)+3CO(g)=CH3OCH3(g)+CO2(g)的ΔH=
a.高温高压 b.加入催化剂 c.分离出CO2
d.增加CO的量 e.分离出二甲醚
(2)某温度下反应2CH3OH(g)
 CH3OCH3(g)+H2O(g)的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
②若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH)=
(3)有研究者在催化剂(含Cu—Zn—Al—O和Al2O3)、压强为5.0 MPa的条件下,在相同时间内测得CH3OCH3产率随温度变化的曲线如图甲所示。其中CH3OCH3产率随温度升高而降低的原因可能是
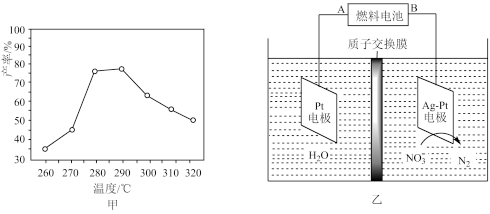
(4)二甲醚直接燃料电池具有启动快、效率高、能量密度高等优点,可用于电化学降解治理水中硝酸盐的污染。电化学降解NO3-的原理如图乙所示。若电解质为酸性,二甲醚直接燃料电池的负极反应式为
(2)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,
则H2CO3
 HCO3-+H+的平衡常数K1=
HCO3-+H+的平衡常数K1=(3)常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液中
c(H2CO3)
 的排放。其原理是在催化剂作用下,用
的排放。其原理是在催化剂作用下,用 等物质将尾气中的
等物质将尾气中的 转化为
转化为 。
。(1)柴油机尾气中的
 是由
是由 和
和 在高温或放电条件下生成的。
在高温或放电条件下生成的。①写出
 的电子式:
的电子式:②高温尾气
 中绝大多数为NO,推测
中绝大多数为NO,推测 为
为(2)在催化剂作用下,
 还原
还原 的化学方程式为
的化学方程式为(3)用传感器检测NO的含量,其工作原理示意图如下:
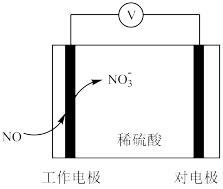
①写出工作电极的电极反应式:
②若用该传感器测定
 的含量,则传感器信号响应方向(即电流方向)相反,从物质性质角度说明原因:
的含量,则传感器信号响应方向(即电流方向)相反,从物质性质角度说明原因:(4)一种研究认为,有氧条件下
 与NO在催化剂表面的催化反应历程如下(催化剂中部分原子未表示):
与NO在催化剂表面的催化反应历程如下(催化剂中部分原子未表示):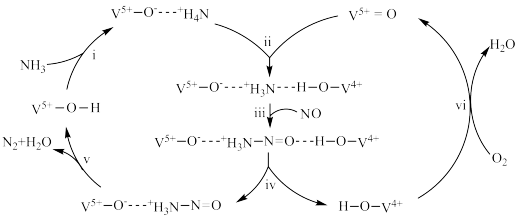
①下列说法正确的是
a.过程涉及了配位键的形成与断裂
b.反应ⅰ~ⅵ均属于氧化还原反应
c.
 与NO反应而不与
与NO反应而不与 直接反应,体现了催化剂的选择性
直接反应,体现了催化剂的选择性②根据上图,写出
 选择性催化还原NO的总反应方程式:
选择性催化还原NO的总反应方程式:(1)可利用甲烷催化还原氮氧化物。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ·mol-1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH=-867kJ·mol-1
则CH4(g)将NO(g)还原为N2(g)的热化学方程式是
(2)汽车内燃机工作时发生的反应为N2(g)+O2(g)
 2NO(g),生成的NO是汽车尾气的主要污染物。T℃时,向5L恒容密闭容器中充入6.5mol N2和7.5mol O2,在5min时反应达到平衡状态,此时容器中NO的物质的量5mol(不考虑后续反应)。则5min内该反应的平均速率v(NO)=
2NO(g),生成的NO是汽车尾气的主要污染物。T℃时,向5L恒容密闭容器中充入6.5mol N2和7.5mol O2,在5min时反应达到平衡状态,此时容器中NO的物质的量5mol(不考虑后续反应)。则5min内该反应的平均速率v(NO)=(3)汽车尾气中也含有CO,已知CO能发生可逆反应:CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH=-41kJ·mol-1。
CO2(g)+H2(g) ΔH=-41kJ·mol-1。①向某容器中充入1.0mol H2O(g)和1.0mol CO(g),在一定条件下发生上述反应。混合气体中CO的物质的量(mol)与时间关系如下表所示:
| 0 | 5min | 10min | 15min | 20min | 25min | |
| Ⅰ(800℃) | 1.0 | 0.80 | 0.70 | 0.65 | 0.50 | 0.50 |
| Ⅱ(800℃) | 1.0 | 0.70 | 0.60 | 0.50 | 0.50 | 0.50 |
相对实验Ⅰ,实验Ⅱ改变的条件可能是
②若开始时向绝热容器中投入一定量二氧化碳、氢气,在一定条件下发生上述可逆反应。下列图象正确且能说明可逆反应已达到平衡状态的是
A.
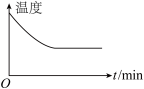 B.
B. C.
C.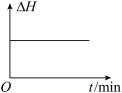 D.
D.
(4)利用ClO2氧化氮氧化物反应过程如下:NO
 NO2
NO2 N2
N2反应Ⅰ的产物中还有两种强酸生成,其中硝酸与NO2的物质的量相等,则其化学方程式是
Ⅰ.蒽醌法的反应过程如下。
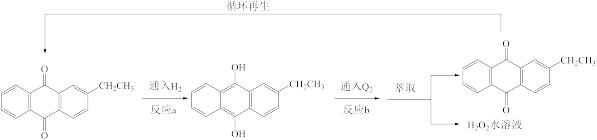
(1)已知:2H2(g)+O2(g)=2H2O(l) ΔH1 = -572 kJ·mol-1
2H2O2(l) = 2H2O(l) + O2(g) ΔH2 = -196 kJ·mol-1
蒽醌法生产H2O2总反应的热化学方程式是
(2)发生反应b时,消耗
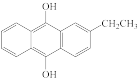 与O2的物质的量之比是
与O2的物质的量之比是(3)测定H2O2含量:取所得H2O2水溶液a mL,用c mol·L-1 KMnO4酸性溶液滴定,消耗KMnO4酸性溶液v mL。已知:MnO
 的还原产物是Mn2+。
的还原产物是Mn2+。① KMnO4酸性溶液与H2O2反应的离子方程式是
② 所得H2O2水溶液中H2O2的物质的量浓度是
Ⅱ.氢氧直接合成法的反应过程如图所示。
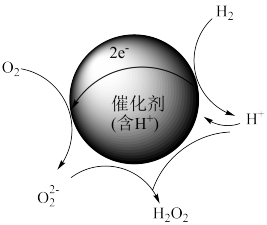
(4)用同位素示踪法研究催化剂中H+的作用:用D2(2H2)代替H2进行实验。催化剂中氢离子参与反应的证据是生成的过氧化氢中有
(5)H2转化率和H2O2选择性随反应时间的变化如图。已知:H2O2选择性是指H2O2在所有生成物中的占比。
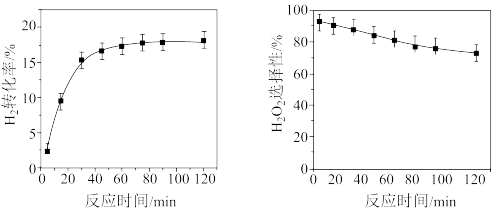
用化学方程式解释H2O2选择性逐渐下降的可能原因:
(1)如图:1 mol CH4完全燃烧生成气态水的能最变化和1 mol S(g)燃烧的能量交化。

已知CH4还原SO2发生的反应为:CH4(g)+2SO2(g)
 2H2O(g)+2S(g)+CO2(g),则该反应的△H=
2H2O(g)+2S(g)+CO2(g),则该反应的△H=(2)焦炭还原二氧化硫的化学方程式:2C(s)+2SO2(g)
 S2(g)+2CO2(g)。一定压强下,向1 L密闭容器中充入足量的焦炭和l mol SO2发生反应,测得SO2的生成速率与S2(g)的生成速率随温度变化关系如图所示:
S2(g)+2CO2(g)。一定压强下,向1 L密闭容器中充入足量的焦炭和l mol SO2发生反应,测得SO2的生成速率与S2(g)的生成速率随温度变化关系如图所示: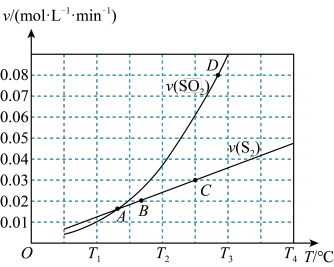
①A、B、C、D四点对应的状态中,达到平衡状态的有
②该反应的ΔH
③下列能够增大SO2平衡转化率的是
A.降低温度 B.增加固态C的量 C.增大容器体积 D.添加高效催化剂
(3)当吸收液失去吸收能力后通入O2可得到NH4HSO4溶液,用如图所示装置电解所得NH4HSO4溶液可制得强氧化剂(NH4)2S2O8。请写出电解NH4HSO4,溶液的化学方程式

(4)用氨水吸收SO2。将含SO2的烟气通入该氨水中,当溶液显中性时,溶液中的
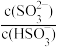 =
= 10-2,Ka2(H2SO3)=6.0
10-2,Ka2(H2SO3)=6.0 10-8)
10-8)
 2Ni(OH)2+ Cd(OH)2,制造密封式镍镉电池的部分工艺如下:
2Ni(OH)2+ Cd(OH)2,制造密封式镍镉电池的部分工艺如下:I.Ni(OH)2的制备
以硫酸镍(NiSO4)为原料制备Ni(OH)2的主要过程如下图所示。制备过程中,通过降低镍离子的浓度可以降低Ni(OH)2沉淀速率,从而避免沉淀团聚,提升电池性能。

已知:Ni2++6NH3·H2O=[Ni(NH3)6]2++6H2O
(1)操作a是
(2)制备过程中,需先加氨水,再加过量NaOH,请分析:
①先加氨水的目的是
②用化学平衡移动原理分析加入NaOH需过量的原因是
(3)用无水乙醇代替水洗涤滤渣的优点是
II.镍镉电池的组装
主要步骤:①将Ni(OH)2和Cd(OH)2固定,中间以隔膜隔开(如下图所示);
②将多组上述结构串联;③向电池中注入KOH溶液;④密封。
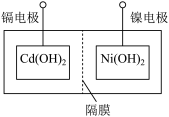
(4)下列对镍镉电池组装和使用的分析正确的是
a.密封镍镉电池可以避免KOH变质
b.镍电极为电池的负极,镉电极为电池的正极
c.电池组装后,应先充电,再使用
(5)该电池充电时,阳极反应式为
(6)已知:①隔膜可以透过阴离子和分子;②O2可以与Cd发生反应生成Cd(OH)2制造电池时,在镉电极加入过量的Cd(OH)2,则Cd(OH)2不会被消耗完,对电池进行过度充电保护,此时:OH-从
【推荐2】2019年诺贝尔化学奖授予美国固体物理学家约翰·巴尼斯特·古迪纳夫(JohnBGoodenough),英国化学家斯坦利·威廷汉(StanleyWhittingham)和日本化学家吉野彰(AkiraYoshino),以表彰他们发明锂离子电池方面做出的贡献。
I.某废旧锂离子电池的正极材料主要含有LiCoO2及少量Al、Fe等,处理该废料的一种工艺流程如图所示(已知:Ksp(Li2CO3)=1.6×10-3,LiCoO2难溶于水,具有强氧化性):
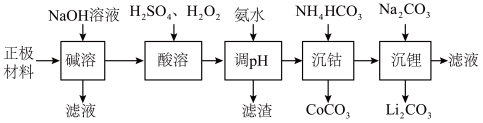
①在碱溶的时候,有哪些措施可以提高反应速率?
②图中用氨水调节溶液pH,得到的固体应为
③该流程中分离出的Li2CO3可以和NH4H2PO4及(CH3COO)2Fe制备正极材料LiFePO4,已知NH3·H2O的电离常数Kb=2×10-5mol/L,H3PO4的各级电离常数为Ka1=1×10-2mol/L、Ka2=6.2×10-8mol/L、Ka3=2.2×10-13mol/L,则常温下NH4H2PO4溶液中c(NH )
) )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。
Ⅱ.已知某锂离子电池的总反应为LiCoO2+xC6 Li1-xCoO2+xLiC6,一种太阳能储能电池的工作原理如图所示,回答下列问题:
Li1-xCoO2+xLiC6,一种太阳能储能电池的工作原理如图所示,回答下列问题:
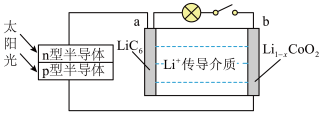
①该锂离子电池充电时,Li+的移动方向
②该锂离子电池放电时,a极上的电极反应式为
Ⅲ.用锂电池电解物质的量均为0.1mol的CuCl2和H2SO4溶于水制成的100mL混合溶液,用石墨做电极电解混合溶液,并收集两电极所产生的气体,通电一段时间后在两极收集到的气体在相同条件下体积相同,则:
①电路中转移的电子数为
②电解后溶液中剩余的溶质的浓度为
a.<1mol/L b.=1mol/L c.>1mol/L
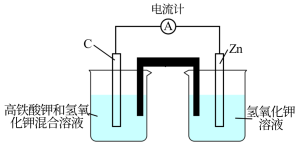
(1)该电池放电时正极的电极反应式为
(2)盐桥中盛有饱和KC1溶液,此盐桥中氯离子向
(3)下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有
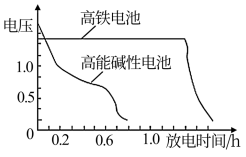
Ⅱ.工业上湿法制备K2FeO4的工艺流程如图。
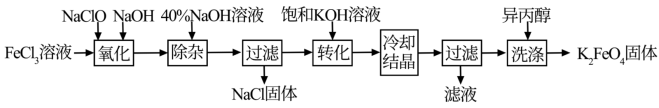
(4)完成“氧化”过程中反应的化学方程式:
(5)加入饱和KOH溶液的目的是
(6)已知25℃时Ksp[Fe(OH)3]=4.0×10-38,此温度下若在实验室中配制5mol/L l00mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入



