常温下,将带有氧化膜的铝条投入盛有一定量稀盐酸的敞口容器中,反应过程中产生氢气速率与时间关系如图所示。下列说法不正确的是


A.反应过程中生成 体积一直增加 体积一直增加 |
B. 速率增大,与反应放热和氧化膜减少有关 速率增大,与反应放热和氧化膜减少有关 |
C. 速率减小,只与 速率减小,只与 减小有关 减小有关 |
D.反应过程中的速率变化是温度、 、Al与盐酸接触面积共同作用的结果 、Al与盐酸接触面积共同作用的结果 |
更新时间:2024-01-11 20:54:52
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】某酮和甲胺的反应机理及能量图像如图所示:
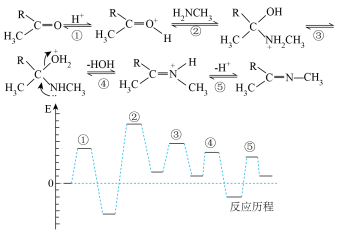
A.该历程中 为催化剂,故 为催化剂,故 浓度越大,反应速率越快 浓度越大,反应速率越快 |
| B.该历程中发生了加成反应和消去反应 |
| C.反应过程中有极性键的断裂和生成 |
| D.该历程中制约反应速率的反应为反应② |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】用一定质量的锌粒与某浓度的稀硫酸反应制取H2,若要增大反应速率,则下列选项中采取的措施全部正确的是
①滴入几滴CuSO4溶液 ②将锌粒改为锌粉 ③改加浓硫酸 ④适当降低温度
①滴入几滴CuSO4溶液 ②将锌粒改为锌粉 ③改加浓硫酸 ④适当降低温度
| A.①③ | B.①② | C.②③ | D.①④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一定条件下,反应H2(g)+Br2(g) 2HBr(g)的速率方程为v=kcα(H2)·cβ(Br2)·cγ(HBr),某温度下,该反应在不同浓度下的反应速率如下:
2HBr(g)的速率方程为v=kcα(H2)·cβ(Br2)·cγ(HBr),某温度下,该反应在不同浓度下的反应速率如下:
根据表中的测定结果,下列结论错误的是
 2HBr(g)的速率方程为v=kcα(H2)·cβ(Br2)·cγ(HBr),某温度下,该反应在不同浓度下的反应速率如下:
2HBr(g)的速率方程为v=kcα(H2)·cβ(Br2)·cγ(HBr),某温度下,该反应在不同浓度下的反应速率如下:| c(H2)/mol·L−1 | c(Br2)/mol·L−1 | c(HBr)/mol·L−1 | 反应速率 |
| 0.1 | 0.1 | 2 | v |
| 0.1 | 0.4 | 2 | 8v |
| 0.2 | 0.4 | 2 | 16v |
| 0.4 | 0.1 | 4 | 2v |
| 0.2 | 0.1 | c | 4v |
| A.α的值为1 |
| B.表中c的值为2 |
| C.反应体系的三种物质中,Br2(g)的浓度对反应速率影响最大 |
| D.在反应体系中保持其他物质浓度不变,增大HBr(g)浓度,会使反应速率降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列装置,可以达到相应实验目的的是
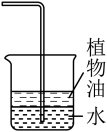 | 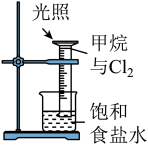 | 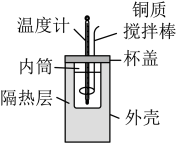 | 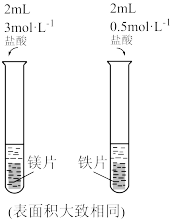 |
| A.吸收氨气尾气 | B.甲烷与氯气的取代反应 | C.中和反应反应热的测定 | D.探究浓度对化学反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验操作、现象及所得到的结论均正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向A、B 2支试管中先加入4mL0.1mol·L-1KMnO4酸性溶液,再分别加入2mL0.01mol·L-1H2C2O4溶液和2mL0.02mol·L-1H2C2O4溶液,B试管先褪色 | 反应物浓度越大,化学反应速率越快 |
| B | 室温下,将BaSO4投入饱和Na2CO3溶液中充分反应,向过滤后所得固体中加入足量盐酸,固体部分溶解有无色无味气体产生 | Ksp(BaSO4)>Ksp(BaCO3) |
| C | 向10 mL 0.2 mol·L-1AgNO3溶液中滴入2滴0.1 mol·L-1NaCl溶液,产生白色沉淀后,再滴加2滴0.1 mol·L-1Na2S溶液,有黑色沉淀生成 | Ksp(AgCl)>Ksp(Ag2S) |
| D | 在CuCl2溶液中存在如下平衡:[Cu(H2O)4]2+(蓝色)+4Cl-⇌[CuCl4]2-(黄色)+4H2O,加热,该溶液由蓝色变为黄绿色 | 该反应为吸热反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
名校
【推荐1】某工业流程中,进入反应塔的混合气体中NO和O2的物质的量分数分别为0.10和0.06,发生化学反应 ,在其他条件相同时,测得实验数据如下表:
,在其他条件相同时,测得实验数据如下表:
根据表中数据,下列说法正确的是
 ,在其他条件相同时,测得实验数据如下表:
,在其他条件相同时,测得实验数据如下表:| 压强/(×105Pa) | 温度/℃ | NO达到所列转化率需要时间/s | ||
| 50% | 90% | 98% | ||
| 1.0 | 30 | 12 | 250 | 2830 |
| 90 | 25 | 510 | 5760 | |
| 8.0 | 30 | 0.2 | 3.9 | 36 |
| 90 | 0.6 | 7.9 | 74 | |
根据表中数据,下列说法正确的是
| A.升高温度,反应速率加快 |
| B.增大压强,反应速率变慢 |
| C.在1.0×105Pa、90℃条件下,当转化率为98%时的反应已达到平衡 |
| D.若进入反应塔的混合气体为amol,反应速率以v=Δn/Δt表示,则在8.0×105Pa、30℃条件下转化率从50%增至90%时段NO的反应速率为4a/370mol/s |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】催化制氢是目前大规模制取氢气的方法之一: △H=-41.2 kJ/mol研究表明,此反应的速率方程为:
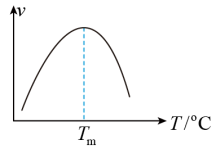
△H=-41.2 kJ/mol研究表明,此反应的速率方程为: 式中,x(CO)、x(H2O)、x(CO2)、x(H2)分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。下列有关说法正确的是
式中,x(CO)、x(H2O)、x(CO2)、x(H2)分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。下列有关说法正确的是
 △H=-41.2 kJ/mol研究表明,此反应的速率方程为:
△H=-41.2 kJ/mol研究表明,此反应的速率方程为: 式中,x(CO)、x(H2O)、x(CO2)、x(H2)分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。下列有关说法正确的是
式中,x(CO)、x(H2O)、x(CO2)、x(H2)分别表示相应的物质的量分数,Kp为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。下列有关说法正确的是
| A.温度越低,Kp越小 |
| B.温度升高,反应速率增大 |
| C.此反应速率只受温度因素影响 |
| D.T>Tm时,Kp减小对反应速率的影响大于k增大的影响 |
您最近一年使用:0次

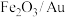 可用作反应
可用作反应 浓度能加快反应速率
浓度能加快反应速率 溶液分解速率影响的是
溶液分解速率影响的是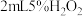 溶液,向其中一支试管中加入少量
溶液,向其中一支试管中加入少量 ,与另一支对比
,与另一支对比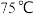 热水中,与另一支对比
热水中,与另一支对比
 溶液,均加入等量的
溶液,均加入等量的

