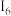磷酸铁锂(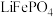 )电极材料主要用于各种锂离子电池。回答下列问题
)电极材料主要用于各种锂离子电池。回答下列问题
(1)Fe位于元素周期表中第___________ 周期第___________ 族,其外围电子排布式为___________ 。
(2)离子半径: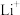
___________  ;第一电离能:Li
;第一电离能:Li___________ Be;电负性:O___________ P。(填“>”“<”或“=”)
(3)下列Li的轨道表示式表示的状态中,能量最低和最高的分别为___________ 、___________ (填标号)。
A. B.
B.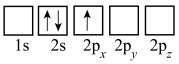
C.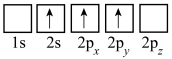 D.
D.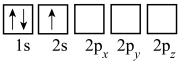
(4)基态P中未成对的电子数为___________ ,其原子核外电子占据的最高能级的电子云轮廓为___________ 形。
(5)Mn与Fe两元素的部分电离能数据如下,由表中两元素的 和
和 可知,气态
可知,气态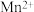 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子更难,对此,你的解释是
再失去一个电子更难,对此,你的解释是___________ 。
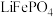 )电极材料主要用于各种锂离子电池。回答下列问题
)电极材料主要用于各种锂离子电池。回答下列问题(1)Fe位于元素周期表中第
(2)离子半径:
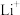
 ;第一电离能:Li
;第一电离能:Li(3)下列Li的轨道表示式表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(4)基态P中未成对的电子数为
(5)Mn与Fe两元素的部分电离能数据如下,由表中两元素的
 和
和 可知,气态
可知,气态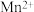 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子更难,对此,你的解释是
再失去一个电子更难,对此,你的解释是| 元素 | Mn | Fe | |
| 电离能(kJ/mol) |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 |
更新时间:2024-02-11 19:42:31
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】三磷酸腺苷(ATP)和活性氧类(如H2O2和 )可在细胞代谢过程中产生。
)可在细胞代谢过程中产生。
(1)ATP的分子式为C10H16N5O13P3,其中电负性最大的元素基态原子的核外电子排布式是________ ,基态N原子的电子排布图为________ 。
(2)对H2O2分子结构的研究,H2O2分子的电子式为:________ ,其中氧原子的杂化轨道类型为:________ ;为确定其空间结构不是直线形分子,应测定H2O2分子中________ (填字母序号)
a. 键长 b.
键长 b. 键能 c.
键能 c. 键角
键角
(3)H2O2是一种绿色氧化剂有广泛应用,写出Cu、稀硫酸与H2O2反应制备硫酸铜的离子方程式:_________ 。
(4)O3分子的空间结构为V形,O3分子是________ 分子(填“极性”或“非极性”)。
 )可在细胞代谢过程中产生。
)可在细胞代谢过程中产生。(1)ATP的分子式为C10H16N5O13P3,其中电负性最大的元素基态原子的核外电子排布式是
(2)对H2O2分子结构的研究,H2O2分子的电子式为:
a.
 键长 b.
键长 b. 键能 c.
键能 c. 键角
键角(3)H2O2是一种绿色氧化剂有广泛应用,写出Cu、稀硫酸与H2O2反应制备硫酸铜的离子方程式:
(4)O3分子的空间结构为V形,O3分子是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请回答下列有关问题。
(1) 元素按周期表分区属于
元素按周期表分区属于________ 区元素
(2)地壳中含量最多的三种元素 、
、 、
、 中,电负性最大的是
中,电负性最大的是______ 。
(3)钠在火焰上灼烧产生的黄光是一种_______ (填字母)
A.吸收光谱 B.发射光谱
(4) 分子的空间构型为
分子的空间构型为_______ 。
(5)钛被称为继铁、铝之后的第三金属,基态钛原子价电子层的电子排布图是______ 。
(6)基态 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为________ 。
(7) 分子中所有原子均满足8电子构型,
分子中所有原子均满足8电子构型, 分子中
分子中 键和
键和 键的个数比为
键的个数比为_______ 。
(1)
 元素按周期表分区属于
元素按周期表分区属于(2)地壳中含量最多的三种元素
 、
、 、
、 中,电负性最大的是
中,电负性最大的是(3)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(4)
 分子的空间构型为
分子的空间构型为(5)钛被称为继铁、铝之后的第三金属,基态钛原子价电子层的电子排布图是
(6)基态
 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为(7)
 分子中所有原子均满足8电子构型,
分子中所有原子均满足8电子构型, 分子中
分子中 键和
键和 键的个数比为
键的个数比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)盐碱地(含较多 、NaCl)不利于植物生长,盐碱地呈碱性的原因:
、NaCl)不利于植物生长,盐碱地呈碱性的原因:___________ (用离子方程式表示)。
(2)D元素的正三价离子的3d轨道为半充满,其基态原子的价层电子排布式为___________ 。
(3)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的简化电子排布式为___________ ,在元素周期表中的位置是___________ 。
(4) 是离子化合物,各原子均满足8电子稳定结构,
是离子化合物,各原子均满足8电子稳定结构, 的电子式是
的电子式是___________ 。
(5)Xe是第五周期的稀有气体元素,与F形成的 室温下易升华。下列对
室温下易升华。下列对 中心原子杂化方式推断合理的是
中心原子杂化方式推断合理的是___________ (填字母)。
(6)为测定某 消毒剂样品中含氯量,用
消毒剂样品中含氯量,用 溶液滴定该样品溶液,操作如下:
溶液滴定该样品溶液,操作如下:
a.取样:取20.00 mL样品溶液置于锥形瓶,加入稀硫酸酸化,发生反应: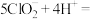
 (
( 极易溶于水);
极易溶于水);
b.氧化:加入足量碘化钾溶液,振荡充分反应;
c.滴定:加入淀粉作指示剂,在锥形瓶下垫一张白纸,用0.1000 mol/L 标准溶液滴定碘单质(已知:
标准溶液滴定碘单质(已知: );
);
d.重复上述操作三次。
滴定终点现象为:加入最后半滴 溶液后,溶液
溶液后,溶液___________ ,即到终点。
测得的实验数据如下表:
由以上数据计算该样品溶液的含氯量(以 计)
计)___________ g/L(保留三位有效数字)。滴定时,有一组数据出现了明显异常,所测含氯量偏大,原因可能有___________ (填字母序号)。
A.取样时用25.00 mL的滴定管液面在5.00 mL处放出所有溶液
B.滴定终点读数时仰视刻度线
C.达终点时滴定管尖嘴有标准液悬挂
D.盛装待测液的锥形瓶未润洗
E.摇动锥形瓶时有液体溅出
(1)盐碱地(含较多
 、NaCl)不利于植物生长,盐碱地呈碱性的原因:
、NaCl)不利于植物生长,盐碱地呈碱性的原因:(2)D元素的正三价离子的3d轨道为半充满,其基态原子的价层电子排布式为
(3)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的简化电子排布式为
(4)
 是离子化合物,各原子均满足8电子稳定结构,
是离子化合物,各原子均满足8电子稳定结构, 的电子式是
的电子式是(5)Xe是第五周期的稀有气体元素,与F形成的
 室温下易升华。下列对
室温下易升华。下列对 中心原子杂化方式推断合理的是
中心原子杂化方式推断合理的是| A.sp | B. | C. | D. |
 消毒剂样品中含氯量,用
消毒剂样品中含氯量,用 溶液滴定该样品溶液,操作如下:
溶液滴定该样品溶液,操作如下:a.取样:取20.00 mL样品溶液置于锥形瓶,加入稀硫酸酸化,发生反应:
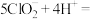
 (
( 极易溶于水);
极易溶于水);b.氧化:加入足量碘化钾溶液,振荡充分反应;
c.滴定:加入淀粉作指示剂,在锥形瓶下垫一张白纸,用0.1000 mol/L
 标准溶液滴定碘单质(已知:
标准溶液滴定碘单质(已知: );
);d.重复上述操作三次。
滴定终点现象为:加入最后半滴
 溶液后,溶液
溶液后,溶液测得的实验数据如下表:
| 实验序号 | 待测液体积(mL) |  标准溶液 标准溶液 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 20.00 | 0.06 | 20.60 |
| 2 | 20.00 | 6.00 | 25.95 |
| 3 | 20.00 | 1.40 | 23.20 |
| 4 | 20.00 | 1.00 | 21.05 |
 计)
计)A.取样时用25.00 mL的滴定管液面在5.00 mL处放出所有溶液
B.滴定终点读数时仰视刻度线
C.达终点时滴定管尖嘴有标准液悬挂
D.盛装待测液的锥形瓶未润洗
E.摇动锥形瓶时有液体溅出
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据元素周期表中完整周期元素的性质,完成下列空格。
(1)在第三周期中,第一电离能最小的元素符号是________ ,其原子的结构示意图为__________ ,第一电离能最大的元素符号是________ ,其价电子排布式为___________________________ 。
(2)在元素周期表中,电负性最大的元素名称是________ ,其价电子排布图为______________
(3)第四周期元素中未成对电子数最多的元素符号是________ ,其原子的简化电子排布式为__________ ,有_____ 个未成对电子,有_____ 个能级,能量最高的能级符号为_______ 。
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是_________ ,原子中所有电子占有________ 个轨道,核外共有________ 个不同运动状态的电子。
(1)在第三周期中,第一电离能最小的元素符号是
(2)在元素周期表中,电负性最大的元素名称是
(3)第四周期元素中未成对电子数最多的元素符号是
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)自然界中存在的碘的稳定性核素是碘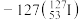 。某次核电站事故释放出的放射性物质中含有人工放射性核素碘
。某次核电站事故释放出的放射性物质中含有人工放射性核素碘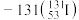 。碘
。碘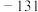 一旦被人体吸入,可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是
一旦被人体吸入,可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是______ (填序号)。
A. 和
和 原子核外的价电子排布不同
原子核外的价电子排布不同
B. 和
和 互为同位素
互为同位素
C. 原子的核外电子排布式中只有1个能级上未充满电子
原子的核外电子排布式中只有1个能级上未充满电子
D. 的中子数与质子数之差为74
的中子数与质子数之差为74
(2)有四种短周期元素,它们的结构、性质等信息如下表所示:
① 元素原子的核外电子排布式为
元素原子的核外电子排布式为______ 。
②离子半径:
______ (填“ ”或“
”或“ ”)
”) 。
。
③ 元素原子的核外电子排布图为
元素原子的核外电子排布图为______ ,其原子核外有______ 个未成对电子,能量最高的电子为______ 轨道上的电子,该轨道呈______ 形。
④写出 、
、 两元素的最高价氧化物对应的水化物反应的离子方程式:
两元素的最高价氧化物对应的水化物反应的离子方程式:______ 。
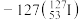 。某次核电站事故释放出的放射性物质中含有人工放射性核素碘
。某次核电站事故释放出的放射性物质中含有人工放射性核素碘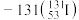 。碘
。碘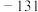 一旦被人体吸入,可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是
一旦被人体吸入,可能会引发甲状腺疾病。下列关于这两种核素的说法正确的是A.
 和
和 原子核外的价电子排布不同
原子核外的价电子排布不同B.
 和
和 互为同位素
互为同位素C.
 原子的核外电子排布式中只有1个能级上未充满电子
原子的核外电子排布式中只有1个能级上未充满电子D.
 的中子数与质子数之差为74
的中子数与质子数之差为74(2)有四种短周期元素,它们的结构、性质等信息如下表所示:
| 元素 | 结构、性质等信息 |
| A | 是短周期元素中(除稀有气体外)第一电离能最小的元素,该元素单质的某种合金是原子反应堆的导热剂 |
| B | 与A同周期,其最高价氧化物对应的水化物呈两性 |
| C | 其气态氢化物极易溶于水,液态时可用作制冷剂 |
| D | 原子核外电子共有17种不同的运动状态 |
①
 元素原子的核外电子排布式为
元素原子的核外电子排布式为②离子半径:

 ”或“
”或“ ”)
”) 。
。③
 元素原子的核外电子排布图为
元素原子的核外电子排布图为④写出
 、
、 两元素的最高价氧化物对应的水化物反应的离子方程式:
两元素的最高价氧化物对应的水化物反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】完成下列问题
(1)元素Mn与Fe的部分电离能数据如下表所示:
根据表中数据可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此,你的解释是
再失去1个电子难,对此,你的解释是___________ 。
(2)已知18g葡萄糖固体在人体组织中被O2完全氧化为CO2气体和液态水,能产生280kJ热量。写出该反应的热化学方程式___________ 。
(1)元素Mn与Fe的部分电离能数据如下表所示:
| 元素 | Mn | Fe | |
| 电离能/(kJ/mol) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此,你的解释是
再失去1个电子难,对此,你的解释是(2)已知18g葡萄糖固体在人体组织中被O2完全氧化为CO2气体和液态水,能产生280kJ热量。写出该反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)下表数据是Na、Mg、Al三种元素的原子逐级失去电子的电离能( ):
):
根据表中数据判断,元素②是__________ 。
(2)Na、Mg、Al的化学活动性依次减弱,试从化学键角度解释其原因__________ 。
(3)基态Al原子转化为下列激发态时,吸收能量最少的是__________(填标号)。
(4)AlCl,为l共价化合物,蒸汽状态下以双聚分子 形式存在,所有原子均满足8电子稳定结构,其结构式为
形式存在,所有原子均满足8电子稳定结构,其结构式为__________ (用“→”表示出分子中的配位键),其中Al的配位数为__________ 。
(5)元素硼(B)和镓(Ga)和铝同族,分别与铝处于相邻周期。已知硼酸(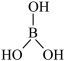 )为一元弱酸,与强碱反应的离子方程式为
)为一元弱酸,与强碱反应的离子方程式为 。在
。在 和
和 中B原子的杂化轨道类型分别为
中B原子的杂化轨道类型分别为__________ 、__________ 。
(6)基态Ga原子的核外电子排布式为[Ar]__________ 。
(7)根据元素周期律分析,
__________ (填序号)。
①只能与强酸反应 ②只能与强碱反应 ③既能与强酸反应,又能与强碱反应
(1)下表数据是Na、Mg、Al三种元素的原子逐级失去电子的电离能(
 ):
):
|
|
|
|
|
| …… | |
元素① | 496 | 4562 | 6912 | 9543 | 13353 | 16610 | …… |
元素② | 577 | 1817 | 2745 | 11575 | 14830 | 18376 | …… |
元素③ | 738 | 1451 | 7733 | 10540 | 13630 | 17995 | …… |
(2)Na、Mg、Al的化学活动性依次减弱,试从化学键角度解释其原因
(3)基态Al原子转化为下列激发态时,吸收能量最少的是__________(填标号)。
A.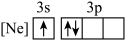 | B.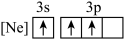 |
C.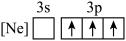 | D.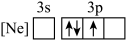 |
(4)AlCl,为l共价化合物,蒸汽状态下以双聚分子
 形式存在,所有原子均满足8电子稳定结构,其结构式为
形式存在,所有原子均满足8电子稳定结构,其结构式为(5)元素硼(B)和镓(Ga)和铝同族,分别与铝处于相邻周期。已知硼酸(
 )为一元弱酸,与强碱反应的离子方程式为
)为一元弱酸,与强碱反应的离子方程式为 。在
。在 和
和 中B原子的杂化轨道类型分别为
中B原子的杂化轨道类型分别为(6)基态Ga原子的核外电子排布式为[Ar]
(7)根据元素周期律分析,

①只能与强酸反应 ②只能与强碱反应 ③既能与强酸反应,又能与强碱反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】镧系为元素周期表中IIIB族、原子序数为57~71的元素。
1.镝(Dy)的基态原子电子排布式为[Xe]4f106s2。镝原子价电子的轨道表示式为:_____ 。
2.高温超导材料镧钡铜氧化物中含有Cu3+,基态时Cu3+的电子排布式为_____ 。
3.观察下面四种镧系元素的电离能数据,判断最有可能显示+3价的元素是______ 填元素名称)。
1.镝(Dy)的基态原子电子排布式为[Xe]4f106s2。镝原子价电子的轨道表示式为:
2.高温超导材料镧钡铜氧化物中含有Cu3+,基态时Cu3+的电子排布式为
3.观察下面四种镧系元素的电离能数据,判断最有可能显示+3价的元素是
| 几种镧系元素的电离能(单位:kJ·mol−l) | ||||
| 元素 | I1 | I2 | I3 | I4 |
| Yb(镱) | 604 | 1217 | 4494 | 5014 |
| Lu(镥) | 532 | 1390 | 4111 | 4987 |
| La(镧) | 538 | 1067 | 1850 | 5419 |
| Ce(铈) | 527 | 1047 | 1949 | 3547 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题。
(1)C、Si、N元素的电负性由大到小的顺序是___________________________ 。C60和金刚石都是碳的同素异形体,金刚石熔点高于C60熔点,原因是__________________________________________________________________________ 。
(2)A、B均为短周期金属元素。依据下表数据和已学知识,
写出B原子的电子排布式:___________________________ 。
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O) 6]2+显粉红色。据此判断,[Mn(H2O) 6]]2+_______ (填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、络合物Fe(CO)5等。
①已知COCl2分子的结构式为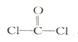 ,则 COCl2分子内含
,则 COCl2分子内含_______ (填标号)。
A.4个 键
键
B.2个 键、2个
键、2个 键
键
C.2个 键、1个
键、1个 键
键
D.3个 键、1个
键、1个 键
键
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是___________ 。
(1)C、Si、N元素的电负性由大到小的顺序是
(2)A、B均为短周期金属元素。依据下表数据和已学知识,
| 电离能/KJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
写出B原子的电子排布式:
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O) 6]2+显粉红色。据此判断,[Mn(H2O) 6]]2+
(4)利用CO可以合成化工原料COCl2、络合物Fe(CO)5等。
①已知COCl2分子的结构式为
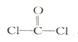 ,则 COCl2分子内含
,则 COCl2分子内含A.4个
 键
键B.2个
 键、2个
键、2个 键
键C.2个
 键、1个
键、1个 键
键D.3个
 键、1个
键、1个 键
键②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】黑磷是磷的一种稳定的同素异形体,黑磷具有正交晶系的晶体结构(图A),晶胞参数a=3.310A,b=4.380A,c=10.500A。黑磷烯是二维的单层黑磷(图B),黑磷烯与石墨烯结构相似,P的配位数为3。与石墨烯相比,黑磷烯具有半导体性质,更适合于制作电子器件。已知黑磷结构中只有一种等效的三配位P,所有P原子的成键环境一样,图A中编号为①的P原子的晶胞内坐标为(0.50,0.090,0.598)。请回答下列问题:
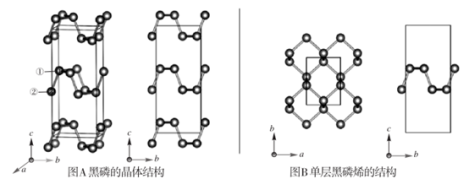
(1)写出P原子的价电子排布:___ 。
(2)P和F的电负性大小顺序是X(P)___ X(F)。(填“<”“=”或“>”)P和F形成的分子PF3和PF5,它们的几何构型分别为__ 、__ 。
(3)①黑磷中P原子杂化类型是__ 。黑磷中不存在__ (选填字母序号)。
A.共价键 B.σ键 C.π键 D.范德华力
②红磷、白磷与黑磷熔点从高到低的顺序为__ ,原因是__ 。
(4)图A中编号为②的P原子的晶胞内坐标为__ ,黑磷的晶胞中含有__ 个P原子。

(1)写出P原子的价电子排布:
(2)P和F的电负性大小顺序是X(P)
(3)①黑磷中P原子杂化类型是
A.共价键 B.σ键 C.π键 D.范德华力
②红磷、白磷与黑磷熔点从高到低的顺序为
(4)图A中编号为②的P原子的晶胞内坐标为
您最近一年使用:0次
【推荐3】深入研究物质的微观结构,有利于理解物质变化的本质。请回答下列问题:
(1)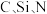 的电负性由大到小的顺序是
的电负性由大到小的顺序是___________ 。
(2)C、N、O、F的第一电离能由大到小的顺序是___________ 。
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为 或
或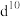 排布时,无颜色;为
排布时,无颜色;为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,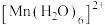
_________ 颜色(填“无”或“有”)。
(4)L的原子核外电子占有9个轨道,而且有一个未成对电子,L是___________ (填元素符号)。
(5) 能与
能与 形成正四面体形的配合物
形成正四面体形的配合物 ,
,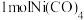 中含有
中含有__________  键。
键。
(1)
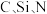 的电负性由大到小的顺序是
的电负性由大到小的顺序是(2)C、N、O、F的第一电离能由大到小的顺序是
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为
 或
或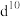 排布时,无颜色;为
排布时,无颜色;为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,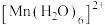
(4)L的原子核外电子占有9个轨道,而且有一个未成对电子,L是
(5)
 能与
能与 形成正四面体形的配合物
形成正四面体形的配合物 ,
,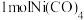 中含有
中含有 键。
键。
您最近一年使用:0次