石油天然气开采和炼制过程中会产生大量含硫废水(其中S元素的主要化合价是-2价),对设备、环境等造成严重危害。
已知: 有剧毒;常温下溶解度为
有剧毒;常温下溶解度为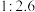 (体积)。
(体积)。
(1) 、
、 、
、 在水溶液中的物质的量分数随pH的分布曲线如图。
在水溶液中的物质的量分数随pH的分布曲线如图。

①当 时,含硫废水中最主要的含硫(-2价)微粒是
时,含硫废水中最主要的含硫(-2价)微粒是_________ 。
②通过图中数据可估算得 的
的______ (填“ ”或“
”或“ ”)。
”)。
(2)沉淀法处理含硫废水:
向 的含硫废水中加入适量
的含硫废水中加入适量 的溶液,产生黑色沉淀且溶液的pH降低。用化学平衡移动的原理解释溶液的pH降低的原因:
的溶液,产生黑色沉淀且溶液的pH降低。用化学平衡移动的原理解释溶液的pH降低的原因:_______ 。
(3)氧化还原法处理含硫废水:
向 的含硫废水中加入一定浓度的
的含硫废水中加入一定浓度的 溶液,加酸将溶液调为
溶液,加酸将溶液调为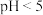 ,产生淡黄色沉淀。
,产生淡黄色沉淀。
①反应的离子方程式是________ 。
②不同pH时,硫化物去除率随时间的变化曲线如图。本工艺选择控制体系的 ,不选择
,不选择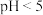 ,从环境保护的角度分析其主要原因:
,从环境保护的角度分析其主要原因:________ 。

(4)电浮选絮凝法处理含硫废水:
铝作阳极、石墨作阴极,以直流电电解含一定浓度 的
的 的含硫废水。阳极产生微小气泡,随后溶液中产生淡黄色浑浊,阳极附近生成的胶体吸附淡黄色浑浊。
的含硫废水。阳极产生微小气泡,随后溶液中产生淡黄色浑浊,阳极附近生成的胶体吸附淡黄色浑浊。
①用离子方程式表述产生淡黄色浑浊的可能原因:________ 。
②阴极产生的气泡把污水中的悬浮物(含阳极扩散的胶体)带到水面形成浮渣层,胶体的化学式:______ ,结合电极反应式解释浮渣层的形成过程:_______ 。
已知:
 有剧毒;常温下溶解度为
有剧毒;常温下溶解度为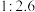 (体积)。
(体积)。(1)
 、
、 、
、 在水溶液中的物质的量分数随pH的分布曲线如图。
在水溶液中的物质的量分数随pH的分布曲线如图。
①当
 时,含硫废水中最主要的含硫(-2价)微粒是
时,含硫废水中最主要的含硫(-2价)微粒是②通过图中数据可估算得
 的
的 ”或“
”或“ ”)。
”)。(2)沉淀法处理含硫废水:
向
 的含硫废水中加入适量
的含硫废水中加入适量 的溶液,产生黑色沉淀且溶液的pH降低。用化学平衡移动的原理解释溶液的pH降低的原因:
的溶液,产生黑色沉淀且溶液的pH降低。用化学平衡移动的原理解释溶液的pH降低的原因:(3)氧化还原法处理含硫废水:
向
 的含硫废水中加入一定浓度的
的含硫废水中加入一定浓度的 溶液,加酸将溶液调为
溶液,加酸将溶液调为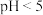 ,产生淡黄色沉淀。
,产生淡黄色沉淀。①反应的离子方程式是
②不同pH时,硫化物去除率随时间的变化曲线如图。本工艺选择控制体系的
 ,不选择
,不选择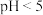 ,从环境保护的角度分析其主要原因:
,从环境保护的角度分析其主要原因:
(4)电浮选絮凝法处理含硫废水:
铝作阳极、石墨作阴极,以直流电电解含一定浓度
 的
的 的含硫废水。阳极产生微小气泡,随后溶液中产生淡黄色浑浊,阳极附近生成的胶体吸附淡黄色浑浊。
的含硫废水。阳极产生微小气泡,随后溶液中产生淡黄色浑浊,阳极附近生成的胶体吸附淡黄色浑浊。①用离子方程式表述产生淡黄色浑浊的可能原因:
②阴极产生的气泡把污水中的悬浮物(含阳极扩散的胶体)带到水面形成浮渣层,胶体的化学式:
更新时间:2024-01-19 11:44:15
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】黄铜矿(主要成分为 ,含有少量
,含有少量 )的分布较广,工业上常采用生物浸出技术处理黄铜矿,进而生产胆矾和绿矾(
)的分布较广,工业上常采用生物浸出技术处理黄铜矿,进而生产胆矾和绿矾( ),主要流程如下:
),主要流程如下:

已知:一些金属氢氧化物沉淀时的pH如下表:
请回答下列问题:
(1)下列有关“生物浸出”过程的说法正确的是___________。
(2)“生物浸出”时,氧气在有细菌存在的酸性溶液中可以将 氧化成硫酸盐,写出该反应的化学方程式:
氧化成硫酸盐,写出该反应的化学方程式:___________ 。
(3)调节pH时,应控制滤液1的pH范围为___________ 。
(4)试剂a和试剂b分别为___________ 、___________ 。
(5)由滤液3得到绿矾晶体的操作为:蒸发浓缩、___________ 、过滤、洗涤、干燥。
 ,含有少量
,含有少量 )的分布较广,工业上常采用生物浸出技术处理黄铜矿,进而生产胆矾和绿矾(
)的分布较广,工业上常采用生物浸出技术处理黄铜矿,进而生产胆矾和绿矾( ),主要流程如下:
),主要流程如下:
已知:一些金属氢氧化物沉淀时的pH如下表:
| 金属氢氧化物 |  |  |  |
| 开始沉淀时的pH | 1.6 | 4.2 | 6.3 |
| 完全沉淀时的pH | 3.1 | 6.2 | 8.3 |
(1)下列有关“生物浸出”过程的说法正确的是___________。
| A.将黄铜矿研磨成粉末可以加快浸出速率 |
| B.将稀硫酸改成浓硫酸可以加快浸出速率 |
| C.浸出时,温度越高浸出速率一定越快 |
| D.浸出时,细菌起到催化反应的作用 |
 氧化成硫酸盐,写出该反应的化学方程式:
氧化成硫酸盐,写出该反应的化学方程式:(3)调节pH时,应控制滤液1的pH范围为
(4)试剂a和试剂b分别为
(5)由滤液3得到绿矾晶体的操作为:蒸发浓缩、
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】某研究小组为“变废为宝”,将一批废弃的线路板简单处理后,得到含Cu、Al及少量Fe的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线。_______ 、_______ 。
(2)步骤①中能否用稀盐酸代替稀硫酸?_______ (填“能”或“否”)。
(3)为了将Fe2+氧化成Fe3+且不引入杂质,氧化剂A最好是_______ (填化学式)。
(4)若步骤②中有红棕色气体生成,该离子反应方程式为_______ ;步骤②中可通过控制H2SO4和HNO3的量,让 尽可能转化为气体逸出,则溶液B的溶质是
尽可能转化为气体逸出,则溶液B的溶质是_______ (填化学式);则从溶液B获得硫酸铜晶体的方法是_______ 。

(2)步骤①中能否用稀盐酸代替稀硫酸?
(3)为了将Fe2+氧化成Fe3+且不引入杂质,氧化剂A最好是
(4)若步骤②中有红棕色气体生成,该离子反应方程式为
 尽可能转化为气体逸出,则溶液B的溶质是
尽可能转化为气体逸出,则溶液B的溶质是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】工业上“中温焙烧——钠化氧化法”回收电镀污泥中的铬已获技术上的突破。其工艺流程如下:
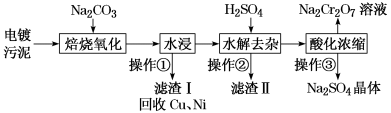
[查阅资料]①电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质;水浸后溶液中含有Na2CrO4、NaAlO2、Na2ZnO2等物质
②Na2SO4、Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表:
请回答:
(1)操作①的名称是___________ , “水浸”后的溶液呈___________ 性
(2)“焙烧氧化”过程中Cr(OH)3转化成Na2CrO4的化学方程式为___________ 。
(3)滤渣Ⅱ的主要成分有Zn(OH)2和X,生成X的离子反应方程式为___________
(4)“酸化浓缩”时,需继续加入H2SO4,使Na2CrO4转化成Na2Cr2O7,反应的离子方程式为___________

[查阅资料]①电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质;水浸后溶液中含有Na2CrO4、NaAlO2、Na2ZnO2等物质
②Na2SO4、Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表:
温度 化学式 | 20 ℃ | 60 ℃ | 100 ℃ |
| Na2SO4 | 19.5 | 45.3 | 42.5 |
| Na2Cr2O7 | 183 | 269 | 415 |
| Na2CrO4 | 84 | 115 | 126 |
(1)操作①的名称是
(2)“焙烧氧化”过程中Cr(OH)3转化成Na2CrO4的化学方程式为
(3)滤渣Ⅱ的主要成分有Zn(OH)2和X,生成X的离子反应方程式为
(4)“酸化浓缩”时,需继续加入H2SO4,使Na2CrO4转化成Na2Cr2O7,反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示)。HAc的应用与其电离平衡密切相关。
25℃时,HAc的。Ka=1.75x10-5=10-4.76
(1)配制250mL0.1mol/L的HAc溶液,需5mol/L的HAc溶液的体积为_______ mL。
(2)下列关于250mL容量瓶的操作,正确的是_______ 。

(3)某小组研究25℃下HAc电离平衡的影响因素。
提出假设。稀释HAc溶液或改变Ac-浓度,HAc电离平衡会发生移动。
设计方案并完成实验。用浓度均为0.1mol/L的HAc和NaAc溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。
①根据表中信息,补充数据:a=_______ ,b=_______ 。
②由实验I和II可知,稀释HAc溶液,电离平衡_______ (填”正”或”逆”)向移动;结合表中数据,给出判断理由:_____________________________________________ 。
③由实验II~VIII可知,增大Ac-浓度,HAc电离平衡逆向移动。实验结论假设成立。
(4)小组分析上表数据发现:随着 的增加,c(H+)的值逐渐接近HAc的Ka。
的增加,c(H+)的值逐渐接近HAc的Ka。
查阅资料获悉:一定条件下,按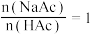 配制的溶液中,c(H+)的值等于HAc的Ka。
配制的溶液中,c(H+)的值等于HAc的Ka。
对比数据发现,实验VIII中pH=4.65与资料数据Ka=10-4.76存在一定差异;推测可能由物质浓度准确程度不够引起,故先准确测定HAc溶液的浓度再验证。
①移取20.00mLHAc溶液,加入2滴酚酞溶液,用0.1000mol/LNaOH溶液滴定至终点,消耗体积为22.08mL,则该HAc溶液的浓度为_______ mol/L。在答题卡虚线框中,画出上述过程的滴定曲线示意图并标注滴定终点_______ 。
②用上述HAc溶液和0.1000mol/LNaOH溶液,配制等物质的量的HAc与NaAc混合溶液,测定pH,结果与资料数据相符。
(5)小组进一步提出:如果只有浓度均约为0.1mol/L的HAc和NaOH溶液,如何准确测定HAc的Ka?小组同学设计方案并进行实验。请完成下表中II的内容。
实验总结: 得到的结果与资料数据相符,方案可行。
25℃时,HAc的。Ka=1.75x10-5=10-4.76
(1)配制250mL0.1mol/L的HAc溶液,需5mol/L的HAc溶液的体积为
(2)下列关于250mL容量瓶的操作,正确的是

(3)某小组研究25℃下HAc电离平衡的影响因素。
提出假设。稀释HAc溶液或改变Ac-浓度,HAc电离平衡会发生移动。
设计方案并完成实验。用浓度均为0.1mol/L的HAc和NaAc溶液,按下表配制总体积相同的系列溶液;测定pH,记录数据。
| 序号 | 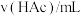 | 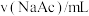 | 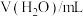 | 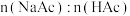 |  |
| I | 40.00 | / | / | 0 | 2.86 |
| II | 4.00 | / | 36.00 | 0 | 3.36 |
| … | |||||
| VII | 4.00 | a | b | 3:4 | 4.53 |
| VIII | 4.00 | 4.00 | 32.00 | 1:1 | 4.65 |
②由实验I和II可知,稀释HAc溶液,电离平衡
③由实验II~VIII可知,增大Ac-浓度,HAc电离平衡逆向移动。实验结论假设成立。
(4)小组分析上表数据发现:随着
 的增加,c(H+)的值逐渐接近HAc的Ka。
的增加,c(H+)的值逐渐接近HAc的Ka。查阅资料获悉:一定条件下,按
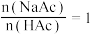 配制的溶液中,c(H+)的值等于HAc的Ka。
配制的溶液中,c(H+)的值等于HAc的Ka。对比数据发现,实验VIII中pH=4.65与资料数据Ka=10-4.76存在一定差异;推测可能由物质浓度准确程度不够引起,故先准确测定HAc溶液的浓度再验证。
①移取20.00mLHAc溶液,加入2滴酚酞溶液,用0.1000mol/LNaOH溶液滴定至终点,消耗体积为22.08mL,则该HAc溶液的浓度为
②用上述HAc溶液和0.1000mol/LNaOH溶液,配制等物质的量的HAc与NaAc混合溶液,测定pH,结果与资料数据相符。
(5)小组进一步提出:如果只有浓度均约为0.1mol/L的HAc和NaOH溶液,如何准确测定HAc的Ka?小组同学设计方案并进行实验。请完成下表中II的内容。
| I | 移取20.00mLHAc溶液,用NaOH溶液滴定至终点,消耗NaOH溶液V1mL |
| II |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)某温度(t℃)时,水的电离图象如下图所示,a点水的离子积Kw=_____ 该温度下,pH=11的NaOH溶液与pH=2的H2SO4溶液等体积混合,溶液显_____ (填“酸”或“碱”)性。

(2)25℃时,向0.1mol•L-1的氨水中加入少量NH4Cl固体,当固体溶解后,测得溶液pH_____ (填“增大”“减小”或“不变”,下同), 的物质的量浓度
的物质的量浓度_____
(3)将体积相等的NaOH稀溶液和CH3COOH溶液混合,若溶液中c(Na+)=c(CH3COO-),则该溶液显_____ (填“酸性”“碱性”或“中性”),则混合前c(NaOH)_____ (填“>”“<”或“=”)c(CH3COOH)
(4)常温下,Ksp[Fe(OH)3]=1×10-38,要使溶液中的Fe3+沉淀完全[残留在溶液中的c(Fe3+)<10-5mol•L-1],则溶液的pH应大于_____
(5)用可溶性碳酸盐,可以浸取CaSO4固体,在溶液浸取过程中会发生反应:CaSO4(s)+ (ag)⇌CaCO3(s)+
(ag)⇌CaCO3(s)+ (aq)。已知:298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,则此温度下该反应的平衡常数K为
(aq)。已知:298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,则此温度下该反应的平衡常数K为_____ (计算结果保留三位有效数字)。
(1)某温度(t℃)时,水的电离图象如下图所示,a点水的离子积Kw=

(2)25℃时,向0.1mol•L-1的氨水中加入少量NH4Cl固体,当固体溶解后,测得溶液pH
 的物质的量浓度
的物质的量浓度(3)将体积相等的NaOH稀溶液和CH3COOH溶液混合,若溶液中c(Na+)=c(CH3COO-),则该溶液显
(4)常温下,Ksp[Fe(OH)3]=1×10-38,要使溶液中的Fe3+沉淀完全[残留在溶液中的c(Fe3+)<10-5mol•L-1],则溶液的pH应大于
(5)用可溶性碳酸盐,可以浸取CaSO4固体,在溶液浸取过程中会发生反应:CaSO4(s)+
 (ag)⇌CaCO3(s)+
(ag)⇌CaCO3(s)+ (aq)。已知:298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,则此温度下该反应的平衡常数K为
(aq)。已知:298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,则此温度下该反应的平衡常数K为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题:
(1)航天领域中常用N2H4作为火箭发射的助燃剂。N2H4与氨气相似,是一种碱性气体,易溶于水,生成弱碱N2H4·H2O。用电离方程式表示N2H4·H2O显碱性的原因是:________ 。
(2)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,但产生的CO又会与CaSO4发生化学反应,相关的热化学方程式如下:
①CaSO4(s)+CO(g) ⇌CaO(s)+SO2(g)+CO2(g) △H=+210.5kJ· mol-1
②CaSO4(s)+4CO(g) ⇌CaS(s)+ 4CO2(g) △H=-189.2 kJ· mol-1
反应CaO(s)+3CO(g)+SO2(g) ⇌CaS(s)+3CO2(g) △H=____ kJ· mol-1
(3)在恒温条件下,1 mol NO2和足量C发生反应2NO2(g)+2C(s)⇌N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
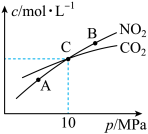
①A、B两点的浓度平衡常数关系:Kc(A)____ Kc(B)(填“<”或“>”或“=”)
②A、B、C三点中NO2的转化率最高的是____ (填“A”或“B”或“C”)点。
(4)已知:亚硝酸(HNO2)性质和硝酸类似,但它是一种弱酸。常温下亚硝酸的电离平衡常数Ka=5.1×10-4;H2CO3的Ka1=4.2×10-7,Ka2=5.61×10-11。在常温下向含有2mol碳酸钠的溶液中加入1mol的HNO2后,则溶液中CO32-、HCO3-和NO2-的离子浓度由大到小的顺序是________ 。
(1)航天领域中常用N2H4作为火箭发射的助燃剂。N2H4与氨气相似,是一种碱性气体,易溶于水,生成弱碱N2H4·H2O。用电离方程式表示N2H4·H2O显碱性的原因是:
(2)一种煤炭脱硫技术可以把硫元素以CaSO4的形成固定下来,但产生的CO又会与CaSO4发生化学反应,相关的热化学方程式如下:
①CaSO4(s)+CO(g) ⇌CaO(s)+SO2(g)+CO2(g) △H=+210.5kJ· mol-1
②CaSO4(s)+4CO(g) ⇌CaS(s)+ 4CO2(g) △H=-189.2 kJ· mol-1
反应CaO(s)+3CO(g)+SO2(g) ⇌CaS(s)+3CO2(g) △H=
(3)在恒温条件下,1 mol NO2和足量C发生反应2NO2(g)+2C(s)⇌N2(g)+2CO2(g),测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:

①A、B两点的浓度平衡常数关系:Kc(A)
②A、B、C三点中NO2的转化率最高的是
(4)已知:亚硝酸(HNO2)性质和硝酸类似,但它是一种弱酸。常温下亚硝酸的电离平衡常数Ka=5.1×10-4;H2CO3的Ka1=4.2×10-7,Ka2=5.61×10-11。在常温下向含有2mol碳酸钠的溶液中加入1mol的HNO2后,则溶液中CO32-、HCO3-和NO2-的离子浓度由大到小的顺序是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】为了探究原电池和电解池的工作原理,某研究性学习小组分别用如图甲、乙所示的装置进行实验,回答下列问题。
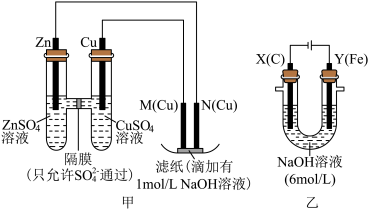
Ⅰ.用甲装置进行第一组实验:
(1)甲中电子的流向正确的是_____ (填序号)。
A.由Cu流向M,M流向N,N流向Zn
B.由Cu沿导线流向M,由N沿导线流向Zn
C.由Zn沿导线流向N,由M沿导线流向Cu
(2)在保证电极反应不变的情况下,下列材料能代替硫酸铜溶液中Cu电极的是_____(填序号)。
(3)实验过程中,甲池左侧的 浓度
浓度_____ (填“增大”或“减小”),滤纸上能观察到的现象是_____ 。
Ⅱ.该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子( )在溶液中呈紫红色。请根据实验现象及资料信息,填写下列空白:
)在溶液中呈紫红色。请根据实验现象及资料信息,填写下列空白:
(4)可用碱性甲烷燃料电池作为乙池的外加电源,写出该燃料电池负极的电极反应式_____ 。
(5)电解过程中,X极附近溶液的碱性_____ (填“增强”“减弱”或“不变”)。
(6)电解过程中,Y极发生的电极反应为 和
和_____ 。

Ⅰ.用甲装置进行第一组实验:
(1)甲中电子的流向正确的是
A.由Cu流向M,M流向N,N流向Zn
B.由Cu沿导线流向M,由N沿导线流向Zn
C.由Zn沿导线流向N,由M沿导线流向Cu
(2)在保证电极反应不变的情况下,下列材料能代替硫酸铜溶液中Cu电极的是_____(填序号)。
| A.石墨 | B.铂 | C.铝 | D.镁 |
 浓度
浓度Ⅱ.该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子(
 )在溶液中呈紫红色。请根据实验现象及资料信息,填写下列空白:
)在溶液中呈紫红色。请根据实验现象及资料信息,填写下列空白:(4)可用碱性甲烷燃料电池作为乙池的外加电源,写出该燃料电池负极的电极反应式
(5)电解过程中,X极附近溶液的碱性
(6)电解过程中,Y极发生的电极反应为
 和
和
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】以黄铜矿精矿为原料,制取金属铜的工艺如下。
I.将黄铜矿精矿(主要成分为 ,含有少量CaO、MgO、
,含有少量CaO、MgO、 )粉碎;
)粉碎;
II.采用如图所示装置进行电化学浸出实验。将精选黄铜矿粉加入电解槽的阳极区,恒速搅拌,使矿粉溶解。在阴极区通入氧气,并加入少量催化剂;

III.一段时间后,抽取阴极区溶液,向其中加入有机萃取剂(RH)发生反应: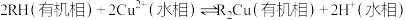 分离出有机相,向其中加入一定浓度的硫酸,使
分离出有机相,向其中加入一定浓度的硫酸,使 得以再生;
得以再生;
IV.电解硫酸铜溶液制得金属铜。
回答下列问题:
(1)黄铜矿粉加入阳极区与硫酸主要发生以下反应: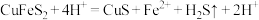 ,阳极区硫酸铁的主要作用是
,阳极区硫酸铁的主要作用是_______ 。
(2)阴极区,电极上开始时有大量气泡产生,后有红色固体析出,一段时间后红色固体溶解。红色固体溶解相当于_______ (选填“析氢”或“吸氧”)腐蚀。
(3)若在实验室进行步骤III,加入有机萃取剂的目的是_______ 。
(4)步骤III中 得以再生的原理是
得以再生的原理是_______ 。
I.将黄铜矿精矿(主要成分为
 ,含有少量CaO、MgO、
,含有少量CaO、MgO、 )粉碎;
)粉碎;II.采用如图所示装置进行电化学浸出实验。将精选黄铜矿粉加入电解槽的阳极区,恒速搅拌,使矿粉溶解。在阴极区通入氧气,并加入少量催化剂;

III.一段时间后,抽取阴极区溶液,向其中加入有机萃取剂(RH)发生反应:
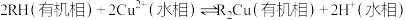 分离出有机相,向其中加入一定浓度的硫酸,使
分离出有机相,向其中加入一定浓度的硫酸,使 得以再生;
得以再生;IV.电解硫酸铜溶液制得金属铜。
回答下列问题:
(1)黄铜矿粉加入阳极区与硫酸主要发生以下反应:
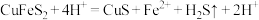 ,阳极区硫酸铁的主要作用是
,阳极区硫酸铁的主要作用是(2)阴极区,电极上开始时有大量气泡产生,后有红色固体析出,一段时间后红色固体溶解。红色固体溶解相当于
(3)若在实验室进行步骤III,加入有机萃取剂的目的是
(4)步骤III中
 得以再生的原理是
得以再生的原理是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学兴趣小组在实验室中以烧杯为容器,用饱和 溶液制备
溶液制备 胶体,并对其性质做了如下探究:
胶体,并对其性质做了如下探究:
(1)将饱和 溶液加到
溶液加到___________ 中,可制得 胶体。制备过程中,发生化学反应的方程式为
胶体。制备过程中,发生化学反应的方程式为___________ 。
(2)小米同学在制备时,加热时间过久,结果未能得到胶体。那么小米同学得到的物质应该是:_______ (填化学式),该物质属于_______ (请从下面选择)。
A.酸 B.碱 C.盐
(3)小庄同学想证明 胶体已经制备成功,她可以利用
胶体已经制备成功,她可以利用___________ (最简单的方法,请写出方法的名称)进行鉴别。
(4)小静同学利用___________ (填方法名称)方法对 胶体提纯。
胶体提纯。
(5)小邱同学将提纯后的 胶体置于U型管中,通入直流电一段时间后,观察到与电源负极相连的那个电极附近的颜色变深,说明可知
胶体置于U型管中,通入直流电一段时间后,观察到与电源负极相连的那个电极附近的颜色变深,说明可知 胶粒带
胶粒带___________ 电荷(填“正”、“负”或者“不带”)。化学上把这种现象称为___________ 。
 溶液制备
溶液制备 胶体,并对其性质做了如下探究:
胶体,并对其性质做了如下探究:(1)将饱和
 溶液加到
溶液加到 胶体。制备过程中,发生化学反应的方程式为
胶体。制备过程中,发生化学反应的方程式为(2)小米同学在制备时,加热时间过久,结果未能得到胶体。那么小米同学得到的物质应该是:
A.酸 B.碱 C.盐
(3)小庄同学想证明
 胶体已经制备成功,她可以利用
胶体已经制备成功,她可以利用(4)小静同学利用
 胶体提纯。
胶体提纯。(5)小邱同学将提纯后的
 胶体置于U型管中,通入直流电一段时间后,观察到与电源负极相连的那个电极附近的颜色变深,说明可知
胶体置于U型管中,通入直流电一段时间后,观察到与电源负极相连的那个电极附近的颜色变深,说明可知 胶粒带
胶粒带
您最近一年使用:0次



