高铁酸钠( )是一种多功能绿色水处理剂,杀菌消毒的同时可生成氢氧化铁胶体。某工厂利用废金属屑(主要成分为Fe和Cu,含有少量
)是一种多功能绿色水处理剂,杀菌消毒的同时可生成氢氧化铁胶体。某工厂利用废金属屑(主要成分为Fe和Cu,含有少量 )制取
)制取 并回收金属Cu,工艺流程如下:
并回收金属Cu,工艺流程如下:
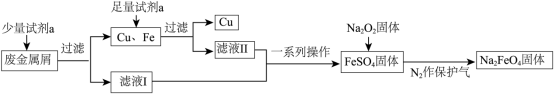
(1)试剂a为___________ (填化学式)。
(2)用离子方程式解释滤液I不含有 可能的原因
可能的原因___________ 。
(3)制备 的原理:
的原理: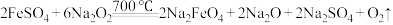 。反应中
。反应中___________ 作还原剂;每生成1mol 转移电子的物质的量为
转移电子的物质的量为___________ mol。
(4)高铁酸钠( )是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。
)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。
①某兴趣小组欲用 固体配制100mL
固体配制100mL 的高铁酸钠溶液,需要高铁酸钠固体的质量为
的高铁酸钠溶液,需要高铁酸钠固体的质量为___________ g。配制所用的容量瓶上标有___________ 、___________ 、刻度线。
②下列操作导致浓度偏低的是___________ 。
A.容量瓶用蒸馏水洗净之后,直接用于溶液的配制
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.摇匀后,发现液面低于刻度线,又滴加蒸馏水至与刻度线相切
D.定容时,俯视刻度线
 )是一种多功能绿色水处理剂,杀菌消毒的同时可生成氢氧化铁胶体。某工厂利用废金属屑(主要成分为Fe和Cu,含有少量
)是一种多功能绿色水处理剂,杀菌消毒的同时可生成氢氧化铁胶体。某工厂利用废金属屑(主要成分为Fe和Cu,含有少量 )制取
)制取 并回收金属Cu,工艺流程如下:
并回收金属Cu,工艺流程如下:
(1)试剂a为
(2)用离子方程式解释滤液I不含有
 可能的原因
可能的原因(3)制备
 的原理:
的原理: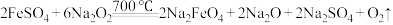 。反应中
。反应中 转移电子的物质的量为
转移电子的物质的量为(4)高铁酸钠(
 )是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。
)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。①某兴趣小组欲用
 固体配制100mL
固体配制100mL 的高铁酸钠溶液,需要高铁酸钠固体的质量为
的高铁酸钠溶液,需要高铁酸钠固体的质量为②下列操作导致浓度偏低的是
A.容量瓶用蒸馏水洗净之后,直接用于溶液的配制
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.摇匀后,发现液面低于刻度线,又滴加蒸馏水至与刻度线相切
D.定容时,俯视刻度线
更新时间:2024-01-24 21:41:58
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】如图是部分金属和非金属材料发现和使用的时间简轴。
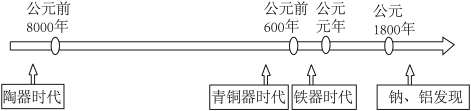
(1)材料的不断发展可以促进社会进步。
①上述金属的常见化合物中,呈淡黄色的是_______ (填化学式)。
②目前应用最多的太阳能电池的光电转化材料是_______ (填化学式)。
③氮化铝(AlN)广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过反应Al2O3+N2+C→AlN+CO合成,配平并用双线桥法标出该反应中电子转移的方向和数目_______ 。
(2)向充满CO2的铝制易拉罐中注入足量的NaOH溶液,立即用胶布封严罐口,罐壁立即内陷,一段时间后,罐壁又重新鼓起来恢复原样。写出易拉罐重新鼓起来时发生反应的化学方程式_______ 。
(3)某同学用下图实验装置探究铁盐与亚铁盐的性质。
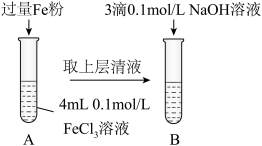
①试管A中发生反应的离子方程式为_______ 。
②试管B中可观察到的现象是_______ 。
(4)“侯氏制碱法”以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。若制得的纯碱中只含有杂质NaCl,要测定该纯碱的纯度,下列方案可行的是_______ (填字母)。
a.向m g纯碱样品中加入足量CaCl2溶液,沉淀经过滤、洗涤、干燥,称其质量为b g
b.向m g纯碱样品中加入足量稀盐酸,用碱石灰(主要成分是CaO和NaOH)吸收产生的气体,碱石灰增重b g
c.准确称量m g样品,加热至恒重,称量得b g固体

(1)材料的不断发展可以促进社会进步。
①上述金属的常见化合物中,呈淡黄色的是
②目前应用最多的太阳能电池的光电转化材料是
③氮化铝(AlN)广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过反应Al2O3+N2+C→AlN+CO合成,配平并用双线桥法标出该反应中电子转移的方向和数目
(2)向充满CO2的铝制易拉罐中注入足量的NaOH溶液,立即用胶布封严罐口,罐壁立即内陷,一段时间后,罐壁又重新鼓起来恢复原样。写出易拉罐重新鼓起来时发生反应的化学方程式
(3)某同学用下图实验装置探究铁盐与亚铁盐的性质。

①试管A中发生反应的离子方程式为
②试管B中可观察到的现象是
(4)“侯氏制碱法”以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。若制得的纯碱中只含有杂质NaCl,要测定该纯碱的纯度,下列方案可行的是
a.向m g纯碱样品中加入足量CaCl2溶液,沉淀经过滤、洗涤、干燥,称其质量为b g
b.向m g纯碱样品中加入足量稀盐酸,用碱石灰(主要成分是CaO和NaOH)吸收产生的气体,碱石灰增重b g
c.准确称量m g样品,加热至恒重,称量得b g固体
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】W、X、Y、Z都是中学化学中常见物质,其中W、X、Y中均含有同一种元素,在一定条件下的相互转化关系如图所示(部分反应中的水已略去)。

根据题意回答下列问题:
(1)若W、X、Y的焰色试验均为黄色,且W为强碱,Z为绿色植物光合作用不可或缺的原料。
①W、X、Y、Z中是电解质的为_______ (填化学式)。
②除去X固体中混有的Y固体的方法为_______ (填除杂方法的名称);若向X的饱和溶液中通入足量的Z,则可观察到的现象为_______ 。
③反应III的离子方程式为_______ 。
(2)若W为气体单质,Z为一种生活中应用最广泛的金属单质。
①反应II的离子方程式为_______ 。
②一定条件下,Z能与水发生反应,该反应的化学方程式为_______ 。

根据题意回答下列问题:
(1)若W、X、Y的焰色试验均为黄色,且W为强碱,Z为绿色植物光合作用不可或缺的原料。
①W、X、Y、Z中是电解质的为
②除去X固体中混有的Y固体的方法为
③反应III的离子方程式为
(2)若W为气体单质,Z为一种生活中应用最广泛的金属单质。
①反应II的离子方程式为
②一定条件下,Z能与水发生反应,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】钪的价格昂贵,在地壳里的含量只有0.0005%,化学性质非常活泼。从铝土矿生产Al2O3的副产品“赤泥”(主要成分为Al2O3、Fe2O3、TiO2、Sc2O3)中回收钪,同时生产聚合硫酸铁铝[ AlFe( OH)6-2n(SO4)n]具有极其重要的工业价值,一种工艺流程如下:
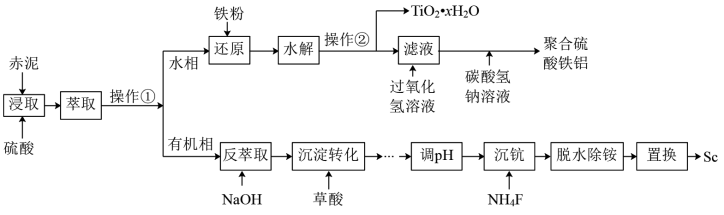
已知:钪离子可以在不同pH下生成[ Sc( OH)n]3-n(n=1~6)。
请回答以下问题:
(1)操作②的名称___________ ,操作①和操作②中都使用的玻璃仪器是___________ 。
(2)加入铁粉的作用___________ 。
(3)生成聚合硫酸铁铝[AlFe( OH)6-2n(SO4)n]的离子方程式为___________ 。
(4)钪的发现较晚,主要是因为___________ 。
(5)“反萃取”时若加的入氢氧化钠过量, Sc(OH)3沉淀会溶解。写出Sc(OH)3与过量NaOH溶液反应的化学方程式___________ 。
(6)常温下,三价Sc的部分存在形式与氟离子浓度的对数[1gc(F-)]、pH的关系如图所示。若溶液中c(F- )=5 ×10-6mol·L-1,“调pH”过程中控制pH=7,则调节pH后三价Sc的存在形式为___________ (填化学式)(lg5=0.7)。

如果Sc的沉淀方式主要是ScF3,则溶液中c(F -)应该大于___________ mol ·L-1(100.6=4)
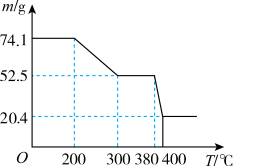
(7)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O分解得到ScF3,固体样品质量与温度的关系如图所示。加热至380-400℃产生白烟, 400℃以上质量不再改变。则a=___________ (填数字)。

已知:钪离子可以在不同pH下生成[ Sc( OH)n]3-n(n=1~6)。
请回答以下问题:
(1)操作②的名称
(2)加入铁粉的作用
(3)生成聚合硫酸铁铝[AlFe( OH)6-2n(SO4)n]的离子方程式为
(4)钪的发现较晚,主要是因为
(5)“反萃取”时若加的入氢氧化钠过量, Sc(OH)3沉淀会溶解。写出Sc(OH)3与过量NaOH溶液反应的化学方程式
(6)常温下,三价Sc的部分存在形式与氟离子浓度的对数[1gc(F-)]、pH的关系如图所示。若溶液中c(F- )=5 ×10-6mol·L-1,“调pH”过程中控制pH=7,则调节pH后三价Sc的存在形式为

如果Sc的沉淀方式主要是ScF3,则溶液中c(F -)应该大于
(7)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O分解得到ScF3,固体样品质量与温度的关系如图所示。加热至380-400℃产生白烟, 400℃以上质量不再改变。则a=

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】在工业上,可以从废水或废料中回收金属单质或金属的化合物。
Ⅰ.某工厂排出的废水中含有大量的Fe2+、Cu2+和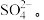 某校研究性学习小组设计如图流程以回收铜和硫酸亚铁。
某校研究性学习小组设计如图流程以回收铜和硫酸亚铁。

(1)操作①中用到的玻璃仪器是_____(填序号)。
(2)固体成份是_____ (填名称)。
(3)原料②的名称_____ 。
(4)回收的铜可用于制备胆矾 ,可将铜和一定浓度稀硫酸混合后并在加热的情况下通入氧气,发生如下反应:
,可将铜和一定浓度稀硫酸混合后并在加热的情况下通入氧气,发生如下反应: ,制得硫酸铜溶液后经过蒸发、浓缩,冷却结晶,过滤可得胆矾。请分析上述反应中,氧化剂是
,制得硫酸铜溶液后经过蒸发、浓缩,冷却结晶,过滤可得胆矾。请分析上述反应中,氧化剂是_____ (填化学式)。
Ⅱ.某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取PAFC(聚合氯化铁铝 设计生产流程如下,请回答下列问题:
设计生产流程如下,请回答下列问题:

(5)用 的浓盐酸配制
的浓盐酸配制 的稀盐酸,所用玻璃仪器除量筒和玻璃棒外,还有_____(填序号)。
的稀盐酸,所用玻璃仪器除量筒和玻璃棒外,还有_____(填序号)。
(6)下列关于PAFC的说法中正确的是_____(填序号)。
(7)步骤Ⅱ中取样分析的目的是_____(填序号)。
(8)写出向溶液中加入NaClO3时,发生反应的离子方程式为_____ 。
Ⅰ.某工厂排出的废水中含有大量的Fe2+、Cu2+和
 某校研究性学习小组设计如图流程以回收铜和硫酸亚铁。
某校研究性学习小组设计如图流程以回收铜和硫酸亚铁。
(1)操作①中用到的玻璃仪器是_____(填序号)。
| A.烧杯 | B.漏斗 | C.玻璃棒 | D.酒精灯 |
(2)固体成份是
(3)原料②的名称
(4)回收的铜可用于制备胆矾
 ,可将铜和一定浓度稀硫酸混合后并在加热的情况下通入氧气,发生如下反应:
,可将铜和一定浓度稀硫酸混合后并在加热的情况下通入氧气,发生如下反应: ,制得硫酸铜溶液后经过蒸发、浓缩,冷却结晶,过滤可得胆矾。请分析上述反应中,氧化剂是
,制得硫酸铜溶液后经过蒸发、浓缩,冷却结晶,过滤可得胆矾。请分析上述反应中,氧化剂是Ⅱ.某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取PAFC(聚合氯化铁铝
 设计生产流程如下,请回答下列问题:
设计生产流程如下,请回答下列问题:
(5)用
 的浓盐酸配制
的浓盐酸配制 的稀盐酸,所用玻璃仪器除量筒和玻璃棒外,还有_____(填序号)。
的稀盐酸,所用玻璃仪器除量筒和玻璃棒外,还有_____(填序号)。| A.容量瓶 | B.烧杯 | C.烧瓶 | D.胶头滴管 |
(6)下列关于PAFC的说法中正确的是_____(填序号)。
| A.PAFC是一种有机高分子化合物 |
| B.PAFC中Fe显+2价 |
| C.PAFC溶于水能电离出OH-,是一种碱 |
| D.PAFC在强酸性和强碱性溶液中均不能稳定存在 |
(7)步骤Ⅱ中取样分析的目的是_____(填序号)。
A.测定溶液中 与 与 的含量比 的含量比 |
| B.测定原料是否完全溶解 |
C.测定溶液中 的含量,以确定加入 的含量,以确定加入 的量 的量 |
| D.测定溶液中Al3+的含量 |
(8)写出向溶液中加入NaClO3时,发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出,所用试剂均足量),其中X是氨水,I为红褐色沉淀。

请回答下列问题:
(1)J的化学式为_________ ,J的颜色是_________
(2)D→E的离子方程式为_________ ,
(3)H→I的化学方程式为_________ ,现象为_________
(4)鉴别G溶液中的金属阳离子时,应滴加的试剂依次是_________ ,现象是_________ ,请写出此鉴别过程中属于氧化还原反应的离子方程式_________

请回答下列问题:
(1)J的化学式为
(2)D→E的离子方程式为
(3)H→I的化学方程式为
(4)鉴别G溶液中的金属阳离子时,应滴加的试剂依次是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3、MgO等,工艺流程简化示意图如下:

根据上图回答下列问题:
(1)将菱锌矿研磨成粉的目的是使_____________________________ 。
(2)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,相对分子质量是89,针铁矿中铁原子数∶氧原子数∶氢原子数=________ 。
(3)请写出氢氧化锌和稀硫酸反应的化学方程式________________________ 。该反应的基本类型是_____________ 。
(4)“滤液3”之前加入锌粉的目的是__________________ 。
(5)“滤液3”之后的操作依次为________ 、干燥。
(6)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于___________ ×100%。

根据上图回答下列问题:
(1)将菱锌矿研磨成粉的目的是使
(2)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,相对分子质量是89,针铁矿中铁原子数∶氧原子数∶氢原子数=
(3)请写出氢氧化锌和稀硫酸反应的化学方程式
(4)“滤液3”之前加入锌粉的目的是
(5)“滤液3”之后的操作依次为
(6)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某次实验需用0.4 mol/L NaOH溶液480mL。配制方法如下:
(1)配制该溶液应选用________ mL容量瓶;
(2)用托盘天平准确称量________ g 固体NaOH,应放在________ (仪器)中称量。
(3)将称量好的NaOH固体放在500mL大烧杯中,倒入约100mL蒸馏水,用玻璃棒搅拌,使固体全部溶解,待______________ 后,将烧杯中的溶液注入容量瓶中;
(4)用少量蒸馏水洗涤烧杯________ 次,洗涤后的溶液_______________ ,轻轻晃动容量瓶,使溶液混合均匀;
(5)向容量瓶中加入蒸馏水,到液面接近刻度线__________ 时,改用_________ 加蒸馏水至液面最低点与刻度线相切。盖好瓶塞,上下颠倒混合均匀;
(6)若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏高的是________ ,偏低的是________ ,对实验结果没有影响的是____________ (填各选项的序号)。
A.所用的NaOH中混有少量Na2CO3
B.用带有生锈砝码的托盘天平称量一定质量固体NaOH
C.配制溶液所用的容量瓶洗净后没有烘干
D.固体NaOH在烧杯中溶解后立即将溶液转移到容量瓶内并接着进行后续操作
E.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
F.最后确定NaOH溶液体积(定容)时,俯视观察液面与容量瓶刻度线
G.定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线
(1)配制该溶液应选用
(2)用托盘天平准确称量
(3)将称量好的NaOH固体放在500mL大烧杯中,倒入约100mL蒸馏水,用玻璃棒搅拌,使固体全部溶解,待
(4)用少量蒸馏水洗涤烧杯
(5)向容量瓶中加入蒸馏水,到液面接近刻度线
(6)若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏高的是
A.所用的NaOH中混有少量Na2CO3
B.用带有生锈砝码的托盘天平称量一定质量固体NaOH
C.配制溶液所用的容量瓶洗净后没有烘干
D.固体NaOH在烧杯中溶解后立即将溶液转移到容量瓶内并接着进行后续操作
E.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
F.最后确定NaOH溶液体积(定容)时,俯视观察液面与容量瓶刻度线
G.定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】8月29日,华为Mate60Pro横空出世,国产麒麟9000s芯片闪耀登场。华为的坚毅不屈成就了中国芯,不仅值得我们骄傲,更值得我们每个中国人学习!大国制造彰显中国实力,化学材料助力科技成果的转化与应用。高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下。

(1)用石英砂和焦炭在电弧炉中制粗硅,该反应的化学方程式为___________ 。
(2) 是生产多晶硅的副产物。已知
是生产多晶硅的副产物。已知 比
比 更易水解,导致
更易水解,导致 更易水解的因素有
更易水解的因素有___________ (填标号)。
a. 键极性更大 b.
键极性更大 b. 的原子半径更大 c.
的原子半径更大 c. 键键能更大
键键能更大
(3) 的晶体类型
的晶体类型___________ ;碳原子和氧原子之间可以形成双键,而硅原子和氧原子很难形成双键,其原因是___________ 。
运用所学化学原理,解决下列问题:
(4)已知: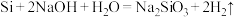 。某同学利用单质硅和铁为电极材料设计原电池(
。某同学利用单质硅和铁为电极材料设计原电池( 为电解质溶液),该原电池负极的电极反应式为
为电解质溶液),该原电池负极的电极反应式为___________ 。
(5)配制实验所需的 溶液时,下列操作会导致所配溶液浓度偏高的是___________。
溶液时,下列操作会导致所配溶液浓度偏高的是___________。

(1)用石英砂和焦炭在电弧炉中制粗硅,该反应的化学方程式为
(2)
 是生产多晶硅的副产物。已知
是生产多晶硅的副产物。已知 比
比 更易水解,导致
更易水解,导致 更易水解的因素有
更易水解的因素有a.
 键极性更大 b.
键极性更大 b. 的原子半径更大 c.
的原子半径更大 c. 键键能更大
键键能更大(3)
 的晶体类型
的晶体类型运用所学化学原理,解决下列问题:
(4)已知:
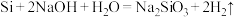 。某同学利用单质硅和铁为电极材料设计原电池(
。某同学利用单质硅和铁为电极材料设计原电池( 为电解质溶液),该原电池负极的电极反应式为
为电解质溶液),该原电池负极的电极反应式为(5)配制实验所需的
 溶液时,下列操作会导致所配溶液浓度偏高的是___________。
溶液时,下列操作会导致所配溶液浓度偏高的是___________。| A.未冷却至室温就定容 | B.容量瓶用蒸馏水洗净后未干燥 |
| C.定容时俯视读取刻度 | D.定容时液面超过了刻度线,并将多余溶液析出 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某小组同学需要85mL0.1mol·L-1Na2CO3溶液以备实验使用,回答下列问题:
(1)85mL0.1mol·L-1Na2CO3溶液中c(Na+)=___ mol·L-1。
(2)该同学应选择___ mL的容量瓶。
(3)若用Na2CO3·10H2O晶体来配制溶液,需用托盘天平称量固体___ 克。
(4)如图是某同学一些配制过程的关键步骤和操作,其中有错误的是___ (选填操作序号)。
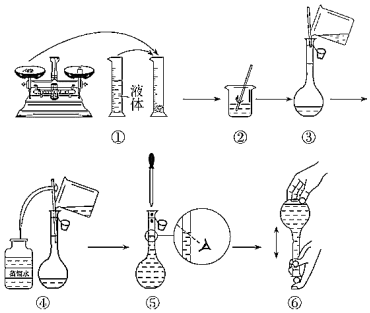
(5)下列操作会使配得的溶液浓度偏低的是___ 。
a.Na2CO3·10H2O晶体失去了部分结晶水
b.定容时液面超过刻度线,吸出一部分溶液
c.碳酸钠晶体不纯,其中混有氯化钠
d.称量碳酸钠晶体时所用砝码生锈
(1)85mL0.1mol·L-1Na2CO3溶液中c(Na+)=
(2)该同学应选择
(3)若用Na2CO3·10H2O晶体来配制溶液,需用托盘天平称量固体
(4)如图是某同学一些配制过程的关键步骤和操作,其中有错误的是

(5)下列操作会使配得的溶液浓度偏低的是
a.Na2CO3·10H2O晶体失去了部分结晶水
b.定容时液面超过刻度线,吸出一部分溶液
c.碳酸钠晶体不纯,其中混有氯化钠
d.称量碳酸钠晶体时所用砝码生锈
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铜和三氧化二铁在工农业生产中用途广泛,用黄铜矿(主要成分为CuFeS2,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:

(1)将黄铜矿粉碎的目的是___________ 。
(2)高温焙烧时发生的反应方程式为 ,1molO2参加反应时,反应中转移电子
,1molO2参加反应时,反应中转移电子___________ mol。
(3)操作a使用的玻璃仪器为___________ 。
(4)向滤液A中通入Cl2的目的是___________ 。
(5)向溶液B中通入NH3时反应的离子方程式为___________ 。
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):
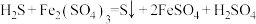 ,
,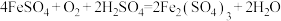
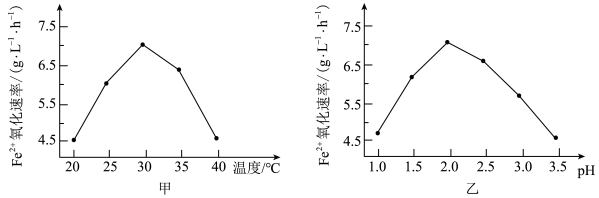
由图甲和图乙判断使用硫杆菌的最佳条件为___________

(1)将黄铜矿粉碎的目的是
(2)高温焙烧时发生的反应方程式为
 ,1molO2参加反应时,反应中转移电子
,1molO2参加反应时,反应中转移电子(3)操作a使用的玻璃仪器为
(4)向滤液A中通入Cl2的目的是
(5)向溶液B中通入NH3时反应的离子方程式为
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):
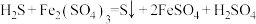 ,
,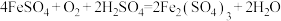
由图甲和图乙判断使用硫杆菌的最佳条件为___________

| A.温度为20℃,pH=2.0 |
| B.温度为30℃,pH=2.0 |
| C.温度为30℃,pH=1.0 |
| D.温度为40℃,pH=2.0 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:____________ 。当有1molC参与反应时,该反应转移的电子数是_____________ 。
(2)还原炉中发生的化学反应方程式为:____________ 。
(3)上述工艺生产中循环使用的物质除Si、SiHCl3外,还有_____________ 。
(4)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为____________ 。
(5)关于硅及其相关化合物的叙述正确的是_____________
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于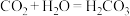 ,因此
,因此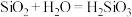
C.硅元素在金属与非金属的分界线处,一般可用于作为半导体材料
D.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
E.玻璃、水泥、陶瓷都是传统的硅酸盐产品
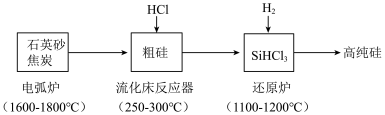
(2)还原炉中发生的化学反应方程式为:
(3)上述工艺生产中循环使用的物质除Si、SiHCl3外,还有
(4)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为
(5)关于硅及其相关化合物的叙述正确的是
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于
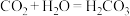 ,因此
,因此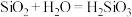
C.硅元素在金属与非金属的分界线处,一般可用于作为半导体材料
D.SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
E.玻璃、水泥、陶瓷都是传统的硅酸盐产品
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】现有X、Y、Z三种元素(1-18号)。①Z的单质可以在Y的单质中燃烧,生成Z2Y2.②X的单质可与Y的单质化合,生成两种液态化合物X2Y,X2Y2
(1)X、Z的元素符号分别为___________ 、___________ 。
(2)将Z的单质溶于X2Y中的离子方程式为___________ 。
(3)如果X2Y,X2Y2含有相同的原子数,则它们的物质的量之比为___________
(4)高铁酸盐(Z2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸盐(Z2FeO4)有多种方法,其中一种方法的化学原理可用化学方程式表示为:3ZClO + 2Fe(OH)3 + 4ZOH = 2Z2FeO4 + 3ZCl + 5H2O
①请用双线桥表示该氧化还原反应中电子转移的方向和数目___________ ;
②该反应中氧化剂是___________ ;
③反应中当有3mol电子转移时,生成高铁酸盐(Z2FeO4)的质量为___________ g;
(1)X、Z的元素符号分别为
(2)将Z的单质溶于X2Y中的离子方程式为
(3)如果X2Y,X2Y2含有相同的原子数,则它们的物质的量之比为
(4)高铁酸盐(Z2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸盐(Z2FeO4)有多种方法,其中一种方法的化学原理可用化学方程式表示为:3ZClO + 2Fe(OH)3 + 4ZOH = 2Z2FeO4 + 3ZCl + 5H2O
①请用双线桥表示该氧化还原反应中电子转移的方向和数目
②该反应中氧化剂是
③反应中当有3mol电子转移时,生成高铁酸盐(Z2FeO4)的质量为
您最近一年使用:0次



