二氯化二硫 常用作杀虫剂、萃取剂以及橡胶的低温硫化剂等。
常用作杀虫剂、萃取剂以及橡胶的低温硫化剂等。 沸点为
沸点为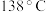 ,遇水会发生化学反应。二氯化二硫具有很高的化学反应活性,能被金属还原生成氯化物和硫化物,向熔融的硫中通入氯气即可生成
,遇水会发生化学反应。二氯化二硫具有很高的化学反应活性,能被金属还原生成氯化物和硫化物,向熔融的硫中通入氯气即可生成 。实验室用S和
。实验室用S和 制备
制备 的装置如图(部分夹持装置已略去)。
的装置如图(部分夹持装置已略去)。
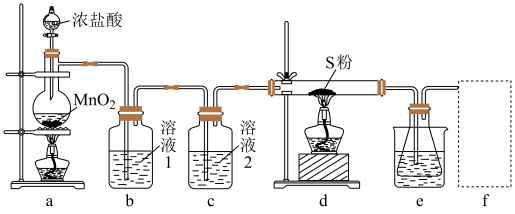
回答下列问题:
(1)装置b用于吸收 ,则溶液1为
,则溶液1为_______ ;溶液2的作用为_______ 。
(2)实验开始时,先点燃a处酒精灯,圆底烧瓶中发生反应的化学方程式为_______ ,当_______ (描述现象)时,点燃d处酒精灯。
(3)e中大烧杯装有冰水,作用是_______ ;f可以选用_______ (填标号)装置。
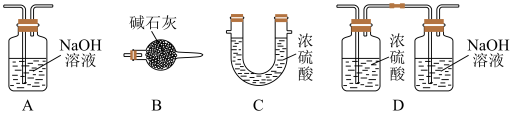
(4) (
( 中S为
中S为 价)遇水会生成
价)遇水会生成 、一种强酸和一种淡黄色固体单质,该反应的化学方程式为
、一种强酸和一种淡黄色固体单质,该反应的化学方程式为_______ ,反应中每转移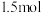 电子,生成的
电子,生成的 在标准状况下的体积为
在标准状况下的体积为_______  。
。
 常用作杀虫剂、萃取剂以及橡胶的低温硫化剂等。
常用作杀虫剂、萃取剂以及橡胶的低温硫化剂等。 沸点为
沸点为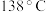 ,遇水会发生化学反应。二氯化二硫具有很高的化学反应活性,能被金属还原生成氯化物和硫化物,向熔融的硫中通入氯气即可生成
,遇水会发生化学反应。二氯化二硫具有很高的化学反应活性,能被金属还原生成氯化物和硫化物,向熔融的硫中通入氯气即可生成 。实验室用S和
。实验室用S和 制备
制备 的装置如图(部分夹持装置已略去)。
的装置如图(部分夹持装置已略去)。
回答下列问题:
(1)装置b用于吸收
 ,则溶液1为
,则溶液1为(2)实验开始时,先点燃a处酒精灯,圆底烧瓶中发生反应的化学方程式为
(3)e中大烧杯装有冰水,作用是

(4)
 (
( 中S为
中S为 价)遇水会生成
价)遇水会生成 、一种强酸和一种淡黄色固体单质,该反应的化学方程式为
、一种强酸和一种淡黄色固体单质,该反应的化学方程式为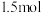 电子,生成的
电子,生成的 在标准状况下的体积为
在标准状况下的体积为 。
。
更新时间:2024-03-01 16:01:20
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】铁是生产、生活及生命中的重要元素。
(1)血红蛋白中的铁元素呈+2价,具有结合O2分子结合成氧合血红蛋白的能力。如果误服亚硝酸盐,会使人中毒,因为二价铁被_______ (填“氧化”或“还原”)。
(2)为防止FeCl2发生氧化反应而变质,存放时应加入_____ (填化学式)。现有一瓶久置的FeCl2溶液,请设计实验检验其中是否含有Fe3+__________________________ 。
(3)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型消毒剂。在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4的离子方程式:__________________________ ;高铁酸钠对水消毒时转化为Fe3+,Fe3+ 净水的有关离子方程式为___________________ 。
(4)球墨铸铁中含有一种铁碳化合物X。实验小组为测定X的组成设计实验如下:
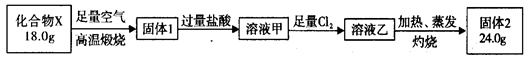
固体2的俗名是________ ,X的化学式可以表示为________ 。
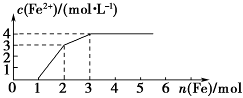
(5)某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度和加入铁粉的物质的量之间的关系如图所示。则溶液中Fe(NO3)3、Cu(NO3)2、HNO3的物质的量浓度之比为________ 。
 。
。
(1)血红蛋白中的铁元素呈+2价,具有结合O2分子结合成氧合血红蛋白的能力。如果误服亚硝酸盐,会使人中毒,因为二价铁被
(2)为防止FeCl2发生氧化反应而变质,存放时应加入
(3)高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型消毒剂。在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4的离子方程式:
(4)球墨铸铁中含有一种铁碳化合物X。实验小组为测定X的组成设计实验如下:

固体2的俗名是
(5)某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度和加入铁粉的物质的量之间的关系如图所示。则溶液中Fe(NO3)3、Cu(NO3)2、HNO3的物质的量浓度之比为
 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】三氧化二铬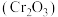 可用作着色剂、分析试剂、催化剂等.一种利用铬铁矿(主要成分为
可用作着色剂、分析试剂、催化剂等.一种利用铬铁矿(主要成分为 ,还含有
,还含有 、
、 等杂质)清洁生产
等杂质)清洁生产 的工艺流程如图:
的工艺流程如图:
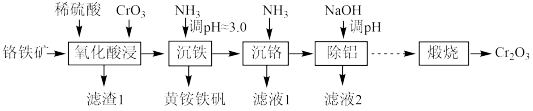
已知:部分离子生成氢氧化物沉淀的
回答下列问题:
(1)“氧化酸浸”时,消耗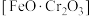 与
与 的物质的量之比为
的物质的量之比为_______
(2)“氧化酸浸”浸出液中含有的阳离子有_______ (用离子符号表示)
(3)“沉铁”时,铁元素以黄铵铁矾沉淀的形式析出,黄铵铁矾的化学式为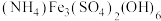 ,则“沉铁”时反应的离子方程式为
,则“沉铁”时反应的离子方程式为_______
(4)“沉铬”时,所得滤液1中所含主要溶质为_______ (用化学式表示)
(5)“除铝”时,需要用 调节溶液的
调节溶液的 的范围应为_______(填字母代号)
的范围应为_______(填字母代号)
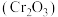 可用作着色剂、分析试剂、催化剂等.一种利用铬铁矿(主要成分为
可用作着色剂、分析试剂、催化剂等.一种利用铬铁矿(主要成分为 ,还含有
,还含有 、
、 等杂质)清洁生产
等杂质)清洁生产 的工艺流程如图:
的工艺流程如图:
已知:部分离子生成氢氧化物沉淀的

| 物质 |  |  |  在 在 时开始溶解, 时开始溶解, 时溶解完全。 时溶解完全。 是两性氢氧化物, 是两性氢氧化物, 在 在 开始溶解. 开始溶解. |
| 开始沉淀 | 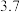 | 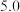 | |
| 完全沉淀 | 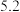 | 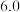 |
回答下列问题:
(1)“氧化酸浸”时,消耗
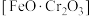 与
与 的物质的量之比为
的物质的量之比为(2)“氧化酸浸”浸出液中含有的阳离子有
(3)“沉铁”时,铁元素以黄铵铁矾沉淀的形式析出,黄铵铁矾的化学式为
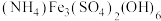 ,则“沉铁”时反应的离子方程式为
,则“沉铁”时反应的离子方程式为(4)“沉铬”时,所得滤液1中所含主要溶质为
(5)“除铝”时,需要用
 调节溶液的
调节溶液的 的范围应为_______(填字母代号)
的范围应为_______(填字母代号)A. | B. | C. | D.稍大于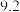 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】化学是一门以实验为基础的科学,其中控制变量思想在探究实验中有重要应用,下列实验对影响化学反应速率的因素进行探究。
实验方案:现有0.0lmol/L酸性KMnO4溶液和0.lmol/L草酸溶液,为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表:
(1)请书写此过程的离子反应方程式:_____________ 。
(2)通过实验①、③可探究草酸的浓度对反应速率的影响,表中Vx=_________ mL,理由是_ 。
(3)对比实验①、②的实验现象是___________________________________ 。
(4)实验①中t min 时溶液褪色,用草酸表示的反应速率v(H2C2O4)=______________ 。
(5)甲同学在研究草酸与高锰酸钾在酸性条件下反应的影响因素时发现,草酸与酸性高锰酸钾溶液开始一段时间反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。针对上述现象,甲同学认为草酸与高锰酸钾反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是________________ 的影响。
实验方案:现有0.0lmol/L酸性KMnO4溶液和0.lmol/L草酸溶液,为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验 序号 | 体积V/mL | 温度/℃ | ||
| KMnO4 溶液 | 水 | H2C2O4溶液 | ||
| ① | 4.0 | 0.0 | 2.0 | 25 |
| ② | 4.0 | 0.0 | 2.0 | 60 |
| ③ | 4.0 | Vx | 1.0 | 25 |
(2)通过实验①、③可探究草酸的浓度对反应速率的影响,表中Vx=
(3)对比实验①、②的实验现象是
(4)实验①中t min 时溶液褪色,用草酸表示的反应速率v(H2C2O4)=
(5)甲同学在研究草酸与高锰酸钾在酸性条件下反应的影响因素时发现,草酸与酸性高锰酸钾溶液开始一段时间反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。针对上述现象,甲同学认为草酸与高锰酸钾反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组设计了如图装置,该装置能制取Cl2,并进行相关性质实验,且可利用装置G储存多余的氯气。

(1)连接好仪器后首先应进行的操作是_______ 。A中发生反应的化学方程式为_______ 。
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①在装置D中能看到的实验现象是_______ 。
②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为_______ 。
③装置F中球形干燥管的作用是_______ 。
(3)储气瓶b内盛放的试剂是_______ 。
(4)装置C中发生反应的离子方程式为_______ 。

(1)连接好仪器后首先应进行的操作是
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①在装置D中能看到的实验现象是
②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为
③装置F中球形干燥管的作用是
(3)储气瓶b内盛放的试剂是
(4)装置C中发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】下图是一个制取氯气并以氯气为原料进行某个特定反应研究的装置。
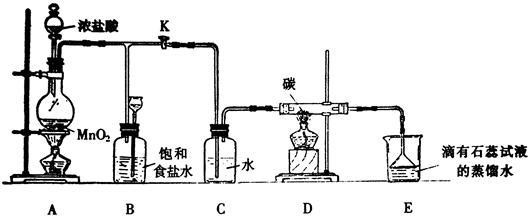
(1)实验开始时,先点燃A处的酒精灯,打开K,使Cl2充满整个装置,再点燃D处酒精灯,然后连接上E装置;E处石蕊试液先变红然后渐变为无色,同时漏斗中的液面略有上升,则产生颜色变化的原因是________________
a.反应中产生CO2的缘故 b.反应中产生HCl的缘故
c.反应中产生HCl并有Cl2溶于水 d.反应中同时有CO2、HCl产生的缘故
D处反应的化学方程式为______________________ 。
(2)装置C的作用是___________________________ 。
(3)若将E处中的液体改为澄清石灰水,反应过程中的现象为__________ 。
a.有白色沉淀产生 b.先生成白色沉淀而后沉淀消失
c.无明显现象 d.开始无沉淀,然后产生白色沉淀
(4)当反应结束后关闭K,移去A处酒精灯,由于余热作用,A处仍有Cl2产生,此时B中现象为________________ ,B的作用是_______________ 。
(5)E装置无法确认D处反应中有CO2产生,为了证明CO2的存在,要对E装置进行改变,下列装置符合要求的是_________ 。
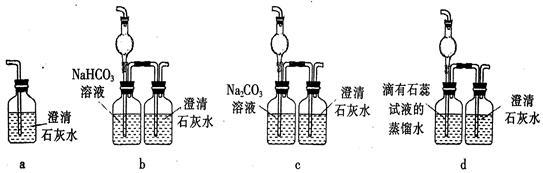
(6)本实验的目的是________________________ 。

(1)实验开始时,先点燃A处的酒精灯,打开K,使Cl2充满整个装置,再点燃D处酒精灯,然后连接上E装置;E处石蕊试液先变红然后渐变为无色,同时漏斗中的液面略有上升,则产生颜色变化的原因是
a.反应中产生CO2的缘故 b.反应中产生HCl的缘故
c.反应中产生HCl并有Cl2溶于水 d.反应中同时有CO2、HCl产生的缘故
D处反应的化学方程式为
(2)装置C的作用是
(3)若将E处中的液体改为澄清石灰水,反应过程中的现象为
a.有白色沉淀产生 b.先生成白色沉淀而后沉淀消失
c.无明显现象 d.开始无沉淀,然后产生白色沉淀
(4)当反应结束后关闭K,移去A处酒精灯,由于余热作用,A处仍有Cl2产生,此时B中现象为
(5)E装置无法确认D处反应中有CO2产生,为了证明CO2的存在,要对E装置进行改变,下列装置符合要求的是

(6)本实验的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。有关物质的部分性质如下表:
实验室用干燥而纯净的二氧化硫和氯气合成硫酰氯,反应的热化学方程式为:SO2(g)+Cl2(g) SO2Cl2(l)△H=-97.3 kJ· mol-1
SO2Cl2(l)△H=-97.3 kJ· mol-1
反应装置如图所示(夹持仪器已省略),请回答有关问题:
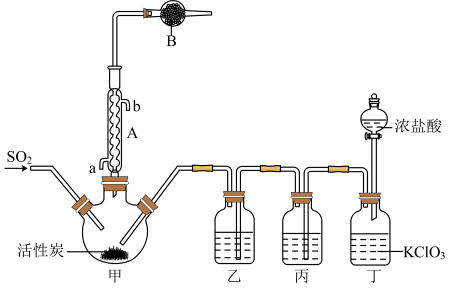
(1)仪器B的名称为________ ;
(2)仪器A的作用是_______ ;
(3)装置乙中盛放的试剂为______ ,在实验室用氢氧化钠溶液吸收多余硫酰氯的离子反应方程式为______ ;
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有_______ (填序号);
①先通冷凝水,再通气体②控制气流速率,宜慢不宜快
③若三颈烧瓶发烫,可适当降温④加热三颈烧瓶
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H=H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸。
①分解产物中分离出硫酰氯的实验操作名称为____ 。
②某同学为检验硫酰氯产品中是否混有硫酸设计实验如下:取少量产品溶于水,加入盐酸酸化的氯化钡溶液,振荡,观察到有白色沉淀生成,则认为产品中含有硫酸。该同学的结论是否正确,请说明理由____ 。
| 物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
| SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾 ②100℃以上易分解SO2和Cl2 |
| H2SO4 | 10.4 | 338 | 具有吸水性且难分解 |
 SO2Cl2(l)△H=-97.3 kJ· mol-1
SO2Cl2(l)△H=-97.3 kJ· mol-1反应装置如图所示(夹持仪器已省略),请回答有关问题:

(1)仪器B的名称为
(2)仪器A的作用是
(3)装置乙中盛放的试剂为
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有
①先通冷凝水,再通气体②控制气流速率,宜慢不宜快
③若三颈烧瓶发烫,可适当降温④加热三颈烧瓶
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H=H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸。
①分解产物中分离出硫酰氯的实验操作名称为
②某同学为检验硫酰氯产品中是否混有硫酸设计实验如下:取少量产品溶于水,加入盐酸酸化的氯化钡溶液,振荡,观察到有白色沉淀生成,则认为产品中含有硫酸。该同学的结论是否正确,请说明理由
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】钼是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强 合金的强度、硬度、可焊性及韧性,还可增强其耐高温及耐腐蚀性能。如图是化工生产中 制备金属钼的主要流程图。
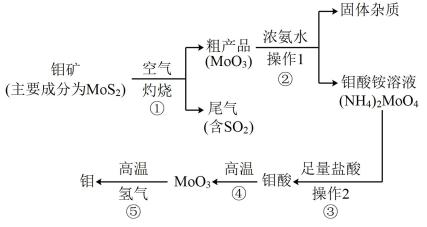
(1)写出在高温下发生反应①的化学方程_________________________________________
(2)生产中用足量的浓氨水吸收反应①的尾气合成肥料,写出该反应的离子方程式:______________________________
(3)如果在实验室模拟操作 1 和操作 2,则需要使用的主要玻璃仪器有______________________________
(4)某同学利用下图所示装置来制备氢气,利用氢气还原三氧化钼,根据要求回答问题:

① 请设计一个实验方案验证 H2的还原性并检验其氧化产物,其装置连接顺序是______________________________
② 在烧瓶 A 中加入少量硫酸铜的目的是_____
③ 两次使用 D 装置,其中所盛的药品依次是_____ 、_____

(1)写出在高温下发生反应①的化学方程
(2)生产中用足量的浓氨水吸收反应①的尾气合成肥料,写出该反应的离子方程式:
(3)如果在实验室模拟操作 1 和操作 2,则需要使用的主要玻璃仪器有
(4)某同学利用下图所示装置来制备氢气,利用氢气还原三氧化钼,根据要求回答问题:

① 请设计一个实验方案验证 H2的还原性并检验其氧化产物,其装置连接顺序是
② 在烧瓶 A 中加入少量硫酸铜的目的是
③ 两次使用 D 装置,其中所盛的药品依次是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上生产高氯酸时,还同时生产了一种常见的重要合氯消毒剂和漂白剂亚氯酸钠(NaClO2),工艺流程如下:
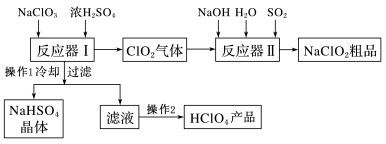
已知:a. NaHSO4的溶解度随着温度的升高而增大,适当条件下可结晶析出;
b.高氯酸是至今为止人们已知酸中的最强酸,沸点:90℃。
(1)操作①冷却过滤的目的是__________________
(2)反应器I中发生化学反应的方程式是_________________ ,反应器I中的温度最佳为__________ (填序号);操作②的名称为______________ 。
A.0℃ B. 20℃ C. 80℃ D. 120℃
(3)反应器II中发生反应的离子方程式为_________ ;SO2的作用为_______________ (氧化剂、还原剂)。
(4)加快反应器II中反应速率的措施有___________ (写出2种措施即可)等。从反应器II中获得NaClO2粗品的实验操作依次是______________ (选序号,下同),进一步提纯的操作名称为______________
A.过滤 B.重结晶 C.蒸馏 D.蒸发浓缩 E.蒸干灼烧 F.冷却结晶

已知:a. NaHSO4的溶解度随着温度的升高而增大,适当条件下可结晶析出;
b.高氯酸是至今为止人们已知酸中的最强酸,沸点:90℃。
(1)操作①冷却过滤的目的是
(2)反应器I中发生化学反应的方程式是
A.0℃ B. 20℃ C. 80℃ D. 120℃
(3)反应器II中发生反应的离子方程式为
(4)加快反应器II中反应速率的措施有
A.过滤 B.重结晶 C.蒸馏 D.蒸发浓缩 E.蒸干灼烧 F.冷却结晶
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铁红(Fe2O3)常用于油漆、油墨及橡胶工业。工业上以一定质量的硫铁矿烧渣(主要成分为Fe2O3、Fe3O4,另含少量难溶杂质)为主要原料制备铁红的一种工艺流程如下:
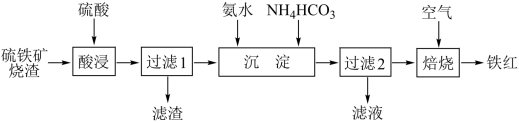
已知:某些过渡元素(如Cu、Fe、Ag等)的离子能与NH3、H2O、OH-、SCN-等形成可溶性配合物。
(1) 工业常将硫铁矿烧渣经过粉碎后再进行“酸浸”,其目的是________ 。
(2) “酸浸”时加入的硫酸不宜过量太多的原因是________ 。
(3) “过滤1”所得滤液中含有的阳离子有________ 。
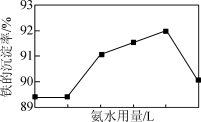
(4) “沉淀”过程中,控制NH4HCO3用量不变,铁的沉淀率随氨水用量变化如右图所示。当氨水用量超过一定体积时,铁的沉淀率下降。其可能的原因是________ 。
(5) “过滤2”所得滤渣的主要成分为FeOOH和FeCO3,所得滤液中的主要溶质是________ (填化学式)。
(6) 写出FeCO3在空气中焙烧生成铁红的化学方程式:________ 。

已知:某些过渡元素(如Cu、Fe、Ag等)的离子能与NH3、H2O、OH-、SCN-等形成可溶性配合物。
(1) 工业常将硫铁矿烧渣经过粉碎后再进行“酸浸”,其目的是

(2) “酸浸”时加入的硫酸不宜过量太多的原因是
(3) “过滤1”所得滤液中含有的阳离子有
(4) “沉淀”过程中,控制NH4HCO3用量不变,铁的沉淀率随氨水用量变化如右图所示。当氨水用量超过一定体积时,铁的沉淀率下降。其可能的原因是
(5) “过滤2”所得滤渣的主要成分为FeOOH和FeCO3,所得滤液中的主要溶质是
(6) 写出FeCO3在空气中焙烧生成铁红的化学方程式:
您最近一年使用:0次



