室温下,两种难溶盐 (白色)、
(白色)、 (砖红色)的离子浓度关系曲线如图所示,其中
(砖红色)的离子浓度关系曲线如图所示,其中 。
。
下列说法错误的是
 (白色)、
(白色)、 (砖红色)的离子浓度关系曲线如图所示,其中
(砖红色)的离子浓度关系曲线如图所示,其中 。
。
下列说法错误的是
A. |
B.向 点的混合溶液中,加入硝酸银固体, 点的混合溶液中,加入硝酸银固体, 变小 变小 |
| C.B点条件下能生成白色沉淀,不能生成砖红色沉淀 |
D.向等浓度的 和 和 混合溶液中滴加 混合溶液中滴加 溶液,先产生白色沉淀 溶液,先产生白色沉淀 |
更新时间:2024-03-02 09:35:31
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】下列指定反应的离子方程式正确的是
A.Cl2与热的NaOH溶液反应制取NaClO3: |
B.澄清石灰水与硬水中Mg(HCO3)2反应: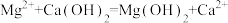 |
C.[Ag(NH3)2]OH与足量盐酸反应生成AgCl: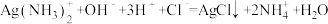 |
D.向FeSO4溶液中滴加碱性NaBH4溶液,生成纳米铁粉、H2和 : :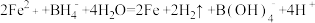 |
您最近一年使用:0次
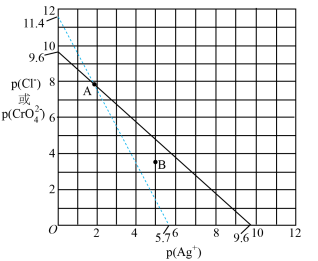
【推荐2】某温度下,饱和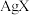 和
和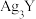 溶液,
溶液,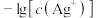 与
与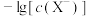 、
、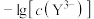 的关系如图所示,
的关系如图所示, 为两线段的交点。下列说法错误的是
为两线段的交点。下列说法错误的是
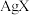 和
和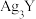 溶液,
溶液,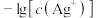 与
与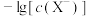 、
、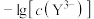 的关系如图所示,
的关系如图所示, 为两线段的交点。下列说法错误的是
为两线段的交点。下列说法错误的是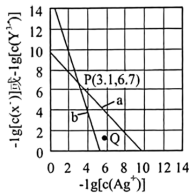
A.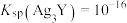 |
| B.图中a代表AgX溶液 |
C.Q点所对应AgX生成沉淀,而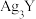 不生成沉淀 不生成沉淀 |
D.向NaX、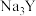 均为 均为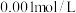 混合溶液中滴加 混合溶液中滴加 溶液,先产生 溶液,先产生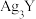 沉淀 沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】工业上以精炼铜的阳极泥为原料(主要成分为Se、CuSe、 等)回收Se。
等)回收Se。 和
和 ,被水吸收时发生反应。
,被水吸收时发生反应。
②Se难溶于水,沸点684.9℃,易与 反应。
反应。
③反应的 ,代表可完全转化。室温下
,代表可完全转化。室温下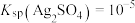 ,
,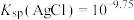 。
。
下列说法正确的是
 等)回收Se。
等)回收Se。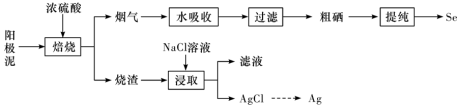
 和
和 ,被水吸收时发生反应。
,被水吸收时发生反应。②Se难溶于水,沸点684.9℃,易与
 反应。
反应。③反应的
 ,代表可完全转化。室温下
,代表可完全转化。室温下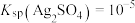 ,
,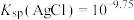 。
。下列说法正确的是
A.理论上,发生反应的 和 和 的物质的量之比为1∶2 的物质的量之比为1∶2 |
| B.在真空中可进行粗硒提纯,可降低体系中硒的沸点 |
C.“滤液”为 溶液 溶液 |
D.加入NaCl溶液浸取时发生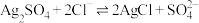 ,该反应过程不可完全转化 ,该反应过程不可完全转化 |
您最近一年使用:0次
单选题
|
较难
(0.4)
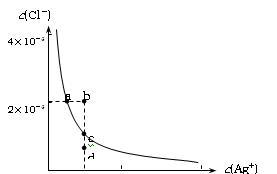
【推荐2】某温度时,AgCl在水中的沉淀溶解平衡曲线如图所示(提示:AgCl(s) Ag+(aq)+Cl-(aq),其平衡常数Ksp=c(Ag+)·c(Cl-),称为溶度积常数;又知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2S)=6.3×10-50)。下列说法正确的是: ( )
Ag+(aq)+Cl-(aq),其平衡常数Ksp=c(Ag+)·c(Cl-),称为溶度积常数;又知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2S)=6.3×10-50)。下列说法正确的是: ( )
 Ag+(aq)+Cl-(aq),其平衡常数Ksp=c(Ag+)·c(Cl-),称为溶度积常数;又知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2S)=6.3×10-50)。下列说法正确的是: ( )
Ag+(aq)+Cl-(aq),其平衡常数Ksp=c(Ag+)·c(Cl-),称为溶度积常数;又知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2S)=6.3×10-50)。下列说法正确的是: ( )
| A.加入NaCl可以使溶液由a点变到b点 |
| B.b点和d点均无AgCl沉淀生成 |
| C.a点对应的Ksp大于c点对应的Ksp |
D.向0.1mol/L的硝酸银溶液中滴加0.1mol/L的NaCl溶液至不再有白色沉淀生成,再向其中滴加0.1mol/L的Na2S溶液,白色沉淀转化为黑色沉淀。其沉淀转化的反应方程式为:2AgCl(s)+S2-(aq) Ag2S(s)+2Cl-(aq) 。 Ag2S(s)+2Cl-(aq) 。 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项| | 实验操作和现象 | 实验结论 |
| A | 向KI溶液中滴加几滴NaNO2溶液,再滴加淀粉溶液后变蓝色 | NO2-的氧化性比I2的强 |
| B | 向麦芽糖样品溶液X中加入银氨溶液,水浴加热,产生银镜 | X中麦芽糖已发生水解 |
| C | 用pH计测得浓度均为0.01mol/L的苯酚钠溶液、Na2CO3溶液的pH依次为10.9、11.1 | 苯酚的酸性比碳酸的强 |
| D | 常温时,向0.1mol/LNa2CrO4溶液中滴入AgNO3溶液至不再有红棕色沉淀(Ag2CrO4),再滴加0.1mol/LNaCl溶液,沉淀逐渐转变为白色 | Ksp(AgCI)<Ksp(Ag2CrO4) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】秦俑彩绘中含有铅白 和黄色的
和黄色的 。常温下,
。常温下, 和黄色的
和黄色的 在不同溶液中分别达到溶解平衡时pM(阳离子浓度的负对数)与pR(阴离子浓度的负对数)的关系如图所示。下列说法正确的是
在不同溶液中分别达到溶解平衡时pM(阳离子浓度的负对数)与pR(阴离子浓度的负对数)的关系如图所示。下列说法正确的是
 和黄色的
和黄色的 。常温下,
。常温下, 和黄色的
和黄色的 在不同溶液中分别达到溶解平衡时pM(阳离子浓度的负对数)与pR(阴离子浓度的负对数)的关系如图所示。下列说法正确的是
在不同溶液中分别达到溶解平衡时pM(阳离子浓度的负对数)与pR(阴离子浓度的负对数)的关系如图所示。下列说法正确的是
A. 表示 表示 达到沉淀溶解平衡时pM与pR的关系 达到沉淀溶解平衡时pM与pR的关系 |
B.在1mol/L的KI溶液中, 的溶解度为 的溶解度为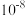 mol/L mol/L |
C.对于分散质 ,X点: ,X点: |
D.向浓度均为0.lmol/L的 、NaI的混合溶液中滴入 、NaI的混合溶液中滴入 溶液,先产生黄色沉淀 溶液,先产生黄色沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下表是25℃时五种物质的溶度积常数,下列有关说法错误的是
| 化学式 |  |  | CuS |  |  |
| 溶度积 | 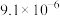 | 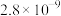 |  | 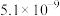 | 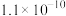 |
A.根据表中数据可推知,常温下 在纯水中的溶解度比 在纯水中的溶解度比 的大 的大 |
B.向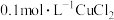 溶液中通入 溶液中通入 可生成CuS沉淀,是因为 可生成CuS沉淀,是因为 |
| C.根据表中数据可推知,向硫酸钡沉淀中加入饱和碳酸钠溶液,不可能有碳酸钡生成 |
D.常温下, 在 在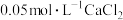 溶液中比在 溶液中比在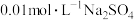 溶液中的溶解度小 溶液中的溶解度小 |
您最近一年使用:0次
【推荐3】25℃时,向2.5L蒸馏水中加入0.05molBaSO4固体粉末,再逐渐加入一定量的Na2CO3固体粉末,边加边搅拌(忽略溶液体积变化)。溶液中部分离子的浓度变化如图所示。下列说法正确的是
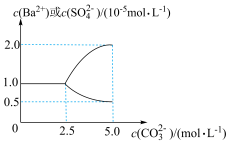

| A.25℃时,Ksp(BaCO3)<Ksp(BaSO4) |
| B.BaSO4在水中的Ksp大于其在BaCl2溶液中的Ksp |
| C.加入1.3molNa2CO3,即可使BaSO4全部转化为BaCO3 |
D.当BaSO4恰好全部转化为BaCO3时,c( )>c(Ba2+)>c( )>c(Ba2+)>c( )>c(OH-) )>c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
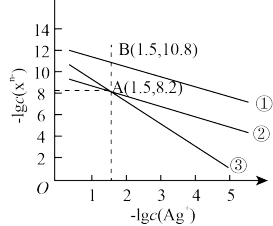
【推荐1】常温下,保持某含少量CaCO3浊液的水体中H2CO3与空气中CO2的平衡,调节水体pH,水体中lgc(X)(X为H2CO3、HCO 、CO
、CO 、Ca2+)与pH的关系如图所示。已知Ksp(CaCO3)=2.8×10-9,下列说法错误的是
、Ca2+)与pH的关系如图所示。已知Ksp(CaCO3)=2.8×10-9,下列说法错误的是
 、CO
、CO 、Ca2+)与pH的关系如图所示。已知Ksp(CaCO3)=2.8×10-9,下列说法错误的是
、Ca2+)与pH的关系如图所示。已知Ksp(CaCO3)=2.8×10-9,下列说法错误的是
A.①代表lgc(HCO )与pH的关系 )与pH的关系 |
B.a点的水体中:c(Ca2+)>c(HCO )>c(CO )>c(CO ) ) |
| C.pH=10.3时,c(Ca2+)=2.8×10-7.9mol·L-1 |
| D.向水体中加入适量Ca(OH)2固体,可使溶液由b点变到c点 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知25℃时,AgI饱和溶液中c(Ag+)为1.22×10﹣8 mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10﹣5 mol/L。若在10mL含有KCl和KI各为0.01mol/L的溶液中,加入16mL 0.01mol/L AgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是( )
| A.c(K+)>c(NO3﹣)>c(Ag+)>c(Cl﹣)>c(I﹣) |
| B.c(K+)>c(NO3﹣)>c(Cl﹣)>c(Ag+)>c(I﹣) |
| C.c(K+)>c(NO3﹣)>c(Ag+)=c(Cl﹣)+c(I﹣) |
| D.c(NO3﹣)>c(K+)>c(Ag+)>c(Cl﹣)>c(I﹣) |
您最近一年使用:0次

 转化为极难溶的
转化为极难溶的 沉淀是化学实验室中进行物质分离、除杂常用的方法,涉及反应为
沉淀是化学实验室中进行物质分离、除杂常用的方法,涉及反应为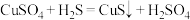 。已知25℃时,下列过程的平衡常数:
。已知25℃时,下列过程的平衡常数: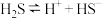





 ,该反应能彻底进行
,该反应能彻底进行 溶液呈碱性
溶液呈碱性 的
的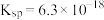 ,因此除去工业废水中
,因此除去工业废水中