工业上以精炼铜的阳极泥为原料(主要成分为Se、CuSe、 等)回收Se。
等)回收Se。 和
和 ,被水吸收时发生反应。
,被水吸收时发生反应。
②Se难溶于水,沸点684.9℃,易与 反应。
反应。
③反应的 ,代表可完全转化。室温下
,代表可完全转化。室温下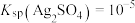 ,
,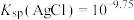 。
。
下列说法正确的是
 等)回收Se。
等)回收Se。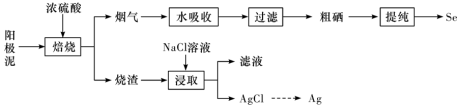
 和
和 ,被水吸收时发生反应。
,被水吸收时发生反应。②Se难溶于水,沸点684.9℃,易与
 反应。
反应。③反应的
 ,代表可完全转化。室温下
,代表可完全转化。室温下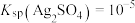 ,
,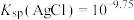 。
。下列说法正确的是
A.理论上,发生反应的 和 和 的物质的量之比为1∶2 的物质的量之比为1∶2 |
| B.在真空中可进行粗硒提纯,可降低体系中硒的沸点 |
C.“滤液”为 溶液 溶液 |
D.加入NaCl溶液浸取时发生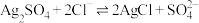 ,该反应过程不可完全转化 ,该反应过程不可完全转化 |
更新时间:2024-05-19 08:41:45
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】铟(In)是一种稀有贵金属,广泛应用于航空航天、太阳能电池等高科技领域。从铜烟灰酸浸渣(主要含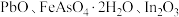 )中提取铟的工艺流程如图:
)中提取铟的工艺流程如图:
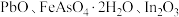 )中提取铟的工艺流程如图:
)中提取铟的工艺流程如图:
| A.整个流程中可循环利用的物质是萃余液 |
| B.亚铁离子在萃取剂中的溶解度大于水中的溶解度 |
C.“水浸”所得浸渣中还含有 |
D.“还原铁”时发生反应的离子方程式为: |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法正确的是
MnCl2+Cl2↑+2H2O。实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法正确的是
 MnCl2+Cl2↑+2H2O。实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法正确的是
MnCl2+Cl2↑+2H2O。实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法正确的是| A.若产物为NaClO、NaCl,则吸收后的溶液中n(ClO-)=n(Cl-) |
| B.若产物为NaClO3、NaCl,则参加反应的氧化剂和还原剂的物质的量之比为1∶5 |
| C.若产物为NaClO、NaClO3、NaCl,则由吸收后的溶液中n(Cl-)和n(ClO-)可计算吸收的n(Cl2) |
| D.若产物为NaClO、NaClO3、NaCl,则NaOH与Cl2相互反应的物质的量之比为2∶1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】下列实验操作对应的图像不正确的是
| 选项 | A | B | C | D |
| 实验操作 | 向MgCl2、AlCl3溶液中(各1 mol),逐滴加入NaOH溶液 | 向HCl、MgCl2、AlCl3、NH4Cl溶液中(各1 mol),逐滴加入NaOH溶液 | 向NaOH、NaAlO2溶液中(各1 mol),逐滴加入HCl溶液 | 向NaOH、Na2CO3混合溶液中(各1 mol)滴加稀盐酸 |
| 图像 |  |  | 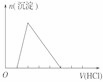 | 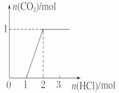 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】工业上以 为原料生产
为原料生产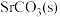 ,对其工艺条件进行研究.现有含
,对其工艺条件进行研究.现有含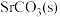 的
的 溶液和含
溶液和含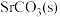 的
的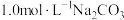 溶液,以及含
溶液,以及含 的
的 溶液和含
溶液和含 的
的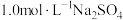 溶液.在一定pH范围内(固体足量),四种溶液中
溶液.在一定pH范围内(固体足量),四种溶液中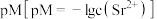 随pH的变化关系如图所示.下列说法错误的是
随pH的变化关系如图所示.下列说法错误的是
 为原料生产
为原料生产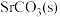 ,对其工艺条件进行研究.现有含
,对其工艺条件进行研究.现有含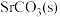 的
的 溶液和含
溶液和含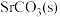 的
的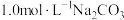 溶液,以及含
溶液,以及含 的
的 溶液和含
溶液和含 的
的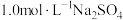 溶液.在一定pH范围内(固体足量),四种溶液中
溶液.在一定pH范围内(固体足量),四种溶液中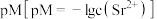 随pH的变化关系如图所示.下列说法错误的是
随pH的变化关系如图所示.下列说法错误的是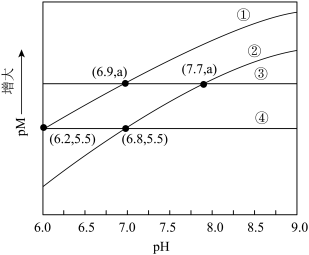
A.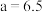 |
B.由图可知,pH越小,越不利于 转化为 转化为 |
C.曲线①代表含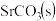 的 的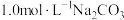 溶液的变化曲线 溶液的变化曲线 |
D.将 状态下的②、④两物料等体积混合后,溶液中pM等于5.5 状态下的②、④两物料等体积混合后,溶液中pM等于5.5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】下列实验中,对应的现象以及解释或结论都正确且有因果关系的是
| 选项 | 操作 | 现象 | 解释或结论 |
| A | 常温下,用pH计分别测定饱和溶液NaA和饱和溶液NaB的pH | pH:NaA>NaB | 常温下酸性:HA<HB |
| B | 向含有ZnS和Na2S的悬浊液中滴加CuSO4溶液 | 生成黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
| C | 向注射器中吸入NO2,针尖堵封针尖处,将注射器体积压缩为原来的一半 | 气体颜色比起始浅 | 加压后,NO2转变为无色的N2O4 |
| D | 用石墨做电极电解Mg(NO3)2,Cu(NO3)2的混合溶液 | 阴极上先析出铜 | 金属活动性:Mg>Cu |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐1】自然界原生铜硫化合物经氧化、淋滤后变成 CuSO4溶液,遇到闪锌矿(ZnS)可慢慢转变为铜蓝(CuS)。已知: 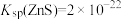 ,
,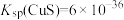 。下列说法正确的是
。下列说法正确的是
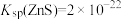 ,
,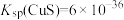 。下列说法正确的是
。下列说法正确的是| A.基态 Cu 核外电子排布式为[Ar]3d94s2 |
B.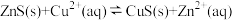 正向进行,需满足 正向进行,需满足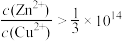 |
C.CuSO4溶液遇 ZnS 后生成 CuS 后的溶液中存在: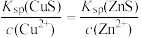 |
| D.将 CuS 固体加入无色饱和硫酸锌溶液(约 3 mol/L)中,溶液会变蓝色 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】常温下,向含有 、
、 、
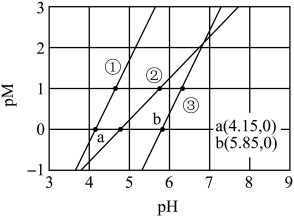
、 的工业废水中逐滴加入NaOH溶液,pM随pH的变化关系如图所示[pM表示
的工业废水中逐滴加入NaOH溶液,pM随pH的变化关系如图所示[pM表示 或
或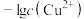 或
或 ]。
]。
已知: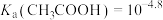 ,
,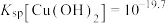 。若溶液中离子浓度小于
。若溶液中离子浓度小于 ,认为该离子沉淀完全。下列说法不正确的是
,认为该离子沉淀完全。下列说法不正确的是
 、
、 、
、 的工业废水中逐滴加入NaOH溶液,pM随pH的变化关系如图所示[pM表示
的工业废水中逐滴加入NaOH溶液,pM随pH的变化关系如图所示[pM表示 或
或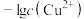 或
或 ]。
]。已知:
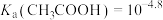 ,
,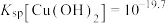 。若溶液中离子浓度小于
。若溶液中离子浓度小于 ,认为该离子沉淀完全。下列说法不正确的是
,认为该离子沉淀完全。下列说法不正确的是
A.曲线①表示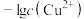 与pH的关系 与pH的关系 |
B. 时,溶液中 时,溶液中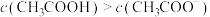 |
C. 时,可认为 时,可认为 沉淀完全 沉淀完全 |
D. 时, 时,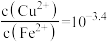 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】湿法提银工艺中,浸出的Ag+需加入Cl-进行沉淀。Ag+与Cl-可结合生成多种络合物,在水溶液中存在如下平衡:AgCl43-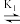 AgCl32-
AgCl32-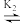 AgCl2-
AgCl2-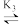 AgCl
AgCl Ag+。25℃时,平衡体系中含Ag微粒的分布系数δ随lgc(Cl-)的变化曲线如图所示。下列说法错误的是
Ag+。25℃时,平衡体系中含Ag微粒的分布系数δ随lgc(Cl-)的变化曲线如图所示。下列说法错误的是

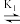 AgCl32-
AgCl32-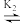 AgCl2-
AgCl2-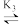 AgCl
AgCl Ag+。25℃时,平衡体系中含Ag微粒的分布系数δ随lgc(Cl-)的变化曲线如图所示。下列说法错误的是
Ag+。25℃时,平衡体系中含Ag微粒的分布系数δ随lgc(Cl-)的变化曲线如图所示。下列说法错误的是
| A.25℃时,Ksp(AgCl)=10-5.08 |
B.曲线c表示AgCl |
C.当c(Cl-)=10-2mol·L-1时,溶液中(AgCl )>c(Ag+)>c(AgCl )>c(Ag+)>c(AgCl ) ) |
| D.25℃时,平衡常数K2=10-0.2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】以某冶金工业产生的废渣(含Cr2O3、SiO2及少量的Al2O3)为原料,根据下列流程可制备K2Cr2O7。
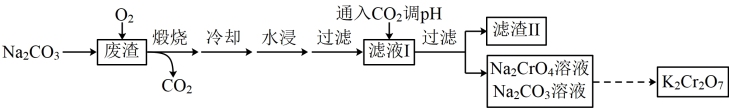
下列说法正确的是

下列说法正确的是
| A.煅烧时没有发生氧化还原反应 |
| B.滤渣Ⅱ中主要成分是Al(OH)3 |
| C.可循环使用的物质是CO2和Na2CO3 |
| D.由Na2CrO4转化为K2Cr2O7的过程中需加入KOH |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】Cr2O3可用作有机合成的催化剂,某课题组以铬铁矿为主要原料制备Cr2O3.铬铁矿主要成分为Fe(CrO2)2,还含有Al2O3、SiO2等杂质,工艺流程如图所示。
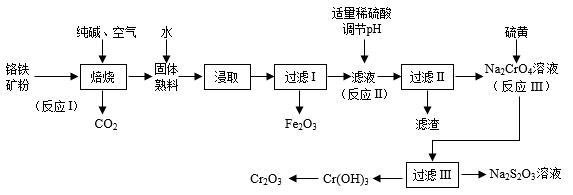
下列说法正确的是

下列说法正确的是
| A.图中“滤渣”成分只有Al(OH)3 |
| B.“焙烧”时,1 mol Fe(CrO2)2参与反应,转移电子数为NA |
C.“反应Ⅲ”的离子方程式为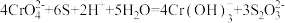 |
| D.用224 kg铬铁矿粉(含80%的Fe(CrO2)2)制备Cr2O3,若产率为75%,则最终可以制得产品91.2 kg |
您最近一年使用:0次


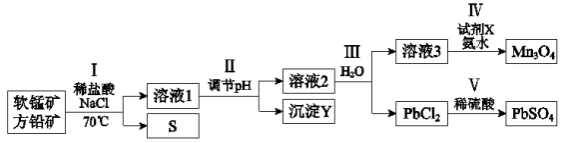

 。下列说法正确的是
。下列说法正确的是 = PbSO4
= PbSO4

