化学实验是研究物质组成和探究物质性质的重要途径。
Ⅰ.某澄清透明溶液(忽略水的电离),可能含有Fe3+、Mg2+、K+、CO 、SO
、SO 、Ba2+、MnO
、Ba2+、MnO 等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示。请你根据上述实验推断:
等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示。请你根据上述实验推断:
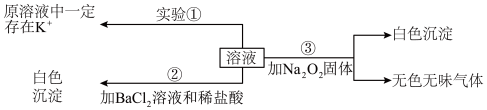
(1)实验①的焰色试验,需要透过_______ ,来观察火焰的颜色。
(2)取100mL溶液进行实验②,经足量盐酸洗涤、干燥后,得沉淀质量为2.33g。该溶液中K+的物质的量浓度为________ 。
(3)实验③产生的无色无味气体为________ ,白色沉淀为_______ (填物质化学式)。原溶液中一定存在的离子有_______ 。
(4)向该溶液中加入硫酸酸化,再通入SO2气体,发生反应使该溶液的颜色发生变化,写出该反应的离子方程式_______ 。
Ⅱ.Na2O2具有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测,Na2O2与H2能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。其中装置A用锌和稀盐酸制取氢气。
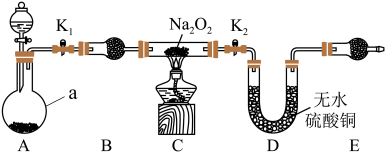
(5)装置B中的试剂是________ 。
(6)下面是实验过程中的重要操作,正确的顺序是_______。
(7)实验过程中观察到淡黄色粉末慢慢变成白色固体,无水硫酸铜未变蓝色。由此可推测出Na2O2与H2反应生成的产物为_______ 。
Ⅰ.某澄清透明溶液(忽略水的电离),可能含有Fe3+、Mg2+、K+、CO
 、SO
、SO 、Ba2+、MnO
、Ba2+、MnO 等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示。请你根据上述实验推断:
等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示。请你根据上述实验推断:
(1)实验①的焰色试验,需要透过
(2)取100mL溶液进行实验②,经足量盐酸洗涤、干燥后,得沉淀质量为2.33g。该溶液中K+的物质的量浓度为
(3)实验③产生的无色无味气体为
(4)向该溶液中加入硫酸酸化,再通入SO2气体,发生反应使该溶液的颜色发生变化,写出该反应的离子方程式
Ⅱ.Na2O2具有强氧化性,H2具有还原性,某同学根据氧化还原反应的知识推测,Na2O2与H2能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。其中装置A用锌和稀盐酸制取氢气。

(5)装置B中的试剂是
(6)下面是实验过程中的重要操作,正确的顺序是_______。
| A.加热至Na2O2逐渐熔化,反应一段时间 | B.用小试管收集气体并检验其纯度 |
| C.打开K1、K2,通入氢气 | D.停止加热,充分冷却,关闭K1、K2 |
(7)实验过程中观察到淡黄色粉末慢慢变成白色固体,无水硫酸铜未变蓝色。由此可推测出Na2O2与H2反应生成的产物为
更新时间:2024-02-12 21:25:04
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】为实现工业含铝、铁、铜合金(假定其余杂质与酸碱都不反应)废料的再利用,某化学兴趣小组设计了如下回收利用方案:
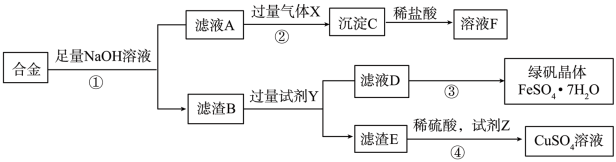
回答下列问题:
(1)合金与NaOH溶液反应的化学方程式为_______ ;操作①为_______ 。
(2)气体X为_______ ;②中发生反应的离子方程式为_______ 。
(3)试剂Y为_______ ,若要从滤液D得到绿矾晶体,步骤③的实验操作有:_______ 、_______ 、过滤、洗涤、干燥。
(4)若试剂Z是H2O2溶液,④中发生反应的化学方程式为_______ 。
(5)为配制240mL0.2mol/L的FeSO4(M=152g/mol)溶液,需称量绿矾晶体质量为_______ g,配制该溶液用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要_______ 、_______ 。下列操作会导致所配溶液浓度偏高的是_______ (填字母)。
A.所称取的晶体失去了部分结晶水 B.转移溶液前容量瓶中存在少量蒸馏水
C.定容前未洗涤烧杯和玻璃棒 D.定容时俯视容量瓶刻度线

回答下列问题:
(1)合金与NaOH溶液反应的化学方程式为
(2)气体X为
(3)试剂Y为
(4)若试剂Z是H2O2溶液,④中发生反应的化学方程式为
(5)为配制240mL0.2mol/L的FeSO4(M=152g/mol)溶液,需称量绿矾晶体质量为
A.所称取的晶体失去了部分结晶水 B.转移溶液前容量瓶中存在少量蒸馏水
C.定容前未洗涤烧杯和玻璃棒 D.定容时俯视容量瓶刻度线
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】已知A为一种盐,C、D、F、N、O为无色气体,E常温常压下为无色无味的液体,N、
H、L为高中常见的单质,I为常见无氧强酸,M的焰色反应为紫色,反应①常用于气体F的检验。
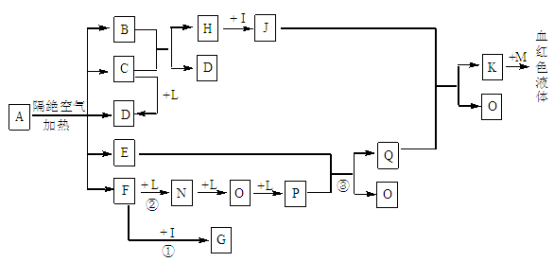
(1)写出D的电子式为_______________ ;
(2)写出反应②的化学方程式:_______________ ;反应③中氧化剂和还原剂的物质的量之比为_________________ ;
(3)将等体积、等浓度的G和F的溶液混合,溶液显碱性,则溶液中离子浓度从大到小的顺序为______ ;
(4)检验J中阳离子的实验方法为_____________________________ ;
(5)已知B中氧元素的质量分数为22.2﹪,且A分解产生的各物质的物质的量之比为n(B):n(C):
n(D):n(E):n(F)=1:2:2:1:2,则A的化学式为__________________________ 。
H、L为高中常见的单质,I为常见无氧强酸,M的焰色反应为紫色,反应①常用于气体F的检验。

(1)写出D的电子式为
(2)写出反应②的化学方程式:
(3)将等体积、等浓度的G和F的溶液混合,溶液显碱性,则溶液中离子浓度从大到小的顺序为
(4)检验J中阳离子的实验方法为
(5)已知B中氧元素的质量分数为22.2﹪,且A分解产生的各物质的物质的量之比为n(B):n(C):
n(D):n(E):n(F)=1:2:2:1:2,则A的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】A~G各物质间的关系如下图,其中B、D为气态单质。
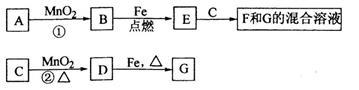
请回答下列问题:
(1)物质C和E的名称分别为________________ 、_______________ ;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为_____________ ;若只能在加热情况下进行,则反应物A应为_____________ ;
(3)反应②的离子方程式为__________________ ;
(4)新配制的F溶液应加入__________________ 以防止其转化为G。检验G溶液中阳离子的常用试剂是_____________ ,实验现象为___________________

请回答下列问题:
(1)物质C和E的名称分别为
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为
(3)反应②的离子方程式为
(4)新配制的F溶液应加入
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,答下列问题:
(1)工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为________________________ ;
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:
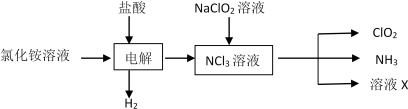
①电解时发生反应的化学方程式为________________________ ;
②设计实验来确定溶液X的成分,请补充完成实验步骤和现象
③除去ClO2中的NH3可选用的试剂是_______ (填标号);
a.水 b.碱石灰 C.浓硫酸 d.饱和食盐水
(3)O2处理过的饮用水会含有一定量的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是_______ 填标号)。
a.明矾b.碘化钾c.盐酸d.硫酸亚铁
(1)工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:

①电解时发生反应的化学方程式为
②设计实验来确定溶液X的成分,请补充完成实验步骤和现象
| 实验步骤 | 实验现象 | 实验结论 |
| I: 取一根铂丝 | 溶液X中含有钠离子 | |
| II: 取少许溶液X于一支试管中,滴加 | 溶液X中含有氯离子 |
a.水 b.碱石灰 C.浓硫酸 d.饱和食盐水
(3)O2处理过的饮用水会含有一定量的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是
a.明矾b.碘化钾c.盐酸d.硫酸亚铁
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】化合物X( )由3种元素组成,某学习小组开展如下探究实验:
)由3种元素组成,某学习小组开展如下探究实验:
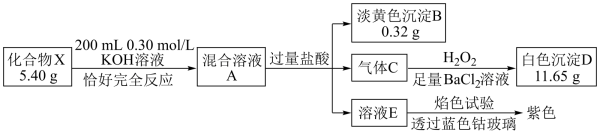
已知:混合溶液A由相对分子质量相差32的甲、乙两种溶质组成;X、甲和乙所含元素完全相同。
请回答:
(1)淡黄色沉淀B的化学式是_______ ,溶液E中所含溶质是_______ (用化学式表示)。
(2)写出气体C生成白色沉淀D的离子方程式_______ 。
(3)写出X与KOH溶液反应的化学方程式_______ 。
(4)实验室常用_______ (填写试剂名称)检验气体C的存在,请写出检验的过程_______ 。
 )由3种元素组成,某学习小组开展如下探究实验:
)由3种元素组成,某学习小组开展如下探究实验:
已知:混合溶液A由相对分子质量相差32的甲、乙两种溶质组成;X、甲和乙所含元素完全相同。
请回答:
(1)淡黄色沉淀B的化学式是
(2)写出气体C生成白色沉淀D的离子方程式
(3)写出X与KOH溶液反应的化学方程式
(4)实验室常用
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】海带中既含有有机碘化合物又含有碘化钠等无机碘化合物。某课题组探究了海带提碘的优化条件,并用色度计测定了某海带样品中碘的含量。实验步骤:
I.预处理:将干海带刷净,剪成 大小的方块,准确称量
大小的方块,准确称量 样品。
样品。
II.灰化:在仪器A中加热干海带,并用玻璃棒不断搅拌,记录加热时间,停止加热,冷却。
III.过滤:将冷却后的海带灰转移到 烧杯中,加入
烧杯中,加入 蒸馏水,静置后过滤。
蒸馏水,静置后过滤。
IV.氧化:向滤液中加入稀 和
和 溶液,充分反应后将滤液转移到分液漏斗中。
溶液,充分反应后将滤液转移到分液漏斗中。
V.萃取:向分液漏斗中加入 ,振荡,静置。待溶液完全分层后,取下层溶液。
,振荡,静置。待溶液完全分层后,取下层溶液。
VI.含量测定:用色度计测定出所得溶液中碘的含量。
VII.回收处理:蒸馏碘的 溶液,回收
溶液,回收
已知:海带灰化后,碘元素以 的形式存在。
的形式存在。
回答下列问题:
(1)第II步中的仪器A是___________ 。
(2)证明第III步滤液中存在 的实验方法是
的实验方法是___________ ,实验现象是___________ 。
(3)第IV步氧化过程中发生反应的离子方程式为___________ 。
(4)第V步可得到 的
的 溶液,也可用如下流程从其中回收
溶液,也可用如下流程从其中回收 :
:
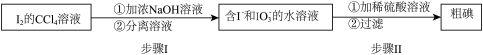
请写出步骤II的离子方程式:___________ 。
(5)碘浓度越大吸光度越大。用色度计测得某碘溶液的吸光度后,利用以溶液吸光度为纵坐标,碘浓度(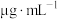 )为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取
)为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取 碘单质,用
碘单质,用 容量瓶配成碘的
容量瓶配成碘的 溶液,取出
溶液,取出 加入一定量
加入一定量 中配得第一份碘的标准溶液
中配得第一份碘的标准溶液 。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是
。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是___________ 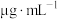 。
。
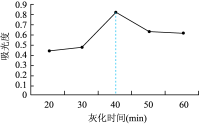
(6)课题组在其他实验条件相同情况下,研究了不同灰化时间对碘提取效果的影响,其结果如图所示。灰化时间超过40min,测得碘的含量逐渐降低,原因是___________ 。
I.预处理:将干海带刷净,剪成
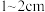 大小的方块,准确称量
大小的方块,准确称量 样品。
样品。II.灰化:在仪器A中加热干海带,并用玻璃棒不断搅拌,记录加热时间,停止加热,冷却。
III.过滤:将冷却后的海带灰转移到
 烧杯中,加入
烧杯中,加入 蒸馏水,静置后过滤。
蒸馏水,静置后过滤。IV.氧化:向滤液中加入稀
 和
和 溶液,充分反应后将滤液转移到分液漏斗中。
溶液,充分反应后将滤液转移到分液漏斗中。V.萃取:向分液漏斗中加入
 ,振荡,静置。待溶液完全分层后,取下层溶液。
,振荡,静置。待溶液完全分层后,取下层溶液。VI.含量测定:用色度计测定出所得溶液中碘的含量。
VII.回收处理:蒸馏碘的
 溶液,回收
溶液,回收
已知:海带灰化后,碘元素以
 的形式存在。
的形式存在。回答下列问题:
(1)第II步中的仪器A是
(2)证明第III步滤液中存在
 的实验方法是
的实验方法是(3)第IV步氧化过程中发生反应的离子方程式为
(4)第V步可得到
 的
的 溶液,也可用如下流程从其中回收
溶液,也可用如下流程从其中回收 :
:
请写出步骤II的离子方程式:
(5)碘浓度越大吸光度越大。用色度计测得某碘溶液的吸光度后,利用以溶液吸光度为纵坐标,碘浓度(
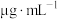 )为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取
)为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取 碘单质,用
碘单质,用 容量瓶配成碘的
容量瓶配成碘的 溶液,取出
溶液,取出 加入一定量
加入一定量 中配得第一份碘的标准溶液
中配得第一份碘的标准溶液 。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是
。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是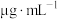 。
。(6)课题组在其他实验条件相同情况下,研究了不同灰化时间对碘提取效果的影响,其结果如图所示。灰化时间超过40min,测得碘的含量逐渐降低,原因是

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】X、Y、Z、W四种化合物均由元素周期表前18号元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。
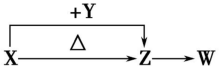
请回答:
(1)W的化学式是__________ 。
(2)X与Y在溶液中反应的离子方程式是__________ 。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置III中生成白色沉淀,装置V中可收集到一种无色气体。
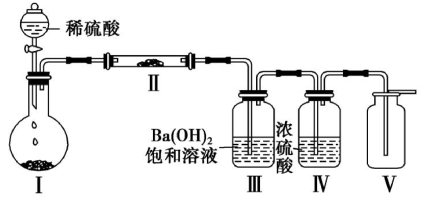
①装置I中反应的化学方程式是__________ 。装置II中物质的化学式是__________ 。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的位置V中气体,该化合物的化学式是__________ ,所需仪器装置是______ (从上图选择必要装置,填写编号)。

请回答:
(1)W的化学式是
(2)X与Y在溶液中反应的离子方程式是
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置III中生成白色沉淀,装置V中可收集到一种无色气体。

①装置I中反应的化学方程式是
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的位置V中气体,该化合物的化学式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】已知A、B、D、E均为中学化学常见单质或化合物,它们之间的转换关系如下图所示(部分产物略去)。
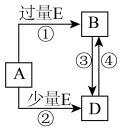
(1)若A为单质,组成A单质的元素是自然界中形成化合物种类最多的元素。
①B属于______ 分子(填“极性”或“非极性”),B分子中所有原子是否都满足8电子结构,____________ (填“是”或“否”)。
②向50 mL 4 mol/L的NaOH溶液中通入1.12 L B(标准状况),反应后溶液中的溶质为_______ (填化学式),物质的量分别为_____________ 。
(2)若A为第三周期中的元素所形成的氯化物。
①写出A溶液→B的离子方程式_________________________________ 。
②写出A和B在溶液中反应的离子方程式_____________________________________ 。
(3)若A为常见的金属,在E的冷、浓溶液中有钝化现象。已知:X为含有非极性键的离子化合物,且1 mol X含有38 mol电子,向D溶液中加入与D等物质的量的固体X,该反应的离子方程式为___________________________________________ 。

(1)若A为单质,组成A单质的元素是自然界中形成化合物种类最多的元素。
①B属于
②向50 mL 4 mol/L的NaOH溶液中通入1.12 L B(标准状况),反应后溶液中的溶质为
(2)若A为第三周期中的元素所形成的氯化物。
①写出A溶液→B的离子方程式
②写出A和B在溶液中反应的离子方程式
(3)若A为常见的金属,在E的冷、浓溶液中有钝化现象。已知:X为含有非极性键的离子化合物,且1 mol X含有38 mol电子,向D溶液中加入与D等物质的量的固体X,该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】A、B、C、D 是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为空气的成分。F 的焰色反应是黄色。在G 中,金属元素与非金属元素的原子个数比为2: 1。在一定条件下,各物质之间的相互转化关系如图(反应条件及部分产物未列出):
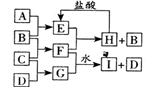
(1)A 的元素符号是______________ ,F的电子式为________________________ 。
(2)E 与F反应的化学方程式:_________________________________________ 。
(3)F 与G 的水溶液反应的离子方程式:______________________________ 。
(4)硫与热浓氢氧化钠溶液反应的离子方程式:__________________________ 。
(5)在加热条件下浓硝酸可把硫单质氧化到最高价产物,写出反应的化学方程式:___________ 。

(1)A 的元素符号是
(2)E 与F反应的化学方程式:
(3)F 与G 的水溶液反应的离子方程式:
(4)硫与热浓氢氧化钠溶液反应的离子方程式:
(5)在加热条件下浓硝酸可把硫单质氧化到最高价产物,写出反应的化学方程式:
您最近一年使用:0次



