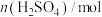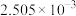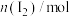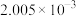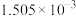氯化铬( )是一种化工原料,可用于催化剂、颜料、印染、陶瓷、电镀等行业。实验室利用铬酸钡(
)是一种化工原料,可用于催化剂、颜料、印染、陶瓷、电镀等行业。实验室利用铬酸钡( )可制备少量氯化铬:
)可制备少量氯化铬:

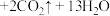 。回答下列问题:
。回答下列问题:
(1)上述反应中,还原剂是_________ ,还原产物与氧化产物的物质的量之比是________ 。
(2)该制备操作方法中,需加稍过量的乙醇,目的是________ 。
(3)制备的氯化铬粗样品利用下列滴定方法测定其纯度(杂质不参加反应):

已知:I.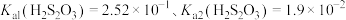 。
。
Ⅱ.上述过程发生反应: 、
、 。
。
① 标准液应盛放在
标准液应盛放在_______ 中进行滴定。
②滴定终点时,溶液由蓝色变为无色,则滴定时加入的指示剂名称是_______ 。
③滴定时,平行测定3次,平均消耗 标准液的体积为
标准液的体积为 ,则该氯化铬粗样品中
,则该氯化铬粗样品中 的纯度是
的纯度是______ (保留四位有效数字)。
 )是一种化工原料,可用于催化剂、颜料、印染、陶瓷、电镀等行业。实验室利用铬酸钡(
)是一种化工原料,可用于催化剂、颜料、印染、陶瓷、电镀等行业。实验室利用铬酸钡( )可制备少量氯化铬:
)可制备少量氯化铬:

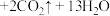 。回答下列问题:
。回答下列问题:(1)上述反应中,还原剂是
(2)该制备操作方法中,需加稍过量的乙醇,目的是
(3)制备的氯化铬粗样品利用下列滴定方法测定其纯度(杂质不参加反应):

已知:I.
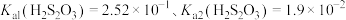 。
。Ⅱ.上述过程发生反应:
 、
、 。
。①
 标准液应盛放在
标准液应盛放在②滴定终点时,溶液由蓝色变为无色,则滴定时加入的指示剂名称是
③滴定时,平行测定3次,平均消耗
 标准液的体积为
标准液的体积为 ,则该氯化铬粗样品中
,则该氯化铬粗样品中 的纯度是
的纯度是
更新时间:2024-02-22 14:59:32
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】运用化学反应原理研究物质的性质具有重要意义。请回答下列问题:
(1)请配平以下化学方程式:___________
______Al+____NaNO3+____NaOH=___NaAlO2+____N2↑+___H2O
若反应过程中转移5 mol电子,则生成标准状况下N2的体积为___________ L。
(2)25℃时,将a mol·L-1的氨水与0.1mol·L-1的盐酸等体积混合,当溶液中离子浓度关系满足c(NH )>c(Cl-)时,则反应的情况可能为
)>c(Cl-)时,则反应的情况可能为___________ 。
a.盐酸不足,氨水剩余 b.氨水与盐酸恰好完全反应 c.盐酸过量
(3)向NH4HSO4溶液中滴加少量的Ba(OH)2溶液的离子方程式___________ 。
(4)25℃,两种酸的电离平衡常数如下表。
① HSO 的电离平衡常数表达式K=
的电离平衡常数表达式K=___________ 。
② 0.10 mol·L-1 Na2SO3溶液中离子浓度由大到小的顺序为___________ 。
③ H2SO3溶液和NaHCO3溶液混合,主要反应的离子方程式为___________ 。
(1)请配平以下化学方程式:
______Al+____NaNO3+____NaOH=___NaAlO2+____N2↑+___H2O
若反应过程中转移5 mol电子,则生成标准状况下N2的体积为
(2)25℃时,将a mol·L-1的氨水与0.1mol·L-1的盐酸等体积混合,当溶液中离子浓度关系满足c(NH
 )>c(Cl-)时,则反应的情况可能为
)>c(Cl-)时,则反应的情况可能为a.盐酸不足,氨水剩余 b.氨水与盐酸恰好完全反应 c.盐酸过量
(3)向NH4HSO4溶液中滴加少量的Ba(OH)2溶液的离子方程式
(4)25℃,两种酸的电离平衡常数如下表。
| Ka1 | Ka2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
① HSO
 的电离平衡常数表达式K=
的电离平衡常数表达式K=② 0.10 mol·L-1 Na2SO3溶液中离子浓度由大到小的顺序为
③ H2SO3溶液和NaHCO3溶液混合,主要反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】研究非金属化合物在生产、生活中的应用具有实际意义。
(1) 为了减少空气中SO2的排放,将含SO2的烟气通过洗涤剂X,再加入稀硫酸,既可以回收SO2,同时又可得到化肥。上述洗涤剂X可以是________ (选填序号)。
a. Ca(OH)2 b. K2CO3 c. NaHSO3 d. NH3·H2O
(2) 磷酸(H3PO4)是一种食品添加剂。它在水溶液中存在的各种微粒的物质的量分数δ随pH的变化曲线如下图。
①向Na3PO4溶液中滴入稀盐酸,溶液pH从10降低到5的过程中发生的主要反应的离子方程式为__________________ 。
②从图中推断:NaH2PO4和Na3PO4两盐在同一溶液中________ 大量共存。(填写“能”或者“不能”)
(3) BrF3是优良的电解溶剂,具有强氧化性,与水反应的化学方程式为:
3BrF3+5H2O===HBrO3+Br2+9HF+O2↑,若反应中产生了1.5 mol O2,则被水还原的BrF3的物质的量是________ mol。
(4) 二茂铁是一种金属有机配合物,可作燃料油的添加剂。二茂铁中配离子为C5H,其对应的环状分子C5H6的核磁共振氢谱如图1所示。C5H6与等物质的量Br2进行加成后的产物有M、N两种,M的核磁共振氢谱如图2所示。
写出C5H6的结构简式________ ;分子M发生加聚反应产物的结构简式________ 。
(1) 为了减少空气中SO2的排放,将含SO2的烟气通过洗涤剂X,再加入稀硫酸,既可以回收SO2,同时又可得到化肥。上述洗涤剂X可以是
a. Ca(OH)2 b. K2CO3 c. NaHSO3 d. NH3·H2O
(2) 磷酸(H3PO4)是一种食品添加剂。它在水溶液中存在的各种微粒的物质的量分数δ随pH的变化曲线如下图。

①向Na3PO4溶液中滴入稀盐酸,溶液pH从10降低到5的过程中发生的主要反应的离子方程式为
②从图中推断:NaH2PO4和Na3PO4两盐在同一溶液中
(3) BrF3是优良的电解溶剂,具有强氧化性,与水反应的化学方程式为:
3BrF3+5H2O===HBrO3+Br2+9HF+O2↑,若反应中产生了1.5 mol O2,则被水还原的BrF3的物质的量是
(4) 二茂铁是一种金属有机配合物,可作燃料油的添加剂。二茂铁中配离子为C5H,其对应的环状分子C5H6的核磁共振氢谱如图1所示。C5H6与等物质的量Br2进行加成后的产物有M、N两种,M的核磁共振氢谱如图2所示。


图1 图2
写出C5H6的结构简式
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】I由FeO、Fe2O3、 Fe3O4 组成的混合物,测得其中铁元素与氧元素的质量比为21:8 ,则这种混合物中FeO、Fe2O3、 Fe3O4 的物质的之比可能为_______ 。
A.1:2:1 B.1:1:1 C.2:1:1 D.1:1:2
II常温下KMnO4氧化浓HCI的反应方程式如下: 2KMnO4 +16HCl (浓) =2KCI+ 2MnCl2十5CI2↑+8H20
(1)用“双线桥法”标明反应中电子转移的方向和数目_______ 。
(2)又已知MnO2 + 4HCI(浓) MnCl2+Cl2↑+2H2O,结合以上反应原理,则MnO2、KMnO4、Cl2的氧化性由强到弱的顺序是:
MnCl2+Cl2↑+2H2O,结合以上反应原理,则MnO2、KMnO4、Cl2的氧化性由强到弱的顺序是:______ 。
(3)若有63.2g高锰酸钾参加反应,则被氧化的HCI的物质的量为______ mol,产
生的Cl2在标准状况下的体积______ L。
A.1:2:1 B.1:1:1 C.2:1:1 D.1:1:2
II常温下KMnO4氧化浓HCI的反应方程式如下: 2KMnO4 +16HCl (浓) =2KCI+ 2MnCl2十5CI2↑+8H20
(1)用“双线桥法”标明反应中电子转移的方向和数目
(2)又已知MnO2 + 4HCI(浓)
 MnCl2+Cl2↑+2H2O,结合以上反应原理,则MnO2、KMnO4、Cl2的氧化性由强到弱的顺序是:
MnCl2+Cl2↑+2H2O,结合以上反应原理,则MnO2、KMnO4、Cl2的氧化性由强到弱的顺序是:(3)若有63.2g高锰酸钾参加反应,则被氧化的HCI的物质的量为
生的Cl2在标准状况下的体积
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】高锰酸钾是一种常用氧化剂,主要用于化工、防腐及制药工业等。可将软锰矿(主要成分为MnO2)和KClO3在碱性介质中制得K2MnO4,然后通入CO2制备高锰酸钾。已知:
(1)制备锰酸钾的主要反应为:3MnO2+6KOH+KClO3=3K2MnO4+KCl+3H2O
①该反应中的氧化剂是_____________ ,还原剂是_____________ 。
②每生成 1mol K2MnO4转移_______ mol 电子。
(2)通入少量CO2气体时,锰酸钾发生歧化反应,生成KMnO4,MnO2,K2CO3。
①则生成的 KMnO4与MnO2的物质的量之比为__________ 。
②若CO2过量会生成KHCO3,导致得到的KMnO4产品的纯度降低,其原因是______________________________ ,可以把通CO2改为加其他的酸。从理论上分析,选用下列酸中_______ ,得到的产品纯度更高。
A.醋酸 B.浓盐酸 C.稀硫酸
| 温度 | 溶解度/g | ||||
| K2CO3 | KHCO3 | KMnO4 | K2SO4 | CH3COOK | |
| 20℃ | 111 | 33.7 | 6.38 | 11.1 | 217 |
(1)制备锰酸钾的主要反应为:3MnO2+6KOH+KClO3=3K2MnO4+KCl+3H2O
①该反应中的氧化剂是
②每生成 1mol K2MnO4转移
(2)通入少量CO2气体时,锰酸钾发生歧化反应,生成KMnO4,MnO2,K2CO3。
①则生成的 KMnO4与MnO2的物质的量之比为
②若CO2过量会生成KHCO3,导致得到的KMnO4产品的纯度降低,其原因是
A.醋酸 B.浓盐酸 C.稀硫酸
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】在弱碱性溶液中,FeS与 反应生成Fe(OH)3、Cr(OH)3和单质S,其离子方程式为
反应生成Fe(OH)3、Cr(OH)3和单质S,其离子方程式为_______ 。
 反应生成Fe(OH)3、Cr(OH)3和单质S,其离子方程式为
反应生成Fe(OH)3、Cr(OH)3和单质S,其离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】铜及其化合物在生产生活有广泛应用,铜在化合物中的常见化合价有+1、+2.已知 与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
(1)工业上可用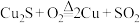 反应制取粗铜,该反应中
反应制取粗铜,该反应中___________ 元素被还原。不考虑杂质的反应,理论上生成1mol的 电子转移的数目为
电子转移的数目为___________
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入 溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为
溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为___________ 。温度控制在50~60℃的原因除了加快反应速率外,还有___________ 。在 溶液中加入一定量的
溶液中加入一定量的 和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:
和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:___________ 。
(3)现向Cu、 和CuO组成的混合物中,加入2L 0.6
和CuO组成的混合物中,加入2L 0.6
 溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。
溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。 跟稀硝酸反应的离子方程式为
跟稀硝酸反应的离子方程式为___________ 。若将上述混合物用足量的 加热还原,所得到固体的质量为
加热还原,所得到固体的质量为___________ g。若上述混合物中含0.2mol Cu,将该混合物与稀硫酸充分反应,消耗 的物质的量为
的物质的量为___________ mol。
 与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。(1)工业上可用
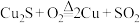 反应制取粗铜,该反应中
反应制取粗铜,该反应中 电子转移的数目为
电子转移的数目为(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入
 溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为
溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为 溶液中加入一定量的
溶液中加入一定量的 和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:
和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:(3)现向Cu、
 和CuO组成的混合物中,加入2L 0.6
和CuO组成的混合物中,加入2L 0.6
 溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。
溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。 跟稀硝酸反应的离子方程式为
跟稀硝酸反应的离子方程式为 加热还原,所得到固体的质量为
加热还原,所得到固体的质量为 的物质的量为
的物质的量为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】配合物乙二胺四乙酸铁钠可溶于水,常用于铁强化盐。某实验小组按如下流程制备NaFeY·3H2O (Y表示乙二胺四乙酸根):

已知:①2Fe(OH)3+ Na2CO3+2H4Y=2[NaFeY·3H2O]+CO2↑+H2O
②NaFeY·3H2O在250℃时完全分解,其溶解度20℃时为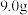 、80℃时为
、80℃时为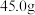
③ +5I-+6H+=3I2+3H2O;FeY-+4H+=H4Y+Fe3+;2Fe3++2I-=2Fe2++I2;I2+2
+5I-+6H+=3I2+3H2O;FeY-+4H+=H4Y+Fe3+;2Fe3++2I-=2Fe2++I2;I2+2 =
= +2I-
+2I-
市售铁强化盐中含有NaCl、KIO3、NaFeY,其中n(KIO3):n(NaFeY)=1∶50。称取mg样品,加稀硫酸溶解后配成 溶液。取出
溶液。取出 ,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用cmol·L-1Na2S2O3标准溶液滴定,重复操作2~3次,消耗Na2S2O3标准溶液的平均值为VmL。
,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用cmol·L-1Na2S2O3标准溶液滴定,重复操作2~3次,消耗Na2S2O3标准溶液的平均值为VmL。
(1)滴定终点的现象为___________ 。
(2)样品中铁元素的质量分数为___________ 。

已知:①2Fe(OH)3+ Na2CO3+2H4Y=2[NaFeY·3H2O]+CO2↑+H2O
②NaFeY·3H2O在250℃时完全分解,其溶解度20℃时为
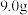 、80℃时为
、80℃时为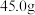
③
 +5I-+6H+=3I2+3H2O;FeY-+4H+=H4Y+Fe3+;2Fe3++2I-=2Fe2++I2;I2+2
+5I-+6H+=3I2+3H2O;FeY-+4H+=H4Y+Fe3+;2Fe3++2I-=2Fe2++I2;I2+2 =
= +2I-
+2I-市售铁强化盐中含有NaCl、KIO3、NaFeY,其中n(KIO3):n(NaFeY)=1∶50。称取mg样品,加稀硫酸溶解后配成
 溶液。取出
溶液。取出 ,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用cmol·L-1Na2S2O3标准溶液滴定,重复操作2~3次,消耗Na2S2O3标准溶液的平均值为VmL。
,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用cmol·L-1Na2S2O3标准溶液滴定,重复操作2~3次,消耗Na2S2O3标准溶液的平均值为VmL。(1)滴定终点的现象为
(2)样品中铁元素的质量分数为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】取一定量 浓溶液的稀释液,加入适量
浓溶液的稀释液,加入适量 、过量
、过量 溶液及一定量的稀
溶液及一定量的稀 ,充分反应。用标准
,充分反应。用标准 溶液滴定(滴定Ⅰ);再以酚酞为指示剂,用标准
溶液滴定(滴定Ⅰ);再以酚酞为指示剂,用标准 溶液滴定(滴定Ⅱ)。
溶液滴定(滴定Ⅱ)。
已知产生 的反应(不考虑
的反应(不考虑 与水反应):
与水反应):



实验数据如表:
(1)用标准 溶液滴定时,无需另加指示剂。判断滴定I到达终点的实验现象是
溶液滴定时,无需另加指示剂。判断滴定I到达终点的实验现象是________________ 。
(2)高纯度 浓溶液中要求
浓溶液中要求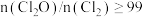 (
( 和
和 均以
均以 计)。结合数据分析所制备的
计)。结合数据分析所制备的 浓溶液是否符合要求
浓溶液是否符合要求_______________ 。
 浓溶液的稀释液,加入适量
浓溶液的稀释液,加入适量 、过量
、过量 溶液及一定量的稀
溶液及一定量的稀 ,充分反应。用标准
,充分反应。用标准 溶液滴定(滴定Ⅰ);再以酚酞为指示剂,用标准
溶液滴定(滴定Ⅰ);再以酚酞为指示剂,用标准 溶液滴定(滴定Ⅱ)。
溶液滴定(滴定Ⅱ)。已知产生
 的反应(不考虑
的反应(不考虑 与水反应):
与水反应):


实验数据如表:
加入量 |
|
滴定Ⅰ测出量 |
|
滴定Ⅰ测出量 |
|
(1)用标准
 溶液滴定时,无需另加指示剂。判断滴定I到达终点的实验现象是
溶液滴定时,无需另加指示剂。判断滴定I到达终点的实验现象是(2)高纯度
 浓溶液中要求
浓溶液中要求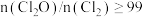 (
( 和
和 均以
均以 计)。结合数据分析所制备的
计)。结合数据分析所制备的 浓溶液是否符合要求
浓溶液是否符合要求
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】滴定法是测定溶液浓度的一种重要方法,常见的有酸碱中和滴定、氧化还原滴定、沉淀滴定法等。请回答下列问题:
(1)学生甲用0.1000 mol·L-1的NaOH溶液来测定未知浓度醋酸溶液。
①碱式滴定管用水洗后,接下来应该进行的操作是用待盛液洗涤2-3次,然后进行___________ ,再调整液面至0刻度或0刻度以下,然后记下液面的读数V1。
②移取20.00mL的醋酸溶液于锥形瓶中,并滴加2滴___________ 试液做指示剂。然后将滴定管中的NaOH溶液逐滴滴入锥形瓶内,滴加至锥形瓶内溶液颜色变为浅红色,且半分钟不褪色,停止滴加,记下读数V2.重复进行三次。
③下列操作中可能使所测醋酸溶液的浓度数值偏高的是___________ (填标号)。
A.水洗涤后的酸式滴定管未用醋酸溶液润洗就直接注入醋酸溶液,并移取20.00mL的醋酸溶液于锥形瓶中
B.滴定快达终点时,用蒸馏水洗涤锥形瓶的瓶壁,然后继续滴定至终点
C.读取NaOH溶液体积时,开始俯视读数,滴定结束时仰视读数
(2)实验室常用标准酸性KMnO4溶液测定绿矾(FeSO4·7H2O)样品的纯度(KMnO4被还原为Mn2+)。学生乙称取5.7 g绿矾样品,溶解,配成250 mL溶液。
①取25.00 mL该溶液于锥形瓶中,将用硫酸酸化的0.01mol/L KMnO4溶液置于酸式滴定管中进行滴定,滴定终点的标志是___________ 。
②若三次平行实验所消耗的标准液体积依次为39.96 mL、40.04mL、39.60mL,该绿矾样品的纯度为___________ 。
③已知亚铁离子被氧气氧化的反应是:4Fe2+ + O2 + (4+2x)H2O 2Fe2O3•xH2O + 8H+,硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧化的原因是
2Fe2O3•xH2O + 8H+,硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧化的原因是___________ 。
(3)某温度下,学生丙以K2CrO4 作指示剂,用0.100 mol·L-1的AgNO3溶液滴定50 mL 0.0500mol·L-1的Cl-溶液的滴定曲线如下图:(已知:Ag2CrO4 砖红色Ksp=1.0×10-12)

①相同实验条件下,若改为滴定0.0300 mol·L-1的Cl-溶液,反应终点c移向___________ (填“a”“b”“d”)。
②终点时溶液中c(Cl-)与c(CrO )的关系式为
)的关系式为___________ 。
(1)学生甲用0.1000 mol·L-1的NaOH溶液来测定未知浓度醋酸溶液。
①碱式滴定管用水洗后,接下来应该进行的操作是用待盛液洗涤2-3次,然后进行
②移取20.00mL的醋酸溶液于锥形瓶中,并滴加2滴
③下列操作中可能使所测醋酸溶液的浓度数值偏高的是
A.水洗涤后的酸式滴定管未用醋酸溶液润洗就直接注入醋酸溶液,并移取20.00mL的醋酸溶液于锥形瓶中
B.滴定快达终点时,用蒸馏水洗涤锥形瓶的瓶壁,然后继续滴定至终点
C.读取NaOH溶液体积时,开始俯视读数,滴定结束时仰视读数
(2)实验室常用标准酸性KMnO4溶液测定绿矾(FeSO4·7H2O)样品的纯度(KMnO4被还原为Mn2+)。学生乙称取5.7 g绿矾样品,溶解,配成250 mL溶液。
①取25.00 mL该溶液于锥形瓶中,将用硫酸酸化的0.01mol/L KMnO4溶液置于酸式滴定管中进行滴定,滴定终点的标志是
②若三次平行实验所消耗的标准液体积依次为39.96 mL、40.04mL、39.60mL,该绿矾样品的纯度为
③已知亚铁离子被氧气氧化的反应是:4Fe2+ + O2 + (4+2x)H2O
 2Fe2O3•xH2O + 8H+,硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧化的原因是
2Fe2O3•xH2O + 8H+,硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧化的原因是(3)某温度下,学生丙以K2CrO4 作指示剂,用0.100 mol·L-1的AgNO3溶液滴定50 mL 0.0500mol·L-1的Cl-溶液的滴定曲线如下图:(已知:Ag2CrO4 砖红色Ksp=1.0×10-12)

①相同实验条件下,若改为滴定0.0300 mol·L-1的Cl-溶液,反应终点c移向
②终点时溶液中c(Cl-)与c(CrO
 )的关系式为
)的关系式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】盐酸、醋酸和碳酸是化学实验和研究中常用的几种酸。
已知室温下:Ka(CH3COOH)=1.7×10-5;H2CO3的电离常数Ka1=4.2×10-7、Ka2=5.6×10-11
(1)①用离子方程式解释碳酸氢钠水溶液显碱性的原因_____________________________ 。
②常温下,物质的量浓度相同的下列四种溶液:a.碳酸钠溶液 b.醋酸钠溶液 c.氢氧化钠溶液 d.氢氧化钡溶液,其pH由大到小的顺序是_______________________________ (填序号)。
(2)某温度下,将pH均为4的盐酸和醋酸溶液分别加水稀释,其pH随溶液体积变化的曲线图中a、b、c三点对应溶液中水的电离程度由大到小的顺序为________________________ ;该醋酸溶液稀释过程中,下列各量一定变小的是_____________ 。

a.c(H+) b.c(OH-) c.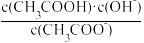 d.
d. 
(3)在t℃时,某NaOH稀溶液中c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知a+b=12,则在该温度下,将100mL 0.1 mol·L-1的稀H2SO4与100mL 0.4 mol·L-1的NaOH溶液混合后,溶液pH=________ 。
已知室温下:Ka(CH3COOH)=1.7×10-5;H2CO3的电离常数Ka1=4.2×10-7、Ka2=5.6×10-11
(1)①用离子方程式解释碳酸氢钠水溶液显碱性的原因
②常温下,物质的量浓度相同的下列四种溶液:a.碳酸钠溶液 b.醋酸钠溶液 c.氢氧化钠溶液 d.氢氧化钡溶液,其pH由大到小的顺序是
(2)某温度下,将pH均为4的盐酸和醋酸溶液分别加水稀释,其pH随溶液体积变化的曲线图中a、b、c三点对应溶液中水的电离程度由大到小的顺序为

a.c(H+) b.c(OH-) c.
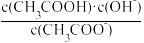 d.
d. 
(3)在t℃时,某NaOH稀溶液中c(H+)=10-amol·L-1,c(OH-)=10-bmol·L-1,已知a+b=12,则在该温度下,将100mL 0.1 mol·L-1的稀H2SO4与100mL 0.4 mol·L-1的NaOH溶液混合后,溶液pH=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】氮及其化合物与人们的生活生产密切相关。回答下列问题:
(1)微生物作用下,废水中的NH4+可转化为NO3-,该反应分两步反应:
I步:2NH4+(aq)+3O2(g)= 2NO2-(aq)+4H+(aq)+2H2O(l) △H=-546 kJ/mol
Ⅱ步:2NO2-(aq)+O2(g)= 2NO3-(aq) △H=-146 kJ/mol。
则低浓度氨氮废水中的NH4+(aq)氧化生成NO3-(aq)的热化学方程式为NH4+(aq)+2O2(g)===2H+(aq)+H2 O(1)+NO3-(aq) △H=___________ kJ/mol。
(2)氮与氧能形成多种二元化合物,这些化合物往往不稳定,其中NO2比较稳定。
①N2O5分解生成NO2和另外一种氮的氧化物,生成1 mol NO2时,转移1mol电子,则该反应的化学方程式是____________________________________________ 。
②已知可逆反应N2O4g) 2NO2(g) △H >0。在恒容密闭容器中充入一定量的N2O4,发生上述反应。测得N2O4的平衡转化率[α(N2O4)]随温度的变化如下图某条曲线:
2NO2(g) △H >0。在恒容密闭容器中充入一定量的N2O4,发生上述反应。测得N2O4的平衡转化率[α(N2O4)]随温度的变化如下图某条曲线:
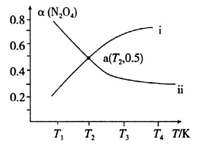
α(N2O4)随温度的变化的正确曲线是___________ (填“i”或“ii”)。若容器中通入N2O4的起始压强为102kPa,则a点温度下的平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,P分=P总×物质的量分数)。
(3)机动车尾气是造成雾霾的主要因素之一,CO、NO在催化剂作用下可转化为无害气体:2NO(g)+2CO(g) N2(g)+2CO2(g) △H<0。已知甲、乙两个恒温恒容容器,容积均为1L,两个容器中加入的CO的物质的量及CO随反应时间的变化如下表:
N2(g)+2CO2(g) △H<0。已知甲、乙两个恒温恒容容器,容积均为1L,两个容器中加入的CO的物质的量及CO随反应时间的变化如下表:

则反应温度高的容器是___________ (填“甲”或“乙”);甲容器中,0~120min的速率v(N2)=___________ mol/(L·min),达到化学平衡后,乙容器中各物质均加倍,则平衡向___________ (“正反应”或“逆反应”)方向移动。
(4)已知:25℃时,电离常数Kb(NH3·H2O)=2.0×10-5,Ka1(H2CO3)=4.0×10-7、Ka2(H2CO3)=5.0×10-11
①判断0.1mol/L的(NH4)2CO3溶液使pH试纸___________ (填“变蓝”“不变色”或“变红”),该溶液中c(CO32-)、c(HCO3-)、c(NH4+)的浓度大小关系是___________ 。
②0.50mol/L的Na2CO3溶液的pH=__________ 。(不考虑CO32-第二步水解和H2O的电离)
(1)微生物作用下,废水中的NH4+可转化为NO3-,该反应分两步反应:
I步:2NH4+(aq)+3O2(g)= 2NO2-(aq)+4H+(aq)+2H2O(l) △H=-546 kJ/mol
Ⅱ步:2NO2-(aq)+O2(g)= 2NO3-(aq) △H=-146 kJ/mol。
则低浓度氨氮废水中的NH4+(aq)氧化生成NO3-(aq)的热化学方程式为NH4+(aq)+2O2(g)===2H+(aq)+H2 O(1)+NO3-(aq) △H=
(2)氮与氧能形成多种二元化合物,这些化合物往往不稳定,其中NO2比较稳定。
①N2O5分解生成NO2和另外一种氮的氧化物,生成1 mol NO2时,转移1mol电子,则该反应的化学方程式是
②已知可逆反应N2O4g)
 2NO2(g) △H >0。在恒容密闭容器中充入一定量的N2O4,发生上述反应。测得N2O4的平衡转化率[α(N2O4)]随温度的变化如下图某条曲线:
2NO2(g) △H >0。在恒容密闭容器中充入一定量的N2O4,发生上述反应。测得N2O4的平衡转化率[α(N2O4)]随温度的变化如下图某条曲线:
α(N2O4)随温度的变化的正确曲线是
(3)机动车尾气是造成雾霾的主要因素之一,CO、NO在催化剂作用下可转化为无害气体:2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H<0。已知甲、乙两个恒温恒容容器,容积均为1L,两个容器中加入的CO的物质的量及CO随反应时间的变化如下表:
N2(g)+2CO2(g) △H<0。已知甲、乙两个恒温恒容容器,容积均为1L,两个容器中加入的CO的物质的量及CO随反应时间的变化如下表:
则反应温度高的容器是
(4)已知:25℃时,电离常数Kb(NH3·H2O)=2.0×10-5,Ka1(H2CO3)=4.0×10-7、Ka2(H2CO3)=5.0×10-11
①判断0.1mol/L的(NH4)2CO3溶液使pH试纸
②0.50mol/L的Na2CO3溶液的pH=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】请回答下列问题:
(1)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497 kJ·mol-1.
N2(g)+O2(g)=2NO(g) △H=+180.0kJ·mol-1。则相同条件下破坏1mol NO分子中的化学键需要吸收的能量为_______ kJ。
(2)25℃时,pH=5的CH3COOH溶液中.由水电离出的氢离子浓度c(H+)=________ kJ·mol-1;往溶液中加入少量NaOH固体,则溶液中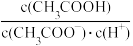
_______ (填“增大”、“减小”或“不变”),写出表示该混合溶液中所有离子浓度之间的一个等式:_________________ 。
(3)25℃下,向某Na2CO3溶液中加入稀盐酸,其中含碳元素的各种微粒物质的量分数(φ)随溶液pH变化的部分情况如图所示。

①在同一溶液中,H2CO3、HCO3-、CO32-______ (填“能”或“不能”)大量共存。
②当pH =7时,溶液中含碳元素的微粒主要为________ 。溶液中各种离子的物质的量浓度大小关系为______________ 。
③反应的CO32-+H2O HCO3-+OH-的平衡常数Kh=
HCO3-+OH-的平衡常数Kh=______________________ 。
(1)已知:N2、O2分子中化学键的键能分别是946kJ·mol-1、497 kJ·mol-1.
N2(g)+O2(g)=2NO(g) △H=+180.0kJ·mol-1。则相同条件下破坏1mol NO分子中的化学键需要吸收的能量为
(2)25℃时,pH=5的CH3COOH溶液中.由水电离出的氢离子浓度c(H+)=
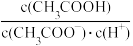
(3)25℃下,向某Na2CO3溶液中加入稀盐酸,其中含碳元素的各种微粒物质的量分数(φ)随溶液pH变化的部分情况如图所示。

①在同一溶液中,H2CO3、HCO3-、CO32-
②当pH =7时,溶液中含碳元素的微粒主要为
③反应的CO32-+H2O
 HCO3-+OH-的平衡常数Kh=
HCO3-+OH-的平衡常数Kh=
您最近一年使用:0次