二氯化二硫 可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点
可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点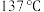 ,在潮湿的空气中剧烈水解而发烟,
,在潮湿的空气中剧烈水解而发烟, 可通过硫与少量氯气在
可通过硫与少量氯气在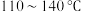 反应制得。
反应制得。
(1)有关 的下列说法正确的是___________。
的下列说法正确的是___________。
(2)选用以下装置制取少量 (夹持装置略):
(夹持装置略):
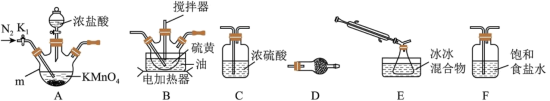
①A中反应的离子方程式为___________ 。
②装置连接顺序:A→___________ 。
③仪器D的名称为___________ ,D中的最佳试剂是___________ (选填序号)。
a.碱石灰 b. c.无水氯化钙
c.无水氯化钙
④实验前打开 ,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是
,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是___________ 。
⑤为了提高 的纯度,实验的关键是控制好温度和
的纯度,实验的关键是控制好温度和___________ 。
(3) 遇水会生成
遇水会生成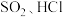 两种气体,某同学设计了如下实验方案来测定该混合气体中
两种气体,某同学设计了如下实验方案来测定该混合气体中 的体积分数。
的体积分数。
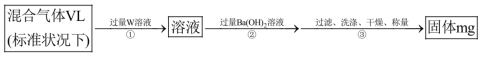
①W溶液可以是下列溶液中的___________ (填标号);
a. 溶液 b.酸性
溶液 b.酸性 溶液 c.氯水
溶液 c.氯水
②该混合气体中二氧化硫的体积分数为___________ (含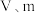 的代数式表示),若去掉①步骤,则所得结果
的代数式表示),若去掉①步骤,则所得结果___________ (填偏大、偏小或不变)。
 可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点
可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点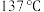 ,在潮湿的空气中剧烈水解而发烟,
,在潮湿的空气中剧烈水解而发烟, 可通过硫与少量氯气在
可通过硫与少量氯气在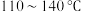 反应制得。
反应制得。(1)有关
 的下列说法正确的是___________。
的下列说法正确的是___________。A.固态时 属于共价晶体 属于共价晶体 |
B. 中 中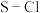 键的键能大于 键的键能大于 键的键能 键的键能 |
C.第一电离能、电负性均为: |
D. 是既有极性键又有非极性键的非极性分子 是既有极性键又有非极性键的非极性分子 |
 (夹持装置略):
(夹持装置略):
①A中反应的离子方程式为
②装置连接顺序:A→
③仪器D的名称为
a.碱石灰 b.
 c.无水氯化钙
c.无水氯化钙④实验前打开
 ,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是
,通入一段时间的氮气排尽装置内空气。实验结束停止加热后,再通入一段时间的氮气,其目的是⑤为了提高
 的纯度,实验的关键是控制好温度和
的纯度,实验的关键是控制好温度和(3)
 遇水会生成
遇水会生成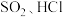 两种气体,某同学设计了如下实验方案来测定该混合气体中
两种气体,某同学设计了如下实验方案来测定该混合气体中 的体积分数。
的体积分数。
①W溶液可以是下列溶液中的
a.
 溶液 b.酸性
溶液 b.酸性 溶液 c.氯水
溶液 c.氯水②该混合气体中二氧化硫的体积分数为
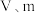 的代数式表示),若去掉①步骤,则所得结果
的代数式表示),若去掉①步骤,则所得结果
更新时间:2024-02-21 10:52:07
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】已知浓硫酸和木炭粉在加热条件下可发生化学反应。
(1)上述反应的化学方程式为_________________________________________ 。
(2)试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。

实验时可观察到装置①中A瓶中的溶液褪色,C瓶中的溶液不褪色。A瓶中的溶液的作用是___________________ ;B瓶中的溶液的作用是___________________ ;C瓶中的溶液的作用是__________________ 。
(3)装置②中所加固体药品是无水硫酸铜。可验证的产物是_______________ 。
(4)装置③中所盛溶液是澄清石灰水,可验证的产物是__________________ 。
(1)上述反应的化学方程式为
(2)试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。

实验时可观察到装置①中A瓶中的溶液褪色,C瓶中的溶液不褪色。A瓶中的溶液的作用是
(3)装置②中所加固体药品是无水硫酸铜。可验证的产物是
(4)装置③中所盛溶液是澄清石灰水,可验证的产物是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
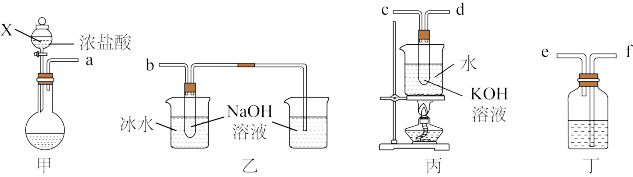
【推荐2】氯酸钾(KClO3)和次氯酸钠(NaClO)是氯元素重要的含氧酸盐,实验室中利用下图装置制备这两种盐。
回答下列问题:
(1)仪器X名称是________ ,甲装置圆底烧瓶中的试剂为K2Cr2O7固体,写出发生反应的离子方程式________ 。
(2)为达成实验目的,上述仪器口连接顺序依次为:a-_________ 。
(3)丁装置中所盛试剂为_______ ;乙装置中采用冰水浴冷却的目的是_______ 。
(4)反应结束,取出b中试管,经冷却结晶,_____ ,______ ,干燥,得到KClO3晶体。
(5)为进一步测定所得KClO3晶体的纯度,设计了如下实验方案:
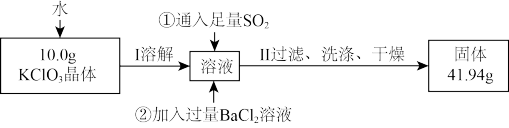
写出通入足量SO2时,溶液中发生反应的离子方程式_________ 。依据上述实验结果,测得该晶体的纯度为_________ 。

回答下列问题:
(1)仪器X名称是
(2)为达成实验目的,上述仪器口连接顺序依次为:a-
(3)丁装置中所盛试剂为
(4)反应结束,取出b中试管,经冷却结晶,
(5)为进一步测定所得KClO3晶体的纯度,设计了如下实验方案:

写出通入足量SO2时,溶液中发生反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】元素的“价—类”二维图是学习元素及其化合物的重要工具。下图是部分硫及其化合物的“价—类”二维图。根据图示回答下列问题:
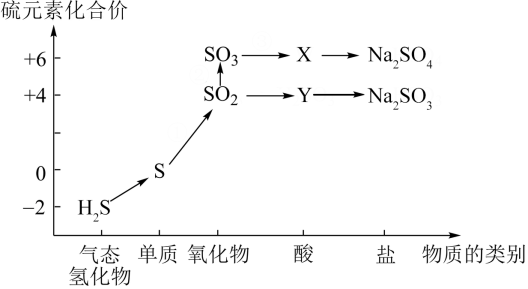
(1)X的化学式为_______ 。
(2)根据“价—类”二维图预测,SO2与酸性KMnO4溶液反应表现_______ 性,反应的离子方程式为_______ 。
(3)下列物质与SO2反应,SO2能表现出氧化性的是_______ (填序号)。
a.H2O b.H2S溶液 c.Na2SO3溶液
(4)SO2与CO2类似,可以和NaOH溶液反应,反应的离子方程式为_______ 。
(5)下列事实能说明硫的非金属性弱于氯的是_______ (填序号)。
a.稳定性:H2S<HCl
b.酸性:H2S<HCl
c.酸性:H2SO4<HClO4
d.往氢硫酸溶液中通入Cl2,产生淡黄色沉淀:H2S+Cl2=2HCl+S↓

(1)X的化学式为
(2)根据“价—类”二维图预测,SO2与酸性KMnO4溶液反应表现
(3)下列物质与SO2反应,SO2能表现出氧化性的是
a.H2O b.H2S溶液 c.Na2SO3溶液
(4)SO2与CO2类似,可以和NaOH溶液反应,反应的离子方程式为
(5)下列事实能说明硫的非金属性弱于氯的是
a.稳定性:H2S<HCl
b.酸性:H2S<HCl
c.酸性:H2SO4<HClO4
d.往氢硫酸溶液中通入Cl2,产生淡黄色沉淀:H2S+Cl2=2HCl+S↓
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】我国科学家借助自主研制的新型钨钴铁合金催化剂攻克了单壁碳纳米管结构的可控制备难题。海底金属软泥是在海底覆盖着的一层红棕色沉积物,蕴藏着大量的金属资源, 含有钨、铁、锰、锌、钴等金属元素。
(1)基态钴原子的价电子排布图为___________ 。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,其碳原子的杂化方式为___________ 。
(2)纳米结构氧化钴可在室温下将甲硫醛(CH2S)完全催化氧化,甲硫醛分子属___________ (填“极性”或“非极性”)分子,其中心原子的VSEPR模型名称为___________ 。
(3)六羰基钨[W(CO)6]的熔点为172 ℃,是一种重要的无机金属配合物,可溶于大多数有机溶剂。三种组成元素的电负性由大到小的顺序为___________ (用元素符号表示)。配体CO中与W形成配位键的原子是C而不是O,原因是___________ 。
(4)多原子分子中各原子若在同一平面内,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”。下列物质中存在“离域π键”的是___________(填字母)。
(1)基态钴原子的价电子排布图为
(2)纳米结构氧化钴可在室温下将甲硫醛(CH2S)完全催化氧化,甲硫醛分子属
(3)六羰基钨[W(CO)6]的熔点为172 ℃,是一种重要的无机金属配合物,可溶于大多数有机溶剂。三种组成元素的电负性由大到小的顺序为
(4)多原子分子中各原子若在同一平面内,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”。下列物质中存在“离域π键”的是___________(填字母)。
| A.苯 | B.二氧化硫 |
| C.四氯化碳 | D.环己烷 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】ECH(环氧氯丙烷,结构为 )是生产环氧树脂的中间体,工业上可由如图路线合成。
)是生产环氧树脂的中间体,工业上可由如图路线合成。

已知: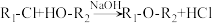
(1)A为丙烯,其分子中含有的官能团是____________ 。
(2)已知B→C为加成反应,A→B的反应类型是_________ 反应。
(3)B→C的反应中,B与次氯酸加成得到的C,有两种结构。
①C结构简式是i:ClCH2-CHCl-CH2OH和ii:_________ 。
②由分子中化学键的极性角度分析,i为B→C的主要产物的原因是_________ 。
(4)原料中的丙烯可由石油裂解得到。在裂解分离得到的含有三个碳原子的馏分中,除丙烯外,杂质气体中含有2种分子式均为C3H4的链烃D和E。
①D分子内含有sp3杂化的碳原子,则D结构简式为_________ 。
②E的核磁共振氢谱只有一组吸收峰,分子内无sp3杂化的碳原子。则
i.E中碳原子的杂化类型是_________ ;
ii.4个氢原子不在同一个平面内,由分子中碳原子的杂化解释其原因_________ 。
 )是生产环氧树脂的中间体,工业上可由如图路线合成。
)是生产环氧树脂的中间体,工业上可由如图路线合成。
已知:
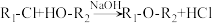
(1)A为丙烯,其分子中含有的官能团是
(2)已知B→C为加成反应,A→B的反应类型是
(3)B→C的反应中,B与次氯酸加成得到的C,有两种结构。
①C结构简式是i:ClCH2-CHCl-CH2OH和ii:
②由分子中化学键的极性角度分析,i为B→C的主要产物的原因是
(4)原料中的丙烯可由石油裂解得到。在裂解分离得到的含有三个碳原子的馏分中,除丙烯外,杂质气体中含有2种分子式均为C3H4的链烃D和E。
①D分子内含有sp3杂化的碳原子,则D结构简式为
②E的核磁共振氢谱只有一组吸收峰,分子内无sp3杂化的碳原子。则
i.E中碳原子的杂化类型是
ii.4个氢原子不在同一个平面内,由分子中碳原子的杂化解释其原因
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】如图所示:下图为A → E五种含同种元素的物质相互转化的关系图,其中A、B、C、D常温下都是气体,D呈红棕色。按要求回答下列问题:
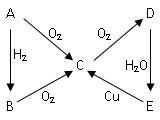
(1) A物质的电子式_______ ;B物质是含______ 键
的______ 分子(填“极性”或者“非极性”)
(2)下列反应的化学方程式为:
①B→C:_____________________________________________
②D→E:_____________________________________________
(3)实验室制取B的化学方程式为:__________________________________________ ,通常用___________ 来干燥B气体;
已知B可以与灼热的氧化铜反应得到A气体和金属铜,则该反应的化学方程式为:________________________________________________ 。

(1) A物质的电子式
的
(2)下列反应的化学方程式为:
①B→C:
②D→E:
(3)实验室制取B的化学方程式为:
已知B可以与灼热的氧化铜反应得到A气体和金属铜,则该反应的化学方程式为:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】倍半硅氧烷在液晶显示、塑料阻燃、生物医用等领域具有重要应用,氢基倍半硅氧烷的分子结构如图A所示,其加热分解产物中SiO2的晶胞结构如图B所示,回答下列问题:

(1)基态Si原子的最外层电子排布式为______ ,其中成对电子之间的主要区别是______
(2)图A分子中H的化合价为______ ,Si原子采用_____ 杂化,形成的极性共价键类型为______ ;键的极性Si-H键______ Si-O(填空“>”、“<”、“=”)
(3)图A分子结构中,一个硅原子被3个____ 元环共有,硅的配位数为____ ,该分子的分子式为____
(4)氢基倍半硅氧烷为___ 晶体,SiO2为____ 晶体;
(5)每个SiO2晶胞含有Si原子的个数为____ ;已知SiO2晶体为面心立体结构,晶胞参为a nm,阿伏加德罗常数的值为NA,则SiO2晶体的密度为____ g·cm-3

(1)基态Si原子的最外层电子排布式为
(2)图A分子中H的化合价为
(3)图A分子结构中,一个硅原子被3个
(4)氢基倍半硅氧烷为
(5)每个SiO2晶胞含有Si原子的个数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】2022年北京冬季奥运会场馆使用了大量不锈钢材质,不锈钢属于合金钢,其基体是铁碳合金,常用的不锈钢中含铬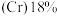 、含镍
、含镍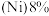 。回答下列问题:
。回答下列问题:
(1)不锈钢所属的晶体类型为_______ 。
(2)铁系元素能与 形成
形成 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点
为浅黄色液体,沸点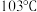 ,则该晶体的晶体类型为
,则该晶体的晶体类型为_______ 晶体, 中含有的化学键类型包括
中含有的化学键类型包括_______ (填字母)。
A.氢键 B.离子键 C.配位键 D.极性共价键 E.金属键 F.范德华力
(3)氧元素与 可形成低价态氧化物
可形成低价态氧化物 。
。
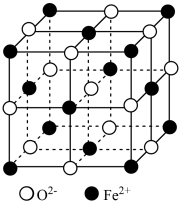
① 立方晶胞结构如图所示,则单位晶胞内
立方晶胞结构如图所示,则单位晶胞内 的个数为
的个数为_______ ;与 紧邻的所有
紧邻的所有 构成的几何构型为
构成的几何构型为_______ 。
②若 与
与 之间最近距离为
之间最近距离为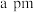 ,则该晶体的密度计算式为
,则该晶体的密度计算式为_______  。(用含
。(用含 的代数式表示,
的代数式表示, 代表阿伏加德罗常数的值)
代表阿伏加德罗常数的值)
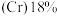 、含镍
、含镍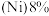 。回答下列问题:
。回答下列问题:(1)不锈钢所属的晶体类型为
(2)铁系元素能与
 形成
形成 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点
为浅黄色液体,沸点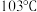 ,则该晶体的晶体类型为
,则该晶体的晶体类型为 中含有的化学键类型包括
中含有的化学键类型包括A.氢键 B.离子键 C.配位键 D.极性共价键 E.金属键 F.范德华力
(3)氧元素与
 可形成低价态氧化物
可形成低价态氧化物 。
。
①
 立方晶胞结构如图所示,则单位晶胞内
立方晶胞结构如图所示,则单位晶胞内 的个数为
的个数为 紧邻的所有
紧邻的所有 构成的几何构型为
构成的几何构型为②若
 与
与 之间最近距离为
之间最近距离为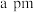 ,则该晶体的密度计算式为
,则该晶体的密度计算式为 。(用含
。(用含 的代数式表示,
的代数式表示, 代表阿伏加德罗常数的值)
代表阿伏加德罗常数的值)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铍由法国人沃克兰(Vauquelin)于1798年发现,其最重要矿物是绿柱石( ),若其中含有2%的Cr即为祖母绿———种极名贵的宝石。回答下列问题:
),若其中含有2%的Cr即为祖母绿———种极名贵的宝石。回答下列问题:
(1)基态Cr原子的价层电子排布式为___________ ,绿柱石中,除Be外,各元素的电负性由大到小的顺序为___________ 。
(2)已知一些物质的熔点数据如表:
Be与Mg同主族, 的熔点低于
的熔点低于 ,原因是
,原因是___________ 。
(3) 具有两性,能与NaOH反应生成
具有两性,能与NaOH反应生成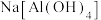 ,
, 中Al属于
中Al属于___________ 区元素(填元素周期表的分区),O原子的杂化轨道类型为___________ ,阴离子中所含化学键类型为___________ (填序号)。
a.极性键 b.非极性键 c.离子键 d.氢键 e.配位键
(4)一种硅氧化合物具有优良的耐高温性能,其晶胞结构如图所示,氧原子位于硅原子构成的正四面体的空隙中,该晶胞中氧原子的配位数为___________ ,A原子的分数坐标为 ,则B原子的分数坐标为
,则B原子的分数坐标为___________ ,已知晶胞密度为 ,则晶体中硅原子间的最近距离为
,则晶体中硅原子间的最近距离为___________ pm。

 ),若其中含有2%的Cr即为祖母绿———种极名贵的宝石。回答下列问题:
),若其中含有2%的Cr即为祖母绿———种极名贵的宝石。回答下列问题:(1)基态Cr原子的价层电子排布式为
(2)已知一些物质的熔点数据如表:
| 物质 |  |  |
| 熔点/℃ | 440 | 714 |
 的熔点低于
的熔点低于 ,原因是
,原因是(3)
 具有两性,能与NaOH反应生成
具有两性,能与NaOH反应生成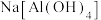 ,
, 中Al属于
中Al属于a.极性键 b.非极性键 c.离子键 d.氢键 e.配位键
(4)一种硅氧化合物具有优良的耐高温性能,其晶胞结构如图所示,氧原子位于硅原子构成的正四面体的空隙中,该晶胞中氧原子的配位数为
 ,则B原子的分数坐标为
,则B原子的分数坐标为 ,则晶体中硅原子间的最近距离为
,则晶体中硅原子间的最近距离为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】二氧化氯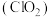 消毒剂可有效灭活新冠病毒。
消毒剂可有效灭活新冠病毒。 沸点为
沸点为 ,不稳定,常转化为
,不稳定,常转化为 产品。
产品。
(1)工业上采用 和
和 混合溶液吸收
混合溶液吸收 制备
制备 ,反应的离子方程式为
,反应的离子方程式为_______ 。吸收一般在冰水浴中进行,其原因可能是防止 分解、
分解、_______ 。
(2)产品中 质量分数的测定:称取
质量分数的测定:称取 产品配成
产品配成 溶液;取
溶液;取 所配溶液,加入足量
所配溶液,加入足量 溶液和稀
溶液和稀 (发生反应
(发生反应 );向充分反应后的混合物中逐滴加入
);向充分反应后的混合物中逐滴加入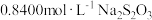 溶液至恰好完全反应(
溶液至恰好完全反应(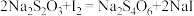 ),共消耗
),共消耗 溶液的体积为
溶液的体积为 。
。
①若加入 溶液后在空气中放置时间过长,会导致测得的
溶液后在空气中放置时间过长,会导致测得的 质量分数
质量分数_______ (选填“偏高”、“偏低”或“无影响”)。
②求产品中 的质量分数
的质量分数_______ (产品中的杂质不与 、
、 发生反应,写出计算过程)。
发生反应,写出计算过程)。
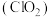 消毒剂可有效灭活新冠病毒。
消毒剂可有效灭活新冠病毒。 沸点为
沸点为 ,不稳定,常转化为
,不稳定,常转化为 产品。
产品。(1)工业上采用
 和
和 混合溶液吸收
混合溶液吸收 制备
制备 ,反应的离子方程式为
,反应的离子方程式为 分解、
分解、(2)产品中
 质量分数的测定:称取
质量分数的测定:称取 产品配成
产品配成 溶液;取
溶液;取 所配溶液,加入足量
所配溶液,加入足量 溶液和稀
溶液和稀 (发生反应
(发生反应 );向充分反应后的混合物中逐滴加入
);向充分反应后的混合物中逐滴加入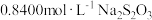 溶液至恰好完全反应(
溶液至恰好完全反应(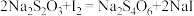 ),共消耗
),共消耗 溶液的体积为
溶液的体积为 。
。①若加入
 溶液后在空气中放置时间过长,会导致测得的
溶液后在空气中放置时间过长,会导致测得的 质量分数
质量分数②求产品中
 的质量分数
的质量分数 、
、 发生反应,写出计算过程)。
发生反应,写出计算过程)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】ICl(氯化碘)是红棕色液体,熔点为13.9°C,沸点为974°C,易水解,接触空气时能形成五氧化二碘,能与许多单质发生作用,溶于乙醇、乙醚等。某校研究性学习小组的同学拟用下列仪器制备氯化碘。回答下列问题:

(1)检查A装置气密性的方法为___________ 。
(2)上述装置,按气流方向连接的顺序为___________ 。(装置可重复使用)。
(3)C装置的作用是___________ 。
(4)E装置中的物质反应时需放在水中,控制温度大约40°C,其目的是______________________ 。
(5)按上述连接好的装置进行实验,实验步骤如下:
①检查装置气密性后,装入药品②打开分液漏斗活塞③关闭分液漏斗活塞④停止加热E,充分冷却⑤水浴加热E
请按正确的顺序填入上述步骤的序号___________ 。
(6)ICl和水反应的化学方程式为___________ 。
(7)自来水厂用ClO2处理后的水,可用碘量法可以检测水中ClO2的浓度,步骤如下:
I、取定体积的水样,加入过量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。(已知:2ClO2+2I-=2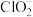 +I2)
+I2)
II、Na2S2O3溶液滴定到终点。(已知:2 +I2=
+I2= +2I-)
+2I-)
问题:①滴定终点时的现象:___________
②若水样的体积为1.0L,在操作II时消耗了1.0×10-3mol·L-1的Na2S2O3溶液15mL,则水样中ClO2的浓度是___________ mol·L-1。
(8)将0.64gCu全部溶于一定量的浓硝酸中,测得生成气体0.009mol(含NO、NO2和N2O4),共消耗硝酸0.032mol。将生成的气体与空气混合,再通入NaOH溶液中,氮氧化物被完全吸收,产物只有NaNO3和H2O。计算空气中参加反应的O2在标准状况下的体积为___________ mL。

(1)检查A装置气密性的方法为
(2)上述装置,按气流方向连接的顺序为
(3)C装置的作用是
(4)E装置中的物质反应时需放在水中,控制温度大约40°C,其目的是
(5)按上述连接好的装置进行实验,实验步骤如下:
①检查装置气密性后,装入药品②打开分液漏斗活塞③关闭分液漏斗活塞④停止加热E,充分冷却⑤水浴加热E
请按正确的顺序填入上述步骤的序号
(6)ICl和水反应的化学方程式为
(7)自来水厂用ClO2处理后的水,可用碘量法可以检测水中ClO2的浓度,步骤如下:
I、取定体积的水样,加入过量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。(已知:2ClO2+2I-=2
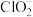 +I2)
+I2)II、Na2S2O3溶液滴定到终点。(已知:2
 +I2=
+I2= +2I-)
+2I-)问题:①滴定终点时的现象:
②若水样的体积为1.0L,在操作II时消耗了1.0×10-3mol·L-1的Na2S2O3溶液15mL,则水样中ClO2的浓度是
(8)将0.64gCu全部溶于一定量的浓硝酸中,测得生成气体0.009mol(含NO、NO2和N2O4),共消耗硝酸0.032mol。将生成的气体与空气混合,再通入NaOH溶液中,氮氧化物被完全吸收,产物只有NaNO3和H2O。计算空气中参加反应的O2在标准状况下的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】高锰酸钾是常见的强氧化剂,其制备流程如图:
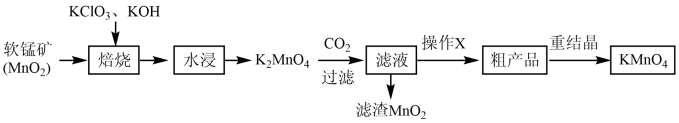
i.制取锰酸钾(K2MnO4)
碱熔:用托盘天平称取5.0gKOH固体、1.5gKClO3固体于坩埚中,混匀、小心加热,不断搅拌,待混合物完全熔融后,加入MnO2粉末3.5g,加热到颜色变为深绿色,用力搅拌到固体干涸、固化,再加热5min,并用铁棒将其尽量捣碎。
浸取:待物料冷却后,置于200mL烧杯中,用50mL蒸馏水浸取,过滤,得到绿色的溶液。
(1)碱熔过程中发生反应的化学方程式为____ ;加热中若不小心将液体溅到皮肤上,应____ 处理;加热时应选择____ (填字母)。
a.瓷坩埚 b.铁坩埚 c.石英坩埚 d.氧化铝坩埚
ii.制取高锰酸钾(KMnO4)
在浸取液中通入CO2气体,至K2MnO4完全反应,用pH试纸测定溶液pH达到10~11时,停止通入CO2。然后把溶液加热,趁热用铺有尼龙布的布氏漏斗进行减压过滤,除去残渣……
已知:常温常压下,饱和碳酸钾溶液的pH为11.6;碳酸氢钾溶液的pH为8.3。
(2)通入CO2发生反应的离子方程式为____ ;判断此反应进行是否完全,也可以用玻璃棒蘸取溶液于滤纸上,若呈现____ 现象,停止通入CO2;过滤时不用滤纸而用尼龙布的原因:____ ;(填“能”或“不能”)____ 用加盐酸的方法代替通入CO2,其理由:____ 。
iii.重结晶提纯
(3)利用重结晶的方法对产品提纯,所得产品质量2.8g,则高锰酸钾的产率为____ 。(精确到0.1%)。

i.制取锰酸钾(K2MnO4)
碱熔:用托盘天平称取5.0gKOH固体、1.5gKClO3固体于坩埚中,混匀、小心加热,不断搅拌,待混合物完全熔融后,加入MnO2粉末3.5g,加热到颜色变为深绿色,用力搅拌到固体干涸、固化,再加热5min,并用铁棒将其尽量捣碎。
浸取:待物料冷却后,置于200mL烧杯中,用50mL蒸馏水浸取,过滤,得到绿色的溶液。
(1)碱熔过程中发生反应的化学方程式为
a.瓷坩埚 b.铁坩埚 c.石英坩埚 d.氧化铝坩埚
ii.制取高锰酸钾(KMnO4)
在浸取液中通入CO2气体,至K2MnO4完全反应,用pH试纸测定溶液pH达到10~11时,停止通入CO2。然后把溶液加热,趁热用铺有尼龙布的布氏漏斗进行减压过滤,除去残渣……
已知:常温常压下,饱和碳酸钾溶液的pH为11.6;碳酸氢钾溶液的pH为8.3。
(2)通入CO2发生反应的离子方程式为
iii.重结晶提纯
(3)利用重结晶的方法对产品提纯,所得产品质量2.8g,则高锰酸钾的产率为
您最近一年使用:0次



