W、X、Y、Z、M、Q是原子序数依次递增的前四周期元素,W元素基态原子的三个能级上电子相同,Y元素基态原子核外有8种不同运动状态的电子,Y与Z位于同主族,M是前四周期基态原子核外未成对电子数最多的元素,Q元素位于ds区,常见的化合价有两种。回答下列问题:
(1)X、Z元素符号分别是___________ ,Q元素在周期表的位置是___________ ,M的基态原子的价电子排布式是___________ 。
(2)原子核外电子的运动有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 号表示,称为电子的自旋磁量子数。对于基态的X原子,其价电子自旋磁量子数的代数和为
号表示,称为电子的自旋磁量子数。对于基态的X原子,其价电子自旋磁量子数的代数和为___________ ,基态的X原子最高能级的电子所在原子轨道的轮廓图形为___________ 。
(3)W、X、Y元素第一电离能最大的是___________ (用元素符号表示,下同),电负性最大的是___________ 。
(4)W与Z的化合物共用电子对偏向于Z,举出一个事实,说明Z的非金属性比W强(用化学方程式表示):___________ 。
(5)在较高温度下QY转化成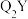 ,从原子结构角度分析
,从原子结构角度分析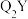 比QY更稳定的原因:
比QY更稳定的原因:___________ 。
(1)X、Z元素符号分别是
(2)原子核外电子的运动有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 号表示,称为电子的自旋磁量子数。对于基态的X原子,其价电子自旋磁量子数的代数和为
号表示,称为电子的自旋磁量子数。对于基态的X原子,其价电子自旋磁量子数的代数和为(3)W、X、Y元素第一电离能最大的是
(4)W与Z的化合物共用电子对偏向于Z,举出一个事实,说明Z的非金属性比W强(用化学方程式表示):
(5)在较高温度下QY转化成
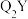 ,从原子结构角度分析
,从原子结构角度分析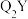 比QY更稳定的原因:
比QY更稳定的原因:
更新时间:2024-03-02 07:17:56
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】铬黄 为黄色或橙黄色结晶性粉末,溶于碱液、无机酸,不溶于水、油类,常用作橡胶、油墨、水彩、油彩、色纸等的着色剂。某化学科研小组以
为黄色或橙黄色结晶性粉末,溶于碱液、无机酸,不溶于水、油类,常用作橡胶、油墨、水彩、油彩、色纸等的着色剂。某化学科研小组以 为原料制备
为原料制备 ,其工艺流程如图所示。
,其工艺流程如图所示。
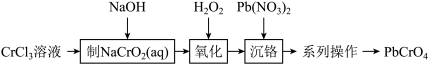
已知: (两性氢氧化物)呈绿色且难溶于水,
(两性氢氧化物)呈绿色且难溶于水, 易溶于水,
易溶于水, 的
的 为
为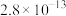 。
。
回答下列问题:
(1)基态 核外未成对电子的数目为
核外未成对电子的数目为_______ , 在元素周期表中的位置为
在元素周期表中的位置为_______ 。
(2)“制 ”时,发生反应的离子方程式为
”时,发生反应的离子方程式为_______ 。
(3)“氧化”时发生反应的离子方程式为_______ ( 转化为
转化为 ),“氧化”时反应温度不宜过高,其原因是
),“氧化”时反应温度不宜过高,其原因是_______ 。
(4)若使溶液中 完全沉淀(浓度低于
完全沉淀(浓度低于 ),则需要溶液中
),则需要溶液中 的浓度不低于
的浓度不低于_______  。
。
(5)“系列操作”包括过滤、洗涤、干燥,洗涤时玻璃棒的作用是_______ ,证明沉淀已洗涤干净的具体操作为_______ 。
 为黄色或橙黄色结晶性粉末,溶于碱液、无机酸,不溶于水、油类,常用作橡胶、油墨、水彩、油彩、色纸等的着色剂。某化学科研小组以
为黄色或橙黄色结晶性粉末,溶于碱液、无机酸,不溶于水、油类,常用作橡胶、油墨、水彩、油彩、色纸等的着色剂。某化学科研小组以 为原料制备
为原料制备 ,其工艺流程如图所示。
,其工艺流程如图所示。
已知:
 (两性氢氧化物)呈绿色且难溶于水,
(两性氢氧化物)呈绿色且难溶于水, 易溶于水,
易溶于水, 的
的 为
为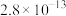 。
。回答下列问题:
(1)基态
 核外未成对电子的数目为
核外未成对电子的数目为 在元素周期表中的位置为
在元素周期表中的位置为(2)“制
 ”时,发生反应的离子方程式为
”时,发生反应的离子方程式为(3)“氧化”时发生反应的离子方程式为
 转化为
转化为 ),“氧化”时反应温度不宜过高,其原因是
),“氧化”时反应温度不宜过高,其原因是(4)若使溶液中
 完全沉淀(浓度低于
完全沉淀(浓度低于 ),则需要溶液中
),则需要溶液中 的浓度不低于
的浓度不低于 。
。(5)“系列操作”包括过滤、洗涤、干燥,洗涤时玻璃棒的作用是
您最近一年使用:0次
【推荐2】下表列出前20号元素中的某些元素性质的一些数据:
试回答下列问题:
(1)以上10种元素中第一电离能最小的是____ (填编号)。比元素B原子序数大10的元素在元素周期表中的位置:第____ 周期第____ 族,其基态原子的核外电子排布式是___________ 。
(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是____ (写分子式,写出两种即可),元素G、I分别和J形成的两种化合物的晶体类型分别是 _________ 、___________ 。
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。 其分子中共形成____ 个σ键,____ 个π键。
(4)短周期某主族元素K的电离能情况如图(A)所示。则K元素位于周期表的第_____ 周期、第____ 族。

图(B)是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第____ 族元素氢化物的沸点的变化规律。不同同学对某主族元素的氢化物的沸点变化趋势画出了两条折线——折线a和折线b,你认为正确的是____ ,理由是_______________ 。
| 元素 | A | B | C | D | E | F | G | H | I | J |
| 原子半径 (10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | — | -2 | — | -4 | -3 | -1 | — | -3 | -4 |
(1)以上10种元素中第一电离能最小的是
(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。 其分子中共形成
(4)短周期某主族元素K的电离能情况如图(A)所示。则K元素位于周期表的第

图(B)是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】一种新型硫酸盐功能电解液由2mol·L-1Na2SO4和0.3mol·L-1MgSO4混合组成,电化学测试表明该电解液构建的Na2Ni[Fe(CN)6]、NaTi2(PO4)3/C电池可以稳定循环500次以上。
请回答下列问题:
(1)MgSO4三种原子中电负性最大的元素是_______ (填名称)。
(2)Na2Ni[Fe(CN)6]中,基态Fe2+核外电子的价电子排布式_______ ,[Fe(CN)6]4-中σ键和π键的数目之比为_______ 。
(3)NaTi2(PO4)3中, 中磷原子的杂化类型是
中磷原子的杂化类型是_______ 。
(4)①氨气溶于水时,大部分NH3与H2O用氢键(用“···”表示)结合形成NH3·H2O分子。根据氨水的性质可推知NH3·H2O的结构式为_______ (填标号)。
A.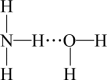 B.
B.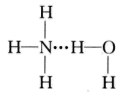
C. D.
D.
②将NH3与CO2以 =2溶于水,充分反应后所得的产物中,阴离子的空间结构为
=2溶于水,充分反应后所得的产物中,阴离子的空间结构为_______ 。
(5)NiaMgbFec的立方晶胞结构如图所示。已知晶胞的边长为npm,设NA为阿伏加德罗常数的值。
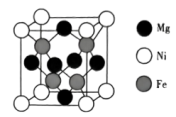
①a:b:c=_______ 。
②该晶体密度是_______ g·cm-3(用含n、NA的代数式表示)。
请回答下列问题:
(1)MgSO4三种原子中电负性最大的元素是
(2)Na2Ni[Fe(CN)6]中,基态Fe2+核外电子的价电子排布式
(3)NaTi2(PO4)3中,
 中磷原子的杂化类型是
中磷原子的杂化类型是(4)①氨气溶于水时,大部分NH3与H2O用氢键(用“···”表示)结合形成NH3·H2O分子。根据氨水的性质可推知NH3·H2O的结构式为
A.
 B.
B.
C.
 D.
D.
②将NH3与CO2以
 =2溶于水,充分反应后所得的产物中,阴离子的空间结构为
=2溶于水,充分反应后所得的产物中,阴离子的空间结构为(5)NiaMgbFec的立方晶胞结构如图所示。已知晶胞的边长为npm,设NA为阿伏加德罗常数的值。

①a:b:c=
②该晶体密度是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】砷化铝(AlAs)常用作光谱分析试剂和制备电子组件的原料,是一种新型半导体材料。回答下列问题:
(1)基态As原子的核外价电子排布图为_______ ;第一电离能I1(As)_______ I1(Se) (填“大于”或“小于”),其原因是_______ 。
(2)As4S4的分子结构中均为单键,且每个原子最外层均满足8e-稳定结构,则该分子中所含共价键数目为_______ ;分子中As、S原子的杂化轨道类型分别为_______ 、_______ 。
(3)AlF3的熔点约为1 040 ℃,AlCl3的熔点为194 ℃,其晶体类型分别是_______ 、_______ 。
(4)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图1所示,其中的致密保护膜可阻止H2O2刻蚀液与下层GaAs(砷化镓)反应。

已知AlAs的立方晶胞如图2所示,其中As的配位数为_______ ;该晶体密度为ρ g·cm-3,设NA为阿伏加德罗常数的值,晶胞参数为_______ pm。

(1)基态As原子的核外价电子排布图为
(2)As4S4的分子结构中均为单键,且每个原子最外层均满足8e-稳定结构,则该分子中所含共价键数目为
(3)AlF3的熔点约为1 040 ℃,AlCl3的熔点为194 ℃,其晶体类型分别是
(4)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图1所示,其中的致密保护膜可阻止H2O2刻蚀液与下层GaAs(砷化镓)反应。

已知AlAs的立方晶胞如图2所示,其中As的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】近年来美国为了遏制中国发展,对我国发起了以封锁“芯片”为核心的全方位打压,此举激发了中国科技人员自研的决心。回答下列问题:
(1)我国现已能够拉制出直径为300mm、重达81kg的大直径硅单晶,晶体硅材料被大量用于电子产业。 反应生成
反应生成 ,判断
,判断 的沸点比
的沸点比 的
的_______ (填“高”或“低”),理由_______ 。
(2)超高导热绝缘耐高温纳米氮化铝,是制造5G芯片的重要绝缘材料。氮化铝晶体与金刚石类似,每个铝原子与_______ 个氮原子相连,氮化铝晶体属于_______ 晶体。
(3)“遥遥领先”的华为芯片制造过程用了蚀刻技术。利用 进行硅芯片蚀刻时的产物均为气体,在蚀刻物表面不留任何残留物。
进行硅芯片蚀刻时的产物均为气体,在蚀刻物表面不留任何残留物。
① 分子的空间构型为
分子的空间构型为_______ 。
② 的一种下游产品三聚氟氰(分子式为:
的一种下游产品三聚氟氰(分子式为: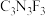 ),分子结构中有类似苯环结构,所有原子均满足8电子结构。写出三聚氟氰的结构式
),分子结构中有类似苯环结构,所有原子均满足8电子结构。写出三聚氟氰的结构式_______ 。
(4)2022年10月宁波南大光电ArF光刻胶生产线正式投产,国内7nm芯片制造材料获得重大突破。一种聚碳酸酯胶的曝光分解原理如下:_______ 。
②聚碳酸酯膜曝光后的产物加热可汽化或溶于水,加热汽化或溶于水克服的作用力有_______ 。
a.配位键 b.离子键 c.范德华力 d.氢键 e.共价键
(5)GaAs是一种制造芯片重要的半导体材料,晶胞结构如图1,将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料,如图2。_______ 。
②若GaAs晶体密度为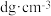 ,设
,设 为阿伏加德罗常数的值,则晶胞中两个As原子间的最小距离为
为阿伏加德罗常数的值,则晶胞中两个As原子间的最小距离为_______ cm(列出计算式即可)。
③稀磁性半导体材料中Mn、As的原子个数比为_______ 。
(1)我国现已能够拉制出直径为300mm、重达81kg的大直径硅单晶,晶体硅材料被大量用于电子产业。
①某同学画出基态Si原子的价层电子排布图: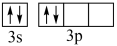 ,该电子排布图违背
,该电子排布图违背
 反应生成
反应生成 ,判断
,判断 的沸点比
的沸点比 的
的(2)超高导热绝缘耐高温纳米氮化铝,是制造5G芯片的重要绝缘材料。氮化铝晶体与金刚石类似,每个铝原子与
(3)“遥遥领先”的华为芯片制造过程用了蚀刻技术。利用
 进行硅芯片蚀刻时的产物均为气体,在蚀刻物表面不留任何残留物。
进行硅芯片蚀刻时的产物均为气体,在蚀刻物表面不留任何残留物。①
 分子的空间构型为
分子的空间构型为②
 的一种下游产品三聚氟氰(分子式为:
的一种下游产品三聚氟氰(分子式为: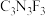 ),分子结构中有类似苯环结构,所有原子均满足8电子结构。写出三聚氟氰的结构式
),分子结构中有类似苯环结构,所有原子均满足8电子结构。写出三聚氟氰的结构式(4)2022年10月宁波南大光电ArF光刻胶生产线正式投产,国内7nm芯片制造材料获得重大突破。一种聚碳酸酯胶的曝光分解原理如下:
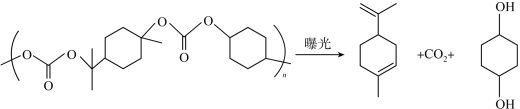
②聚碳酸酯膜曝光后的产物加热可汽化或溶于水,加热汽化或溶于水克服的作用力有
a.配位键 b.离子键 c.范德华力 d.氢键 e.共价键
(5)GaAs是一种制造芯片重要的半导体材料,晶胞结构如图1,将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料,如图2。
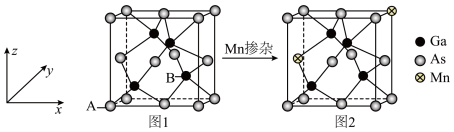
②若GaAs晶体密度为
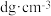 ,设
,设 为阿伏加德罗常数的值,则晶胞中两个As原子间的最小距离为
为阿伏加德罗常数的值,则晶胞中两个As原子间的最小距离为③稀磁性半导体材料中Mn、As的原子个数比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为2NaNH2+N2O=NaN3+NaOH+NH3, 3NaNH2+NaNO3=NaN3+3NaOH+NH3↑。 回答下列问题:
(1)氮元素所在的周期中,电负性最大的元素是___________ ,第一电离能最小的元素是___________ 。
(2)基态氮原子的L层电子排布图为___________ 。
(3)与N 互为等电子体的分子为
互为等电子体的分子为___________ (写出一种),写出NH 的电子式
的电子式___________ 。
(4)叠氮化钠中不含有 的化学键类型有___________ 。
A.离子键 B.极性共价键 C.σ键 D.π键
(5)N2O沸点(-88.49℃)比NH3沸点(-33.34℃)低,其主要原因是___________ 。
(1)氮元素所在的周期中,电负性最大的元素是
(2)基态氮原子的L层电子排布图为
(3)与N
 互为等电子体的分子为
互为等电子体的分子为 的电子式
的电子式(4)叠氮化钠中
A.离子键 B.极性共价键 C.σ键 D.π键
(5)N2O沸点(-88.49℃)比NH3沸点(-33.34℃)低,其主要原因是
您最近一年使用:0次
【推荐1】现有属于前四周期的A、B、C、D、E、F、G七种元素原子序数依次增大。A元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的 ;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)A、B、C三种元素的电负性由大到小的顺序为_______ (用元素符号表示)A、B、C三种元素的简单氢化物的稳定性顺序为:_______ (用化学式表示)。
(2)E原子的结构示意图为_______ 。
(3)F元素位于元素周期表的_______ 区。
(4)G元素可能的性质_______ 。
A.其单质可作为半导体材料 B.其电负性大于磷 C.其原子半径大于锗 D.其第一电离能小于硒
(5)电离能比较:I1(Mg)_______ I1(Al)(填“>”或“<”),其原因_______ 。
 ;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。(1)A、B、C三种元素的电负性由大到小的顺序为
(2)E原子的结构示意图为
(3)F元素位于元素周期表的
(4)G元素可能的性质
A.其单质可作为半导体材料 B.其电负性大于磷 C.其原子半径大于锗 D.其第一电离能小于硒
(5)电离能比较:I1(Mg)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】由两种短周期元素组成的A、B、C、D化合物分子,都含有18个电子,它们分子中所含原子的数目依次为2、3、4、6。A和C分子中的原子个数比均为1∶1,B和D分子中原子个数比均为1∶2。D可作为火箭推进剂的燃料。请回答下列问题:
(1)A、B、C、D分子中相对原子质量较大的四种元素第一电离能由大到小为_______ (填元素符号)。
(2)A与HF相比,其熔、沸点较低,原因是_______ 。
(3)B分子的空间构型为_______ 形,C分子属于_______ (填“极性”或“非极性”)分子。
(4)A、B两分子中心原子的氧化物对应的水化物酸性最强的是_______ (填该含氧酸的化学式)。
(5)D分子中心原子的杂化方式是_______ ,由该中心原子组成的常见单质分子中包含_______ 个 键,与该单质分子互为等电子体的常见分子的结构式为
键,与该单质分子互为等电子体的常见分子的结构式为_______ 。
(1)A、B、C、D分子中相对原子质量较大的四种元素第一电离能由大到小为
(2)A与HF相比,其熔、沸点较低,原因是
(3)B分子的空间构型为
(4)A、B两分子中心原子的氧化物对应的水化物酸性最强的是
(5)D分子中心原子的杂化方式是
 键,与该单质分子互为等电子体的常见分子的结构式为
键,与该单质分子互为等电子体的常见分子的结构式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】请按要求回答:
(1)蓝矾(CuSO4·5H2O)的结构如图所示: 的空间结构是
的空间结构是___________ ,其中S原子的杂化轨道类型是___________ ;
(2)气态SO3分子的空间结构为___________ ;将纯液态SO3冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如图所示,此固态SO3中S原子的杂化轨道类型是___________ 。___________ 。
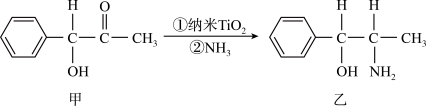
(4)二氧化钛(TiO2)是常用的具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米TiO2催化的一个实例如图所示。___________ ,化合物乙中采取sp3杂化的原子对应元素的第一电离能由小到大的顺序为___________ 。
(1)蓝矾(CuSO4·5H2O)的结构如图所示:
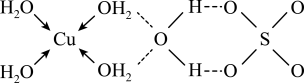
 的空间结构是
的空间结构是(2)气态SO3分子的空间结构为

(4)二氧化钛(TiO2)是常用的具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米TiO2催化的一个实例如图所示。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】短周期主族元素C、N、O、S、Cl在化学与生活中应用广泛,回答下列问题。
(1)基态N原子的电子排布式为___________ ,基态O原子的外围电子排布图为___________ ,S元素在元素周期表的___________ 区。
(2)写出与SO2互为等电子体的一种微粒___________ , Cl2O的空间构型___________ 中心原子的轨道杂化方式为___________ 。
(3)H2O和H2S二者沸点较高的是___________ ,判断的理由是___________ 。CO2与SO2在水中溶解度较大的是___________ ,判断的理由是___________
(4)基态C、N、O第一电离能的大小顺序是___________ ,原因是___________ ,S原子的第一电离能小于第二电离能,请从结构与性质的角度解释其原因___________ 。
(1)基态N原子的电子排布式为
(2)写出与SO2互为等电子体的一种微粒
(3)H2O和H2S二者沸点较高的是
(4)基态C、N、O第一电离能的大小顺序是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】O、S、Cl、Fe、Cu五种元素的单质及其化合物在工农业生产和生活中有着广泛的应用。请回答下列问题:
(1)基态Fe原子价电子的轨道表示式为_______ 。
(2)O、S、Cl的电负性由大到小的顺序是_______ (填元素符号)。
(3)O、S的最简单氢化物中键角较大的是_______ (填化学式),原因是_______ 。
(4) 的空间结构为
的空间结构为_______ 。
(5)O、Cu组成的一种化合物的晶胞结构示意图如下。
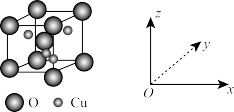
则该化合物的化学式为_______ 。
(1)基态Fe原子价电子的轨道表示式为
(2)O、S、Cl的电负性由大到小的顺序是
(3)O、S的最简单氢化物中键角较大的是
(4)
 的空间结构为
的空间结构为(5)O、Cu组成的一种化合物的晶胞结构示意图如下。

则该化合物的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】阅读资料,获取信息,回答问题。
(A) A、 B、C、D为四种元素,A原子的1S轨道为半充满;在元素周期表中,B的电负性最大;C的原子序数为24;D2+的电子排布式和Ar相同。
(B)两元素电负性差值大于1. 7,原子间一般形成离子键;小于1. 7,原子间一般形成共价键。
(C)下列是周期表中部分元素的电负性x和第一电离能I1 (KJ·mol-1):

(1).A原子的轨道表示式为_______ ,B原子的价电子排布式为________ ,C原子的电
子排布式为___________ ,D在周期表中的位置为________ 周期________ 族。
(2).电负性最小的元素位于______ 族,第一电离能最大的元素是(填元素符号)______ ;
锂元素的电负性取值范围为____ <x(Li)<_____ ;A12S3属______ 化合物
(3)标出化合物OF2、 LiAlH4中各元素的化合价(写在元素符号上)____ 、____ 。
(A) A、 B、C、D为四种元素,A原子的1S轨道为半充满;在元素周期表中,B的电负性最大;C的原子序数为24;D2+的电子排布式和Ar相同。
(B)两元素电负性差值大于1. 7,原子间一般形成离子键;小于1. 7,原子间一般形成共价键。
(C)下列是周期表中部分元素的电负性x和第一电离能I1 (KJ·mol-1):

(1).A原子的轨道表示式为
子排布式为
(2).电负性最小的元素位于
锂元素的电负性取值范围为
(3)标出化合物OF2、 LiAlH4中各元素的化合价(写在元素符号上)
您最近一年使用:0次



