CO2的回收和资源化对于实现“碳中和”具有重要意义。
(1)CH4与CO2重整生成H2和CO的反应为CH4(g)+CO2(g)=2H2(g)+2CO(g) ΔH=+247.6kJ•mol-1
①已知H2(g)和CO(g)的燃烧热分别为285.8kJ•mol-1和283.0kJ•mol-1.则CH4的燃烧热为_______ 。
②CH4与CO2重整过程中还发生反应H2(g)+CO2(g)=H2O(g)+CO(g)ΔH=+41.2kJ•mol-1。在恒压、反应物起始物质的量比n(CH4):n(CO2)=1:1条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。
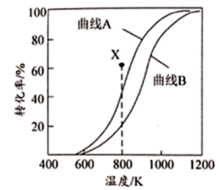
I.曲线_______ (填“A”或“B”)表示CH4的平衡转化率随温度的变化。
Ⅱ.800K、起始n(CH4):n(CO2)=1:1条件下,要让CH4平衡转化率达到X点的值,可以采取的措施是_______ (过程中不充入或分离出任何物质)。
(2)M中存在的粒子有Na+、A2-、HA-、H+、OH-、H2O和H2A。根据题意回答下列问题:
①H2A为_______ 酸(填“强”或“弱”),往H2A溶液中加水会使 的值
的值_______ (填“增大”、“减小”或“不变”)。
②往Na2A溶液中加入_______ 可抑制其水解(选填字母序号)。
a.浓盐酸 b.KOH固体 c.水 d.升高温度
③浓度均为0.1mol·L-1的Na2A、NaHA混合溶液中: =
=_______ 。
(1)CH4与CO2重整生成H2和CO的反应为CH4(g)+CO2(g)=2H2(g)+2CO(g) ΔH=+247.6kJ•mol-1
①已知H2(g)和CO(g)的燃烧热分别为285.8kJ•mol-1和283.0kJ•mol-1.则CH4的燃烧热为
②CH4与CO2重整过程中还发生反应H2(g)+CO2(g)=H2O(g)+CO(g)ΔH=+41.2kJ•mol-1。在恒压、反应物起始物质的量比n(CH4):n(CO2)=1:1条件下,CH4和CO2的平衡转化率随温度变化的曲线如图所示。

I.曲线
Ⅱ.800K、起始n(CH4):n(CO2)=1:1条件下,要让CH4平衡转化率达到X点的值,可以采取的措施是
(2)M中存在的粒子有Na+、A2-、HA-、H+、OH-、H2O和H2A。根据题意回答下列问题:
①H2A为
 的值
的值②往Na2A溶液中加入
a.浓盐酸 b.KOH固体 c.水 d.升高温度
③浓度均为0.1mol·L-1的Na2A、NaHA混合溶液中:
 =
=
更新时间:2024-03-16 08:41:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示。[已知:2SO2(g)+O2(g) 2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
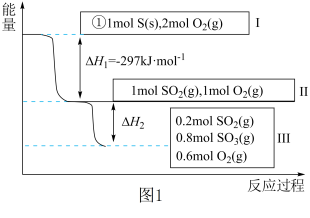
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:___________ 。
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有___________。
(3)恒温恒容时,1mol SO2和2mol O2充分反应,放出热量的数值比|ΔH2|___________ (填“大”、“小”或“相等”)。
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是___________ ;图中表示平衡混合物中SO3的含量最高的一段时间是___________ 。

 2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有___________。
| A.升高温度 | B.充入He | C.再充入1mol SO2(g)和1mol O2(g) | D.使用催化剂 |
(3)恒温恒容时,1mol SO2和2mol O2充分反应,放出热量的数值比|ΔH2|
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知下列热化学方程式:①H2(g)+1/2O2(g)=H2O(l)ΔH=-285kJ·mol-1,②H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8kJ·mol-1,③C(s)+1/2O2(g)=CO(g)ΔH=-110.5kJ·mol-1,④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1,回答下列问题:
(1)H2燃烧热的热化学方程式为___________ ;C燃烧热的热化学方程式为___________ 。(选数字)
(2)燃烧1gH2生成液态水,放出的热量为_________________ 。
(3)液态水的稳定性_______ 气态水的稳定性(填“大于”、“小于”、“等于”)。。
(1)H2燃烧热的热化学方程式为
(2)燃烧1gH2生成液态水,放出的热量为
(3)液态水的稳定性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】碳是形成化合物种类最多的元素,其单质及其部分化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程:
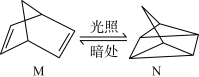 ΔH=+88.6kJ·mol-1,则M、N相比,较稳定的是
ΔH=+88.6kJ·mol-1,则M、N相比,较稳定的是__________ 。
(2)随着人们对环保的重视程度日益提高,乙醇在某些行业作为燃料被广泛应用。下列有关乙醇作为燃料的说法正确的是________ 。
①燃烧时只发生氧化反应 ②充分燃烧的产物不污染环境
③乙醇是一种可再生能源 ④燃烧时放出大量的热
A.①②③ B.①②④ C.①③④ D.②③④
(3)CCS技术是将工业和有关能源产业中所产生的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天然气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:
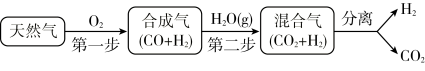
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1 g CH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式___________________________________________________________ 。
(1)有机物M经过太阳光光照可转化成N,转化过程:
 ΔH=+88.6kJ·mol-1,则M、N相比,较稳定的是
ΔH=+88.6kJ·mol-1,则M、N相比,较稳定的是(2)随着人们对环保的重视程度日益提高,乙醇在某些行业作为燃料被广泛应用。下列有关乙醇作为燃料的说法正确的是
①燃烧时只发生氧化反应 ②充分燃烧的产物不污染环境
③乙醇是一种可再生能源 ④燃烧时放出大量的热
A.①②③ B.①②④ C.①③④ D.②③④
(3)CCS技术是将工业和有关能源产业中所产生的CO2进行捕捉与封存的技术,被认为是拯救地球、应对全球气候变化最重要的手段之一。其中一种以天然气为燃料的“燃烧前捕获系统”的简单流程图如图所示(部分条件及物质未标出)。回答下列问题:
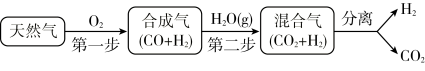
CH4在催化剂作用下实现第一步,也叫CH4不完全燃烧,1 g CH4不完全燃烧反应放出2.21kJ热量,写出该反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】含硫化合物在生产、生活中有广泛应用,其吸收和处理也十分重要。回答下列问题:
1.SO2具有还原性,写出将SO2气体通入 FeCl3溶液中的离子方程式_________ ,并标出电子转移的数目及方向。_____________________________________________________________
2.在Na2SO3溶液中滴加酚酞,溶液变红色,若在该溶液中滴入过量的BaCl2溶液,现象是_________ ,请结合离子方程式,运用平衡原理进行解释_____________________ 。
3.等体积等物质的量浓度的 NaClO溶液与Na2SO3溶液混合后,溶液显______ 性。此时溶液中浓度相等的微粒是___________________________________________ 。
4.已知:H2S:Ki1=1.3×10-7Ki2=7.1×10-15 H2CO3:Ki1=4.3×10-7Ki2=5.6×10-11
含H2S尾气用足量的Na2CO3溶液来吸收。写出离子反应方程式。____________
常温时,等体积等浓度的Na2S和Na2CO3溶液的离子总数:N前___ N后(填“>”或“<”)。
1.SO2具有还原性,写出将SO2气体通入 FeCl3溶液中的离子方程式
2.在Na2SO3溶液中滴加酚酞,溶液变红色,若在该溶液中滴入过量的BaCl2溶液,现象是
3.等体积等物质的量浓度的 NaClO溶液与Na2SO3溶液混合后,溶液显
4.已知:H2S:Ki1=1.3×10-7Ki2=7.1×10-15 H2CO3:Ki1=4.3×10-7Ki2=5.6×10-11
含H2S尾气用足量的Na2CO3溶液来吸收。写出离子反应方程式。
常温时,等体积等浓度的Na2S和Na2CO3溶液的离子总数:N前
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】10℃时,在烧杯中加入0.1mol·L-1的NaHCO3溶液400mL,加热,测得该溶液的pH发生如下变化:
(1)甲同学认为,该溶液的pH升高的原因是HCO 的水解程度增大,故碱性增强,该反应的离子方程式为
的水解程度增大,故碱性增强,该反应的离子方程式为_____ 。
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解生成了Na2CO3,并推断Na2CO3的水解程度_____ (填“大于”或“小于”)NaHCO3。
(3)丙同学认为:要确定上述哪种说法合理,只要把加热后的溶液冷却到10℃后再测定溶液pH,若pH_____ 8.3(填“>”“<”或“=”),说明甲正确;若pH____ 8.3(填“>”“<”或“=”),说明乙正确。
(4)丁同学设计如图实验方案对甲、乙同学的解释进行判断:实验装置如图,加热煮沸NaHCO3溶液,发现试管A中澄清石灰水变浑浊,说明____ (填“甲”或“乙”)推测正确。

(5)将一定体积0.1mol·L-1的NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为9.8;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为10.1。据此资料可以判断____ (填“甲”或“乙”)推测正确,原因是____ 。
| 温度/℃ | 10 | 20 | 30 | 50 | 70 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 |
 的水解程度增大,故碱性增强,该反应的离子方程式为
的水解程度增大,故碱性增强,该反应的离子方程式为(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解生成了Na2CO3,并推断Na2CO3的水解程度
(3)丙同学认为:要确定上述哪种说法合理,只要把加热后的溶液冷却到10℃后再测定溶液pH,若pH
(4)丁同学设计如图实验方案对甲、乙同学的解释进行判断:实验装置如图,加热煮沸NaHCO3溶液,发现试管A中澄清石灰水变浑浊,说明

(5)将一定体积0.1mol·L-1的NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为9.8;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为10.1。据此资料可以判断
您最近一年使用:0次



