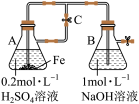
纳米铁粉具有较强的还原性和吸附性。利用纳米铁粉去除水体中 (Ⅵ)的反应机理及
(Ⅵ)的反应机理及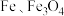 和
和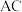 (碳)按不同配比在相同条件对
(碳)按不同配比在相同条件对 (Ⅵ)的去除效果如图所示,反应过程中除
(Ⅵ)的去除效果如图所示,反应过程中除 外无其它气体产生,下列说法正确的是
外无其它气体产生,下列说法正确的是
 (Ⅵ)的反应机理及
(Ⅵ)的反应机理及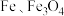 和
和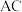 (碳)按不同配比在相同条件对
(碳)按不同配比在相同条件对 (Ⅵ)的去除效果如图所示,反应过程中除
(Ⅵ)的去除效果如图所示,反应过程中除 外无其它气体产生,下列说法正确的是
外无其它气体产生,下列说法正确的是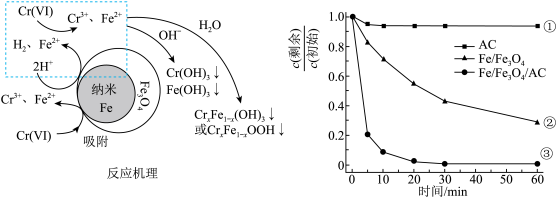
A. (Ⅵ)转化为 (Ⅵ)转化为 (Ⅲ)的途径有2种 (Ⅲ)的途径有2种 |
B.①中去除 (Ⅵ)是因为碳粉在纳米条件下还原 (Ⅵ)是因为碳粉在纳米条件下还原 (Ⅵ) (Ⅵ) |
| C.③比②去除速率快的主要原因是形成原电池 |
D. 与 与 共沉淀的离子方程式为 共沉淀的离子方程式为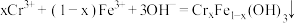 |
2024·山东潍坊·一模 查看更多[2]
更新时间:2024-03-15 16:27:37
|
相似题推荐
【推荐1】污水处理厂处理含CN-废水的过程分两步进行:①向含CN-的废水中加入过量NaClO将CN-转化为CNO-;②调节①所得溶液为酸性,使CNO-继续被NaClO转化为两种无污染的气体。下列关于上述过程的叙述错误的是( )
A.CN-的电子式为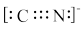 |
| B.过程①中,生成CNO-的反应中氧化剂与还原剂的物质的量之比为1:1 |
| C.过程②中,生成的两种无污染的气体为CO2和N2 |
| D.氧化性:CNO->C1O- |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】工业上制取高铁酸钾(K2FeO4),是先制取高铁酸钠,然后在低温下,往高铁酸钠溶液中加入KOH至饱和就可以析出高铁酸钾。湿法制备Na2FeO4的主要反应为:2Fe(OH)3+3ClO-+4OH-═2FeO +3Cl-+5H2O干法制备Na2FeO4的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2SO4+O2↑。下列有关说法不正确的是
+3Cl-+5H2O干法制备Na2FeO4的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2SO4+O2↑。下列有关说法不正确的是
 +3Cl-+5H2O干法制备Na2FeO4的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2SO4+O2↑。下列有关说法不正确的是
+3Cl-+5H2O干法制备Na2FeO4的主要反应为:2FeSO4+6Na2O2═2Na2FeO4+2Na2SO4+O2↑。下列有关说法不正确的是| A.湿法与干法制备中,各生成1molNa2FeO4,转移电子的物质的量的比为3:4 |
| B.高铁酸钾在低温下的溶解度比高铁酸钠的溶解度小 |
| C.干法制备的主要反应中Na2O2的作用只是氧化剂 |
| D.K2FeO4处理水时,既能杀菌消毒,生成的Fe(OH)3胶体还能吸附水中的悬浮杂质 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】过渡元素在生活、生产和科技等方面有广泛的用途。现代污水处理工艺中常利用聚合铁{简称PFS,化学式为:[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是
| 元素 | Mn | Fe | |
| 电离能(kJ·mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
| A.PFS中铁显+3价 |
| B.二价铁离子的价电子排布式是3d44s2 |
| C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程 |
| D.由表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述正确的是
| A.KSp[MgF2]>KSp[Mg(OH)2],不能实现Mg(OH)2转化为MgF2。 |
| B.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
| C.等物质的量浓度的NH4Cl溶液和NH4HSO4溶液,后者的c(NH4+)大 |
| D.FeCl3与KSCN反应达到平衡时,加入KCl溶液,则溶液颜色变深 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于Fe3+、Fe2+性质实验的说法正确的是( )
| A.用如图装置不可以制备沉淀Fe(OH)2
|
| B.配制FeCl3溶液时,直接将FeCl3晶体溶于水即可 |
| C.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,此现象确定溶液中含有Fe2+ |
| D.向FeCl2溶液中加入少量铁粉是为了防止Fe2+被氧化 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列说法正确的是
| A.配制Fe(NO3)2溶液时,向溶液中滴加几滴稀硝酸,以防止Fe(NO3)2发生水解 |
| B.向二氧化硫水溶液中滴加氯化钡溶液,再滴加双氧水,产生白色沉淀 |
| C.中和热的测定实验中,测酸后的温度计未用水清洗便立即去测碱的浓度,所测中和热的数值偏小 |
| D.配制1mol·L-1的NH4NO3溶液时,溶解后立即转移至容量瓶,所配溶液浓度偏高 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作能达到目的的是
| 选项 | 操作 | 目的 |
| A | 除去 中的 中的 杂质 杂质 | 向混合物中加入足量NaOH溶液,充分反应后过滤、洗涤、干燥 |
| B | 测定相同浓度的HCl溶液、HBr溶液的pH | 比较Cl和Br的非金属性强弱 |
| C | 将相同大小的镁片和铝片用导线连接,插入NaOH溶液中 | 证明原电池中活泼性较强的金属作负极 |
| D | 向蔗糖溶液中加入新制的银氨溶液,水浴加热 | 证明蔗糖是非还原性糖 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】一种全天候太阳能电池光照时的工作原理如图所示。

下列说法不正确的是

下列说法不正确的是
| A.硅太阳能电池供电原理与该电池相同 |
| B.光照时,b极的电极反应式为VO2+﹣e-+H2O=VO2++2H+ |
| C.光照时,每转移1mol电子,有2molH+由b极区经质子交换膜向a极区迁移 |
| D.夜间时,该电池相当于蓄电池放电,a极发生氧化反应 |
您最近一年使用:0次