用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间结构,也可推测键角大小,下列判断错误的是
A. 是V形分子 是V形分子 | B. 键角大于 键角大于 的 的 |
C. 是直线形分子 是直线形分子 | D. 和 和 的空间结构相同 的空间结构相同 |
更新时间:2024-03-24 12:48:18
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列有关二氯化锡(SnCl2)分子的说法正确的是
| A.有一个σ键、一个π键 | B.是直线形分子 |
| C.中心原子Sn是sp2杂化 | D.键角等于120° |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】四氯化碳是常用的不燃溶剂,由如下反应制备: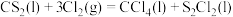 。下列说法正确的是
。下列说法正确的是
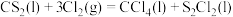 。下列说法正确的是
。下列说法正确的是| A.CS2的熔沸点比CO2的低 | B.CCl4的热稳定性比CF4的高 |
| C.该制备反应是熵增过程 | D.CS2的键角大于CCl4的键角 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】 、
、 、
、 等含磷化合物是重要的化工原料,其中
等含磷化合物是重要的化工原料,其中 经常以
经常以 的形式存在。
的形式存在。 的分子空间结构具有对称性,模型如图所示(其中短线代表单键或双键),下列说法错误的是
的分子空间结构具有对称性,模型如图所示(其中短线代表单键或双键),下列说法错误的是
 、
、 、
、 等含磷化合物是重要的化工原料,其中
等含磷化合物是重要的化工原料,其中 经常以
经常以 的形式存在。
的形式存在。 的分子空间结构具有对称性,模型如图所示(其中短线代表单键或双键),下列说法错误的是
的分子空间结构具有对称性,模型如图所示(其中短线代表单键或双键),下列说法错误的是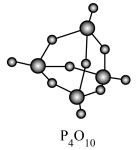
A. 中含有σ键和π键 中含有σ键和π键 |
B. 是非极性分子 是非极性分子 |
C. 分子的空间构型为三角锥形 分子的空间构型为三角锥形 |
D. 中所有原子都满足 中所有原子都满足 稳定结构 稳定结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】当将钼酸铵和磷酸盐的溶液进行酸化时,得到一种黄色沉淀12-磷钼酸铵,可利用该原理进行磷酸盐的定量测定,反应为 。下列有关说法错误的是
。下列有关说法错误的是
 。下列有关说法错误的是
。下列有关说法错误的是| A.电负性:O>N>P>H |
B. 与Cr同族,基态Mo原子的价层电子表示式为 与Cr同族,基态Mo原子的价层电子表示式为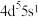 |
C. 中H-N-H的键角比 中H-N-H的键角比 中H-N-H的键角大 中H-N-H的键角大 |
D. 和 和 的空间结构均为正四面体形 的空间结构均为正四面体形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关说法正确的是
| A.HCl与NaCl的晶体类型相同 |
B. 与 与 中的O—Cl—O夹角都为109°28' 中的O—Cl—O夹角都为109°28' |
| C.CuCl2中Cu2+核外电子排布式为[Ar]3d9 |
| D.Cl2O与HClO都是由极性键构成的非极性分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
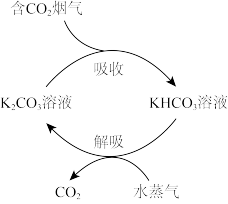
【推荐1】一种富集烟气(水蒸气、 、
、 等)中
等)中 的原理示意图如下。下列说法错误的是
的原理示意图如下。下列说法错误的是
 、
、 等)中
等)中 的原理示意图如下。下列说法错误的是
的原理示意图如下。下列说法错误的是
A. 分子的空间构型为直线形 分子的空间构型为直线形 |
B. 中碳原子的杂化方式为 中碳原子的杂化方式为 |
C. 的键角小于 的键角小于 的键角 的键角 |
D. 易溶于水是因为 易溶于水是因为 分子能与 分子能与 分子形成分子间氢键 分子形成分子间氢键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】工业制备硫酸可通过反应 制得
制得 。下列说法正确的是
。下列说法正确的是
 制得
制得 。下列说法正确的是
。下列说法正确的是A. 的电子数为26 的电子数为26 | B. 的电子式为 的电子式为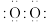 |
C. 属于离子化合物,仅含离子键 属于离子化合物,仅含离子键 | D. 的空间填充模型为 的空间填充模型为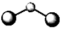 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2;元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。X、Y形成的化合物晶体有两种常见的晶胞,如图所示。下列说法错误是
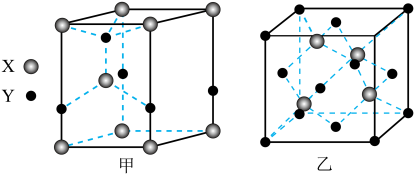

| A.Y元素位于周期表中第三周期第ⅥA族 |
B.由晶胞甲和晶胞乙推知该化合物的化学式为 |
C.元素电负性的关系是: |
D.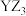 的空间结构为平面三角形 的空间结构为平面三角形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 发生催化氧化反应生成NO,强碱条件下能被NaClO氧化生成
发生催化氧化反应生成NO,强碱条件下能被NaClO氧化生成 ;
; 可被NaClO继续氧化生成
可被NaClO继续氧化生成 ,也可被
,也可被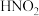 氧化生成
氧化生成 ,
, 能与
能与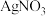 溶液反应产生银镜;
溶液反应产生银镜; 是一种弱酸,酸性与醋酸相当。下列有关含氮化合物的性质与制备,说法正确的是
是一种弱酸,酸性与醋酸相当。下列有关含氮化合物的性质与制备,说法正确的是
 发生催化氧化反应生成NO,强碱条件下能被NaClO氧化生成
发生催化氧化反应生成NO,强碱条件下能被NaClO氧化生成 ;
; 可被NaClO继续氧化生成
可被NaClO继续氧化生成 ,也可被
,也可被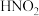 氧化生成
氧化生成 ,
, 能与
能与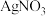 溶液反应产生银镜;
溶液反应产生银镜; 是一种弱酸,酸性与醋酸相当。下列有关含氮化合物的性质与制备,说法正确的是
是一种弱酸,酸性与醋酸相当。下列有关含氮化合物的性质与制备,说法正确的是A.分析结构可推得, 难溶于水 难溶于水 |
B. 、 、 中N原子都采取 中N原子都采取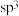 杂化 杂化 |
C.制备 时应将 时应将 慢慢通入强碱性的NaClO溶液中 慢慢通入强碱性的NaClO溶液中 |
D.可向 溶液中通 溶液中通 来制备 来制备 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】 、
、 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在
属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在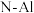 键、
键、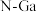 键。下列说法错误的是
键。下列说法错误的是
 、
、 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在
属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在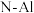 键、
键、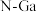 键。下列说法错误的是
键。下列说法错误的是A. 的熔点高于 的熔点高于 | B.晶体中所有化学键均为极性键 |
C.晶体中所有原子均采取 杂化 杂化 | D.晶体中所有原子的配位数均相同 |
您最近一年使用:0次

 、
、 是大气中主要的污染气体。随着人们环保意识的增强,燃油汽车都已经装上了尾气处理装置。汽车尾气在催化剂作用下可发生如下反应:
是大气中主要的污染气体。随着人们环保意识的增强,燃油汽车都已经装上了尾气处理装置。汽车尾气在催化剂作用下可发生如下反应: 。下列关于
。下列关于 的说法正确的是
的说法正确的是

