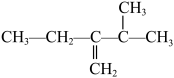
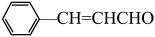按要求完成下列小题。
(1)Cu2+基态核外电子排布式为_______ 。
(2)我国科研人员研制出了M-LiH(M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度,压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Mn原子未成对的电子数为_______ 。
②第三电离能I3(Fe)<I3(Mn),原因是_______ 。
(3)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O分子比NH3分子稳定的原因为_______
②H2O分子的空间结构分别是_______ ,键角H2O_______ NH3。(填>、<或=)
(1)Cu2+基态核外电子排布式为
(2)我国科研人员研制出了M-LiH(M为Fe、Mn等金属)等催化剂,使得合成氨工业的温度,压强分别降到了350℃、1MPa,这是近年来合成氨反应研究中的重要突破。
①基态Mn原子未成对的电子数为
②第三电离能I3(Fe)<I3(Mn),原因是
(3)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O分子比NH3分子稳定的原因为
②H2O分子的空间结构分别是
更新时间:2024-03-26 07:58:53
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大且总和为24。则W、X、Y、Z分别为___________ 。


您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W是原子序数依次增大的短周期主族元素。通常状况下,X与W元素均能形成-1价的气态氢化物,Y为同周期主族元素中原子半径最大的元素,X、Z和W的原子最外层电子数之和为20。回答下列问题:
(1) W在元素周期表中的位置是__________ 。
(2)X和Y元素简单离子的半径较大的是________ (填离子符号);Z和W元素气态氢化物的稳定性较弱的是__________ (填化学式)。
(3)Y的氧化物中既含离子键又含共价键的是__________ (用电子式表示)。
(4)Z的最高价氧化物对应水化物的浓溶液(过量)和氧化亚铜共热,反应的化学方程式为________ 。
(1) W在元素周期表中的位置是
(2)X和Y元素简单离子的半径较大的是
(3)Y的氧化物中既含离子键又含共价键的是
(4)Z的最高价氧化物对应水化物的浓溶液(过量)和氧化亚铜共热,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】试分析下列各种情况下微粒间作用力的变化情况(填“离子键”“极性键”“非极性键”或“分子间作用力”):
(1)NaCl溶于水时破坏___________________________________ ;
(2)HCl溶于水时破坏____________________________________ ;
(3)SO2溶于水时破坏____________________________________ ;
(4)酒精溶于水时破坏____________________________________ ;
(5)NaOH和HCl反应时形成_______ 和_______ ;
(6)反应2H2+O2=2H2O中,被破坏的是________ ,形成的是________ ;
(7)CaCl2和Na2CO3反应时,被破坏的化学键有________ ,形成的化学键有________ ;
(8)Na2O熔化时被破坏的是________ 。
(1)NaCl溶于水时破坏
(2)HCl溶于水时破坏
(3)SO2溶于水时破坏
(4)酒精溶于水时破坏
(5)NaOH和HCl反应时形成
(6)反应2H2+O2=2H2O中,被破坏的是
(7)CaCl2和Na2CO3反应时,被破坏的化学键有
(8)Na2O熔化时被破坏的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Na、Mg、C、N、O、S、Cl等元素单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧产生的黄光是一种___________ 光谱(填“发射”或“吸收”)。
(2)基态碳原子核外电子排布式为___________ ,共有___________ 种能量不同的轨道,其原子核外未成对电子数为___________ 。
(3)N、O、Mg元素的前3级电离能如下表所示:
①、②、③中为氮元素的是___________ (填序号),判断理由是___________ 。
(4)用一个离子方程式说明氯元素和硫元素非金属性的相对强弱:___________ 。
(1)钠在火焰上灼烧产生的黄光是一种
(2)基态碳原子核外电子排布式为
(3)N、O、Mg元素的前3级电离能如下表所示:
| 元素 | 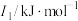 | 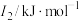 | 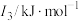 |
| ① | 737.7 | 1450.7 | 7732.7 |
| ② | 1313.9 | 3388.3 | 5300.5 |
| ③ | 1402.3 | 2856.0 | 4578.1 |
(4)用一个离子方程式说明氯元素和硫元素非金属性的相对强弱:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请完成下列各题:
(1)前四周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有_______ 种。
(2)请写出Cr元素的核外电子排布式_______ 。
(3)某元素的正三价离子的3d能级为半充满,该元素的元素名称为_______ ,其单质在一定条件下能与S反应,试写出该反应的化学方程式_______ 。
(4)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的电子排布图为_______ 。
(1)前四周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有
(2)请写出Cr元素的核外电子排布式
(3)某元素的正三价离子的3d能级为半充满,该元素的元素名称为
(4)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的电子排布图为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)下列物质变化,只与范德华力有关的是___ 。
A.干冰熔化 B.乙酸汽化 C.乙醇溶于水 D.碘溶于四氯化碳
(2)下面是s能级与p能级的原子轨道图:
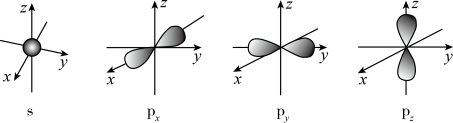
请回答下列问题:
s电子的原子轨道呈__ 形,每个s能级有__ 个原子轨道;p电子的原子轨道呈___ 形,每个p能级有___ 个原子轨道.
(3)Na、Mg、Al第一电离能的由大到小的顺序:___ 。
(4)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列:
①2s ②3d ③4s ④3s ⑤4p ⑥3p
轨道能量由低到高排列顺序是___ 。
A.干冰熔化 B.乙酸汽化 C.乙醇溶于水 D.碘溶于四氯化碳
(2)下面是s能级与p能级的原子轨道图:

请回答下列问题:
s电子的原子轨道呈
(3)Na、Mg、Al第一电离能的由大到小的顺序:
(4)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列:
①2s ②3d ③4s ④3s ⑤4p ⑥3p
轨道能量由低到高排列顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】原子结构与元素周期表存在着内在联系。根据已学知识,请回答下列问题:
(1)基态N原子电子占据___________ 个能层,电子占据的最高能级的符号是___________ ;基态N原子共有___________ 种不同空间运动状态的电子。
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:___________ ,位于元素周期表的___________ 区。
(3)比较Cu和Zn的第二电离能大小[用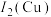 和
和 表示]:
表示]:___________ 。
(4)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填选项)。
(5)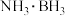 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(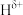 ),与B原子相连的H负电性(
),与B原子相连的H负电性(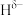 )。在H、B、N三种元素中,电负性由大到小的顺序是
)。在H、B、N三种元素中,电负性由大到小的顺序是___________ 。
(1)基态N原子电子占据
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:
(3)比较Cu和Zn的第二电离能大小[用
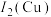 和
和 表示]:
表示]:(4)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填选项)。
A.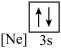 | B.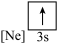 | C. | D.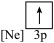 |
(5)
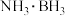 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(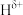 ),与B原子相连的H负电性(
),与B原子相连的H负电性(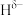 )。在H、B、N三种元素中,电负性由大到小的顺序是
)。在H、B、N三种元素中,电负性由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】磷酸亚铁锂( )可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用
)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用 、
、 等作为原料制备。请回答下列问题:
等作为原料制备。请回答下列问题:
(1)P在元素周期表中的位置为___________ 。
(2)基态 原子的价层电子排布式为
原子的价层电子排布式为___________ ,基态 与
与 中未成对的电子数之比为
中未成对的电子数之比为___________ 。
(3)基态 原子的核外电子有
原子的核外电子有___________ 种空间运动状态,其能量最高的电子的电子云轮廓图为___________ 。
(4)组成 ,的非金属元素中,N、P、O的电负性由大到小的顺序为
,的非金属元素中,N、P、O的电负性由大到小的顺序为___________ (填元素符号);第一电离能:N___________ (填“>”或“<”)O,原因是___________ 。
 )可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用
)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用 、
、 等作为原料制备。请回答下列问题:
等作为原料制备。请回答下列问题:(1)P在元素周期表中的位置为
(2)基态
 原子的价层电子排布式为
原子的价层电子排布式为 与
与 中未成对的电子数之比为
中未成对的电子数之比为(3)基态
 原子的核外电子有
原子的核外电子有(4)组成
 ,的非金属元素中,N、P、O的电负性由大到小的顺序为
,的非金属元素中,N、P、O的电负性由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】键角
①定义:在多原子分子中,两个_______ 之间的夹角称为键角。

②常见分子的键角:
③意义:键角可反映分子的空间构型,是描述分子结构的重要参数,多原子分子的键角一定,表明共价键具有_______ 。
①定义:在多原子分子中,两个

②常见分子的键角:
| 分子式 | 键角 | 分子空间构型 |
| CO2 | 180° | 直线形 |
| H2O | 105° | V形 |
| NH3 | 107° | 三角锥形 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硒化物(如KCu4Se8)可用于太阳能电池、光传感器、热电发电与制冷等。回答下列问题:
(1)K与Cu位于同周期,金属钾的熔点比铜的低,这是因为___________ 。
(2)O、S、Se均位于元素周期表第ⅥA族,它们的氢化物H2O、H2S及H2Se分子的键角从大到小顺序为___________ 。
(3)配合物[Cu(CH3CN)4]BF4中,阴离子的空间构型为___________ ,配合离子中与Cu(Ⅱ)形成配位键的原子是___________ ,配体中碳原子的杂化方式是___________ 。
(4)TMTSF( )中共价键的类型是
)中共价键的类型是___________ 。
(1)K与Cu位于同周期,金属钾的熔点比铜的低,这是因为
(2)O、S、Se均位于元素周期表第ⅥA族,它们的氢化物H2O、H2S及H2Se分子的键角从大到小顺序为
(3)配合物[Cu(CH3CN)4]BF4中,阴离子的空间构型为
(4)TMTSF(
 )中共价键的类型是
)中共价键的类型是
您最近一年使用:0次