过渡金属及其化合物在生产、生活中有重要的应用。回答下列问题:
(1)一种含Ti的催化剂X能催化乙烯、丙烯等的聚合,其结构如图所示。X中C原子的杂化类型有________ ,含有的作用力类型有________ (填字母),非金属元素电负性由大到小的顺序为________ 。
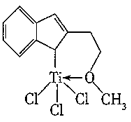
A.π键 B.氢键 C.配位键 D.σ键 E.离子键
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于_______ (填晶体类型)。Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=_______ 。
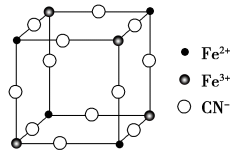
(3)有一种蓝色晶体可表示为MxFey(CN)6,经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上。其晶体中阴离子的最小结构单元如图所示,通过计算x和y的数值,可进一步确定该晶体的化学式为_______ ,该晶体属于_______ 晶体,M呈_______ 价。
(1)一种含Ti的催化剂X能催化乙烯、丙烯等的聚合,其结构如图所示。X中C原子的杂化类型有

A.π键 B.氢键 C.配位键 D.σ键 E.离子键
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于
(3)有一种蓝色晶体可表示为MxFey(CN)6,经X射线研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上。其晶体中阴离子的最小结构单元如图所示,通过计算x和y的数值,可进一步确定该晶体的化学式为

更新时间:2024-03-26 10:02:16
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】原子序数依次递增且都小于36的A、B、C、D、E五种元素,其中A的一种核素中没有中子,B原子基态时最外层电子数是其内层电子数的2倍,D原子基态时2p原子轨道上有2个未成对的电子,E元素的原子结构中3d能级上未成对电子数是成对电子数的2倍。回答下列问题:
(1)A、B、C、D四种元素的电负性从大到小的顺序为___________ (用元素符号表示);化合物 的沸点比化合物
的沸点比化合物 的高,其主要原因是
的高,其主要原因是___________ 。
(2)元素E能形成多种配合物,如: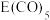 等。
等。
①基态E原子的价电子排布式为___________ 。
②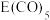 常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断
常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断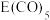 晶体属于
晶体属于___________ (填晶体类型),该晶体中E的化合价为___________ 。
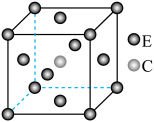
(3)E和C形成的一种化合物的晶胞结构如图所示,该晶胞的化学式为___________ 。若两个最近的E原子间的距离为 ,则该晶体的密度是
,则该晶体的密度是___________  。
。
(1)A、B、C、D四种元素的电负性从大到小的顺序为
 的沸点比化合物
的沸点比化合物 的高,其主要原因是
的高,其主要原因是(2)元素E能形成多种配合物,如:
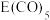 等。
等。①基态E原子的价电子排布式为
②
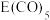 常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断
常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断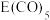 晶体属于
晶体属于(3)E和C形成的一种化合物的晶胞结构如图所示,该晶胞的化学式为
 ,则该晶体的密度是
,则该晶体的密度是 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】元素X、Y、Z、T、R的原子序数依次增大且小于20,其最外层电子数与原子半径间大大小关系如图所示。
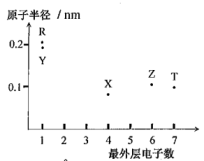
请按要求回答下列问题:
(1)写出基态R原子的价层电子排布式:_______ 。
(2)上述五种元素中,电负性最大的是(写元素符号,下同)_______ ,第一电离能最小的是_______ 。
(3)Z所在主族元素的氢化物中,其中稳定性最强是(用化学式表示)_______ 。
(4)向Y的最高价氧化物的水溶液中充入少量Z的氢化物,写出反应的离子方程式为_______ 。
(5)某化学兴趣小组为探究涉及上述元素性质的变化规律,设计了以下系列实验。
①甲同学欲探究同主族部分元素性质的递变规律,以元素Y、R为例,请完成其实验步骤:_______ 。通过观察现象得出的结论:相同条件下,同主族元素R的金属性比Y的强。
②乙同学欲探究第三周期部分元素性质的递变规律,以元素Z、T为例,自拟通过一步反应实现实验目的,其原理的化学方程式为:_______ 。欲观察到现象为:_______ ;结论:_______ 。

请按要求回答下列问题:
(1)写出基态R原子的价层电子排布式:
(2)上述五种元素中,电负性最大的是(写元素符号,下同)
(3)Z所在主族元素的氢化物中,其中稳定性最强是(用化学式表示)
(4)向Y的最高价氧化物的水溶液中充入少量Z的氢化物,写出反应的离子方程式为
(5)某化学兴趣小组为探究涉及上述元素性质的变化规律,设计了以下系列实验。
①甲同学欲探究同主族部分元素性质的递变规律,以元素Y、R为例,请完成其实验步骤:
②乙同学欲探究第三周期部分元素性质的递变规律,以元素Z、T为例,自拟通过一步反应实现实验目的,其原理的化学方程式为:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铜是人类最早使用的金属之一,用黄铜矿(主要成分为CuFeS2)生产粗铜的反应原理如下:
CuFeS2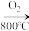 Cu2S
Cu2S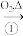 Cu2O
Cu2O Cu
Cu
回答下列问题:
(1)第三周期主族元素中电负性比S小的元素有___________ 种,H2S 分子的空间结构名称为___________ ,H2S的沸点比H2O的___________ (填“高”或“低”),原因是___________ 。
(2)Cu2O和Cu2S均为___________ 晶体,Cu2O 的熔点为1235 °C ,Cu2S的熔点为1130 °C ,Cu2O熔点较高的原因是___________ 。
(3)反应①、②中会生成气体SO2,其中心原子的杂化方式为___________ 。
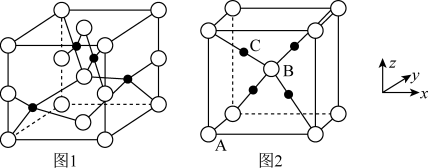
(4)铜的两种氧化物的晶胞如图1、图2所示,图1表示___________ (填化学式),图2中,A原子坐标参数为(0,0,0),B原子为( ,
, ,
, )则C原子的坐标参数为
)则C原子的坐标参数为____ 。 若图2表示的晶体的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则图2晶胞中Cu原子与O原子之间的最小距离为____ (用含ρ和NA的式子表示)pm。
CuFeS2
 Cu2S
Cu2S Cu2O
Cu2O Cu
Cu回答下列问题:
(1)第三周期主族元素中电负性比S小的元素有
(2)Cu2O和Cu2S均为
(3)反应①、②中会生成气体SO2,其中心原子的杂化方式为
(4)铜的两种氧化物的晶胞如图1、图2所示,图1表示
 ,
, ,
, )则C原子的坐标参数为
)则C原子的坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】钴元素是三元锂离子电池阳极材料的重要成分。请回答下列问题:
(1)钴元素在周期表中的位置是_______ ,其价电子排布式为______ 。
(2)第四电离能大小:I4(Fe)> I4(Co),从原子结构的角度分析可能的原因是____ 。
(3)取1mol配合物CoCl3·6NH3(黄色)溶于水,加入足量硝酸银溶液,产生3mol白色沉淀,沉淀不溶于稀硝酸。原配合物中络离子形状为正八面体。
①根据上述事实推测原配合物中络离子化学式为_______ 。
②该配合物在热NaOH溶液中发生反应,并释放出气体,该反应的化学方程式_____ ;生成气体分子的中心原子杂化方式为____ 。
(4)经X射线衍射测定发现,晶体钴在417℃以上堆积方式的剖面图如图所示,则该堆积方式属于_____ ,若该堆积方式下钴原子的半径为r,则该晶体的空间利用率为______ (列出表达式并写出最终结果)。

(1)钴元素在周期表中的位置是
(2)第四电离能大小:I4(Fe)> I4(Co),从原子结构的角度分析可能的原因是
(3)取1mol配合物CoCl3·6NH3(黄色)溶于水,加入足量硝酸银溶液,产生3mol白色沉淀,沉淀不溶于稀硝酸。原配合物中络离子形状为正八面体。
①根据上述事实推测原配合物中络离子化学式为
②该配合物在热NaOH溶液中发生反应,并释放出气体,该反应的化学方程式
(4)经X射线衍射测定发现,晶体钴在417℃以上堆积方式的剖面图如图所示,则该堆积方式属于

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,

请参照元素A~H在表中的位置,用化学用语回答下列问题:
(1)D、E、F的原子半径由大到小的顺序为___________ 。
(2)B、C、D的第一电离能由大到小的顺序为___________ 。
(3) A、D、E、H中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:___________ 。
(4)E、F的最高价氧化物的水化物相互反应的离子方程式:___________ 。
(5)在B所形成的化合物CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有___________ ;与CO分子互为等电子体的分子和离子分别为___________ 和___________ ,根据等电子理论推测CO分子的结构式可表示成___________ ,一个CO分子中有___________ 个σ键,___________ 个π键。
(6)根据价电子对互斥理论预测D和H所形成的HD 的空间构型为
的空间构型为___________ 形。

请参照元素A~H在表中的位置,用化学用语回答下列问题:
(1)D、E、F的原子半径由大到小的顺序为
(2)B、C、D的第一电离能由大到小的顺序为
(3) A、D、E、H中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
(4)E、F的最高价氧化物的水化物相互反应的离子方程式:
(5)在B所形成的化合物CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有
(6)根据价电子对互斥理论预测D和H所形成的HD
 的空间构型为
的空间构型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】H、C、N、O、S、Cu 均为前四周期常见元素。回答下列问题。
(1)S 位于元素周期表第_____ 族;N 的基态原子核外有_____ 个未成对电子。
(2)N、O、S 三种元素的第一电离能从大到小的顺序为_________ ;CuH 晶体中金属阳离子的基态核外电子排布式为_____ 。
(3)比较沸点:H2O_____ H2S(填“>”、“<”或“=”);干冰熔化时克服微粒间的 作用力类型是_________ 。
(4)SO42-的立体构型为_____ ;NO2- 中氮原子的杂化轨道类型为________ , 与其是等电子体的分子有_________ (填 1 个)。
(5)Cu2O 晶体如图所示的晶胞中每个氧原子与_____ 个铜原子配位。Cu2O 晶体 的密度为 dg·cm-3,则 Cu 与 O 的最近距离是_________ (用 M 表示 Cu2O 的摩尔质量,NA 表示阿伏加 德罗常数值)。

(1)S 位于元素周期表第
(2)N、O、S 三种元素的第一电离能从大到小的顺序为
(3)比较沸点:H2O
(4)SO42-的立体构型为
(5)Cu2O 晶体如图所示的晶胞中每个氧原子与

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】2020年12月17日嫦娥五号返回器带回月球土壤样品。研究发现,月球土壤样品中存在铁、金、银、铅、锌、铜等矿物颗粒。请回答下列问题:
(1)基态Fe原子核外填充有电子的原子轨道数目为___________ ,基态 与
与 中未成对电子数之比为
中未成对电子数之比为___________ 。邻二氮菲(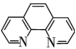 )中N原子可与
)中N原子可与 通过配位键形成橙红色邻二氮菲亚铁离子,利用该反应可测定
通过配位键形成橙红色邻二氮菲亚铁离子,利用该反应可测定 浓度,该反应的适宜pH范围为2~9,试解释若pH<2会产生什么影响
浓度,该反应的适宜pH范围为2~9,试解释若pH<2会产生什么影响___________ 。
(2)Zn在元素周期表中的位置为___________ ,其基态原子的M电子层中电子占据的最高能级是___________ 。
(3)我国科学家研究发现,十八胺在较高温度下具有一定的还原性,由于从十八胺中获得电子的能力不同,不同的金属盐在十八胺体系中反应可以得到不同的产物:
已知元素的电负性数据:
据此推测单一的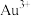 盐在十八胺体系中反应的产物为
盐在十八胺体系中反应的产物为___________ (写化学式)。
(1)基态Fe原子核外填充有电子的原子轨道数目为
 与
与 中未成对电子数之比为
中未成对电子数之比为 )中N原子可与
)中N原子可与 通过配位键形成橙红色邻二氮菲亚铁离子,利用该反应可测定
通过配位键形成橙红色邻二氮菲亚铁离子,利用该反应可测定 浓度,该反应的适宜pH范围为2~9,试解释若pH<2会产生什么影响
浓度,该反应的适宜pH范围为2~9,试解释若pH<2会产生什么影响(2)Zn在元素周期表中的位置为
(3)我国科学家研究发现,十八胺在较高温度下具有一定的还原性,由于从十八胺中获得电子的能力不同,不同的金属盐在十八胺体系中反应可以得到不同的产物:
| 单一金属盐 |  |  |
| 在十八胺体系中的产物 | ZnO | Ag |
| 元素 | Zn | Ag | Au |
| 电负性(鲍林标度) | 1.6 | 1.9 | 2.4 |
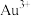 盐在十八胺体系中反应的产物为
盐在十八胺体系中反应的产物为
您最近一年使用:0次
【推荐2】全球首次在350公里时速的奥运版复兴号高铁列车上依托5G技术打造的超高清直播演播室,实现了超高清信号的长时间稳定传输。请回答下列问题:
(1)5G芯片主要材质是高纯硅。基态Si原子价层电子的运动状态有___________ 种。高纯硅制备过程中会生成 、
、 等中间产物。这两种物质的沸点:
等中间产物。这两种物质的沸点:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(2)已知电负性: ,则
,则 充分水解的化学方程式为
充分水解的化学方程式为___________ 。
(3)复兴号高铁车体材质用到Mn、Co等元素。Mn的一种配合物化学式为[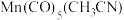 ],下列说法正确的是___________(填字母标号)。
],下列说法正确的是___________(填字母标号)。
(4)时速600公里的磁浮列车需用到超导材料。超导材料 具有
具有 型结构(如图),晶胞参数(晶胞边长)为
型结构(如图),晶胞参数(晶胞边长)为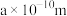 ,则最近的两个
,则最近的两个 间的距离为
间的距离为___________ m;阿伏伽德罗常数的值为 ,则该氮化钛的密度
,则该氮化钛的密度___________  (列出计算式即可)。
(列出计算式即可)。

(1)5G芯片主要材质是高纯硅。基态Si原子价层电子的运动状态有
 、
、 等中间产物。这两种物质的沸点:
等中间产物。这两种物质的沸点:
 (填“>”或“<”)。
(填“>”或“<”)。(2)已知电负性:
 ,则
,则 充分水解的化学方程式为
充分水解的化学方程式为(3)复兴号高铁车体材质用到Mn、Co等元素。Mn的一种配合物化学式为[
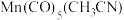 ],下列说法正确的是___________(填字母标号)。
],下列说法正确的是___________(填字母标号)。A. 与Mn原子配位时,提供孤电子对的是C原子 与Mn原子配位时,提供孤电子对的是C原子 |
| B.Mn原子的配位数为6 |
C. 中C原子的杂化类型为 中C原子的杂化类型为 、 、 |
D. 中 中 键与 键与 键数目之比为 键数目之比为 |
 具有
具有 型结构(如图),晶胞参数(晶胞边长)为
型结构(如图),晶胞参数(晶胞边长)为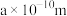 ,则最近的两个
,则最近的两个 间的距离为
间的距离为 ,则该氮化钛的密度
,则该氮化钛的密度 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】镍的合金及镍的配合物[如Ni(CO)4、[Ni(CN)4]2- 、 Ni(en)3]SO4等]在生产和科学研究中有重要应用。回答下列问题:
(1)基态Ni原子的价电子排布式为___________
(2)Ni与Ca同周期且最外层电子构型相同,镍的熔、沸点依次为1453℃、2 732℃,钙的熔、沸点依次为842℃、1484℃,镍的熔沸点均比钙高得多,这是因为___________ 。
(3)CuNi(CN)4是一种二维负热膨胀材料,可通过下列反应(未配平)制备:

CuNi( CN)4中Cu、Ni的配位原子依次为___________ 、___________ ,其σ键与π键数目之比为___________ 。
(4)Ni(CO)4的中心原子为sp3杂化,Ni(CO)4的空间构型为___________ ;[Ni(CN)4]2-的中心原子含s、p、d轨道的杂化轨道,其中Ni采敢的杂化类型为___________ (填标号)。
①dsp2②sp3d ③sp3d2
(5)乙二胺(en,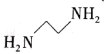 )的沸点为117.3℃,正丁烷的沸点为-0.5℃,前者沸点比后者高得多的主要原因是
)的沸点为117.3℃,正丁烷的沸点为-0.5℃,前者沸点比后者高得多的主要原因是___________ 。
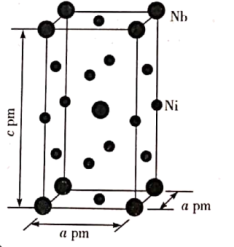
(6)某Ni、Nb合金的晶胞结构如图所示,设Ni和Nb的原子半径分别为rNipm和rNbpm,则金属原子的空间利用率为___________ % (列出计算表达式)。
(1)基态Ni原子的价电子排布式为
(2)Ni与Ca同周期且最外层电子构型相同,镍的熔、沸点依次为1453℃、2 732℃,钙的熔、沸点依次为842℃、1484℃,镍的熔沸点均比钙高得多,这是因为
(3)CuNi(CN)4是一种二维负热膨胀材料,可通过下列反应(未配平)制备:

CuNi( CN)4中Cu、Ni的配位原子依次为
(4)Ni(CO)4的中心原子为sp3杂化,Ni(CO)4的空间构型为
①dsp2②sp3d ③sp3d2
(5)乙二胺(en,
 )的沸点为117.3℃,正丁烷的沸点为-0.5℃,前者沸点比后者高得多的主要原因是
)的沸点为117.3℃,正丁烷的沸点为-0.5℃,前者沸点比后者高得多的主要原因是(6)某Ni、Nb合金的晶胞结构如图所示,设Ni和Nb的原子半径分别为rNipm和rNbpm,则金属原子的空间利用率为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】原子序数小于36的X、Y、Z、W、J、G六种元素,原子序数依次增大,其中X元素的原子在所有原子中半径最小,Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,W元素原子最外层电子数是内层电子数的3倍,J元素原子核外的3p能级有两个电子,G元素原子核外有6个未成对电子。回答下列问题。
(1)写出G元素的基态原子的价电子排布式_____ ; 分子中σ键与π键数目之比为
分子中σ键与π键数目之比为_____ 。
(2)Y、Z、W三种元素第一电离能由小到大的顺序为_____ (用元素符号表示)。
(3) 在水中的溶解度较大,可能的原因有
在水中的溶解度较大,可能的原因有_____ 。
A.氨分子和水分子间可以形成氢键 B.NH3能与水反应 C.NH3与水都是极性分子
(4)判断J与W形成的化合物JW2是晶体还是非晶体,最科学的办法是_____ ;XYZ分子中Y原子轨道的杂化类型为_____ 。
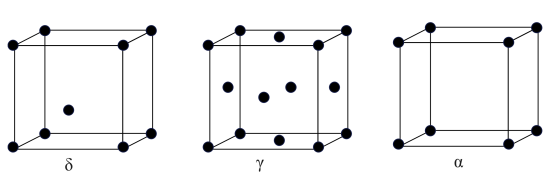
(5)G元素有δ、γ、α三种同素异形体,晶胞结构如图所示。三种晶体的晶胞中所含有的G原子数之比为_____ 。在γ晶胞结构中,设阿伏加德罗常数为NA,G原子半径为apm,G的相对原子质量为M,则该晶体的密度为_____ g/cm3.(用含NA、M和a的代数式表示)
(1)写出G元素的基态原子的价电子排布式
 分子中σ键与π键数目之比为
分子中σ键与π键数目之比为(2)Y、Z、W三种元素第一电离能由小到大的顺序为
(3)
 在水中的溶解度较大,可能的原因有
在水中的溶解度较大,可能的原因有A.氨分子和水分子间可以形成氢键 B.NH3能与水反应 C.NH3与水都是极性分子
(4)判断J与W形成的化合物JW2是晶体还是非晶体,最科学的办法是
(5)G元素有δ、γ、α三种同素异形体,晶胞结构如图所示。三种晶体的晶胞中所含有的G原子数之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铝、磷、硫及其化合物在生产生活及科研中应用广泛。

(1) 可用于制造火柴,其分子结构如图1所示。
可用于制造火柴,其分子结构如图1所示。
① 分子中硫原子的杂化类型为
分子中硫原子的杂化类型为___________ , 分子中P原子的化合价为
分子中P原子的化合价为___________ 。
② 分子可以形成配合物
分子可以形成配合物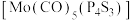 ,该配合物中Mo的配位数为
,该配合物中Mo的配位数为___________ ;1个该配合物分子中 键数目为
键数目为___________ 。
(2)磷化铝熔点为2000℃,它与晶体硅互为等电子体,磷化铝晶胞结构如图2所示。
①磷化铝晶体中磷与铝微粒间的作用力为___________ ,晶胞中由4个铝原子围成的空间构型是___________ 。
②已知相邻的P原子和Al原子的核间距是d nm,B原子的分数坐标为___________ ,磷化铝晶胞的密度为___________  。
。

(1)
 可用于制造火柴,其分子结构如图1所示。
可用于制造火柴,其分子结构如图1所示。①
 分子中硫原子的杂化类型为
分子中硫原子的杂化类型为 分子中P原子的化合价为
分子中P原子的化合价为②
 分子可以形成配合物
分子可以形成配合物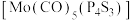 ,该配合物中Mo的配位数为
,该配合物中Mo的配位数为 键数目为
键数目为(2)磷化铝熔点为2000℃,它与晶体硅互为等电子体,磷化铝晶胞结构如图2所示。
①磷化铝晶体中磷与铝微粒间的作用力为
②已知相邻的P原子和Al原子的核间距是d nm,B原子的分数坐标为
 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】贵州的矿产资源丰富,在全国占优势地位的有铝、磷、煤、锰、重晶石、黄金、铅锌、锑等众多品种。回答下列问题:
(1)金元素属于铜族元素,原子结构与铜相似,在元素周期表中位于第六周期,基态金原子的外围电子排布图为__________ ;Cu2+能与多种离子或分子形成稳定性不同的配合物。经X射线衍射测得配合物酞菁铜的晶体结构,其局部结构如图所示:

①酞菁铜结构中非金属元素电负性由大到小的顺序为__________ ;
②酞菁铜结构中N原子的轨道杂化类型为__________ 。酞菁铜结构中不存在的化学键类型为__________
A.配位键 B.金属键 C.σ键 D.π键
(2)煤通过干馏、气化、液化可获得清洁燃料和多种化工原料,氨是其中之一。NH3的 VSEPR模型为__________ 。
(3)锰、铁两元素中第三电离能较大的是__________ (填元素符号),原因是___________ 。
(4)碲化锌(ZnTe)具有宽禁带的特性,常用于制作半导体材料,碲化锌晶体有立方和六方两种晶型,其立方晶胞结构如下图所示。
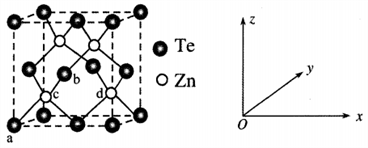

①原子坐标参数表示晶胞内部各原子的相对位置。已知a、b、c的原子坐标参数分别为(0,0,0)、( ,0,
,0, )、(
)、( ,
, ,
, )。则d的原子坐标参数为
)。则d的原子坐标参数为__________ 。
②若两个距离最近的Te原子间距离为apm,则晶体密度为__________ g/cm3(列式即可)。
(1)金元素属于铜族元素,原子结构与铜相似,在元素周期表中位于第六周期,基态金原子的外围电子排布图为

①酞菁铜结构中非金属元素电负性由大到小的顺序为

②酞菁铜结构中N原子的轨道杂化类型为
A.配位键 B.金属键 C.σ键 D.π键
(2)煤通过干馏、气化、液化可获得清洁燃料和多种化工原料,氨是其中之一。NH3的 VSEPR模型为
(3)锰、铁两元素中第三电离能较大的是
(4)碲化锌(ZnTe)具有宽禁带的特性,常用于制作半导体材料,碲化锌晶体有立方和六方两种晶型,其立方晶胞结构如下图所示。


①原子坐标参数表示晶胞内部各原子的相对位置。已知a、b、c的原子坐标参数分别为(0,0,0)、(
 ,0,
,0, )、(
)、( ,
, ,
, )。则d的原子坐标参数为
)。则d的原子坐标参数为②若两个距离最近的Te原子间距离为apm,则晶体密度为
您最近一年使用:0次



