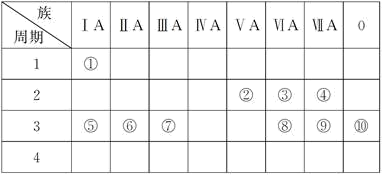
下表为长式元素周期表的主要部分。①~⑬代表13种元素,⑭表示元素周期表中某一区域。
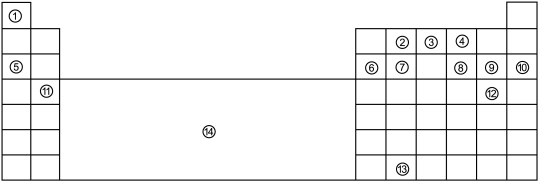
请回答:
(1)①、②、④的原子半径从大到小排列的顺序是______ 。(填化学式)
(2)①与③组成的含10个电子的阳离子的化学式是______ 。
(3)有些族的元素有特别的名称,⑨所在主族的元素叫做______ 元素。
(4)⑩的元素符号是______ 。
(5)⑪的元素名称是______ 。
(6)⑫的原子结构示意图是______ 。
(7)⑬在元素周期表中的位置是______ 。
(8)下列说法不正确 的是______ 。
A. ②的原子所含原子数即
②的原子所含原子数即 任何粒子的粒子数
任何粒子的粒子数
B.⑥、⑦的氧化物均能与⑤的最高价氧化物对应水化物反应
C.⑧的某种氧化物进入大气会形成酸雨
D.⑨的某种氧化物可用于自来水消毒
E.⑭所示区域内的元素常见于农药中
(9)⑥的单质与 溶液反应的化学方程式是
溶液反应的化学方程式是______ 。

请回答:
(1)①、②、④的原子半径从大到小排列的顺序是
(2)①与③组成的含10个电子的阳离子的化学式是
(3)有些族的元素有特别的名称,⑨所在主族的元素叫做
(4)⑩的元素符号是
(5)⑪的元素名称是
(6)⑫的原子结构示意图是
(7)⑬在元素周期表中的位置是
(8)下列说法
A.
 ②的原子所含原子数即
②的原子所含原子数即 任何粒子的粒子数
任何粒子的粒子数B.⑥、⑦的氧化物均能与⑤的最高价氧化物对应水化物反应
C.⑧的某种氧化物进入大气会形成酸雨
D.⑨的某种氧化物可用于自来水消毒
E.⑭所示区域内的元素常见于农药中
(9)⑥的单质与
 溶液反应的化学方程式是
溶液反应的化学方程式是
更新时间:2024-04-04 11:41:37
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】2021年5月,中国可持续发展研究会碳中和委员会成立。可持续发展需要注意“环境保护”和“节约能源”。
(1)以煤炭为主的能源结构易导致酸雨的形成,形成这类酸雨的主要气体是___________ ;
(2)氮氧化物(NOx)是大气中的主要气态污染物之一、汽车尾气中含有NO2、CO和碳氢化合物等。汽车尾气净化装置里装有Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用的机理如图所示。
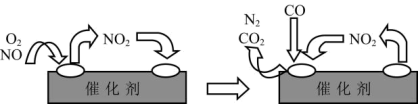
尾气净纯装置中发生的总反应化学方程式为___________ ;
(3)工业废水需处理达标后才能排放,下列处理方法合理的是___________ (填字母);
A.用中和法除去废水中的酸
B.用絮凝剂除去废水中的重金属离子
C.用氯气除去废水中的悬浮物
(4)焦炭的主要组成元素为碳元素,写出工业上用焦炭在高温下还原二氧化硅制备粗硅的化学方程式:___________ 。若转移1 mol电子则生成的气体在标准状况下的体积为___________ L。工业上可通过如下流程由粗硅制取纯硅: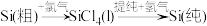 ,若上述反应中Si(粗)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产100.8 t纯硅,需纯度为75%的石英砂(主要成分为SiO2)
,若上述反应中Si(粗)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产100.8 t纯硅,需纯度为75%的石英砂(主要成分为SiO2)___________ 吨。
(1)以煤炭为主的能源结构易导致酸雨的形成,形成这类酸雨的主要气体是
(2)氮氧化物(NOx)是大气中的主要气态污染物之一、汽车尾气中含有NO2、CO和碳氢化合物等。汽车尾气净化装置里装有Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用的机理如图所示。

尾气净纯装置中发生的总反应化学方程式为
(3)工业废水需处理达标后才能排放,下列处理方法合理的是
A.用中和法除去废水中的酸
B.用絮凝剂除去废水中的重金属离子
C.用氯气除去废水中的悬浮物
(4)焦炭的主要组成元素为碳元素,写出工业上用焦炭在高温下还原二氧化硅制备粗硅的化学方程式:
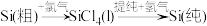 ,若上述反应中Si(粗)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产100.8 t纯硅,需纯度为75%的石英砂(主要成分为SiO2)
,若上述反应中Si(粗)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产100.8 t纯硅,需纯度为75%的石英砂(主要成分为SiO2)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】为消除燃煤烟气中含有的SO2、NOx,研究者提出了若干烟气“脱硫”、“脱硝”的方法。
(1)向燃煤中加入适量石灰石,高温时将SO2转化为CaSO4的化学方程式是__________ 。
(2)选择性催化还原法(SCR)“脱硝”。在催化剂的作用下,选取还原剂将烟气中的NOx进行无害化处理。NH3还原NO2的化学方程式是_______________________________ 。
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”。控制溶液的pH=5.5,将烟气中的SO2、NO转化为SO42−、NO3−,均为放热反应。
①在图1中画出“放热反应”的反应过程中的能量变化示意图。_________

②NaClO溶液吸收烟气中NO的离子方程式是________________________________ 。
③一定时间内,温度对硫、硝脱除率的影响曲线如图2,SO2的脱除率高于NO,可能的原因是____ (写出1种即可)。

④烟气中SO2和NO的体积比为3∶1,50℃时的脱除率见图2,则此吸收液中烟气转化生成的Cl−和NO3−的物质的量之比为______________________ (写最简整数比)。
(1)向燃煤中加入适量石灰石,高温时将SO2转化为CaSO4的化学方程式是
(2)选择性催化还原法(SCR)“脱硝”。在催化剂的作用下,选取还原剂将烟气中的NOx进行无害化处理。NH3还原NO2的化学方程式是
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”。控制溶液的pH=5.5,将烟气中的SO2、NO转化为SO42−、NO3−,均为放热反应。
①在图1中画出“放热反应”的反应过程中的能量变化示意图。

②NaClO溶液吸收烟气中NO的离子方程式是
③一定时间内,温度对硫、硝脱除率的影响曲线如图2,SO2的脱除率高于NO,可能的原因是

④烟气中SO2和NO的体积比为3∶1,50℃时的脱除率见图2,则此吸收液中烟气转化生成的Cl−和NO3−的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硫、氮元素是高中化学学习的两种重要非金属元素,其价-类二维图分别如图。
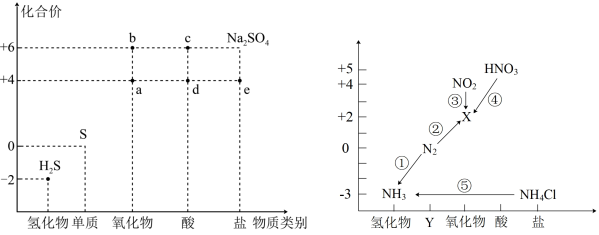
(1)图中物质“d”的化学式是___________ ;若不加任何其它试剂完成转化过程⑤,则⑤的反应为___________ 反应(填“吸热”或“放热”)。
(2)将一定量的a气体通入下列溶液中,能观察到白色沉淀现象的是___________(填标号)。
(3)写出反应③的离子方程式___________ 。
(4)a的水溶液与H2S发生反应可观察到的实验现象是___________ 。
(5)若e为钾元素的正盐,能被硫酸酸化的K2Cr2O7氧化为K2SO4,Cr2O 被还原为Cr3+,请配平化学方程式:
被还原为Cr3+,请配平化学方程式:_________
___________K2SO3+___________K2Cr2O7+___________H2SO4=___________Cr2(SO4)3+___________K2SO4+___________H2O
(6)如图为合成氨以及氨氧化制硝酸的流程示意图:
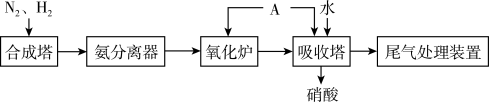
已知:用NaOH溶液进行尾气处理时的化学反应为: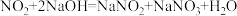 ,
,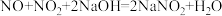 。
。
为了防止环境污染,用NaOH溶液进行尾气处理,若尾气能完全被吸收,则尾气中NO2与NO的体积必须满足的条件是:
___________ 。

(1)图中物质“d”的化学式是
(2)将一定量的a气体通入下列溶液中,能观察到白色沉淀现象的是___________(填标号)。
| A.Ba(NO3)2溶液 | B.CaCl2溶液 | C.H2O2溶液 | D.Na2CO3溶液 |
(4)a的水溶液与H2S发生反应可观察到的实验现象是
(5)若e为钾元素的正盐,能被硫酸酸化的K2Cr2O7氧化为K2SO4,Cr2O
 被还原为Cr3+,请配平化学方程式:
被还原为Cr3+,请配平化学方程式:___________K2SO3+___________K2Cr2O7+___________H2SO4=___________Cr2(SO4)3+___________K2SO4+___________H2O
(6)如图为合成氨以及氨氧化制硝酸的流程示意图:

已知:用NaOH溶液进行尾气处理时的化学反应为:
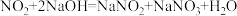 ,
,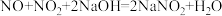 。
。为了防止环境污染,用NaOH溶液进行尾气处理,若尾气能完全被吸收,则尾气中NO2与NO的体积必须满足的条件是:

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(填写序号不得分):
(1)⑦元素的离子半径__ S2-(填“>”或“<”),比较③与⑥的氢化物,___ 更稳定(填化学式),最不活泼的元素是___ (填元素符号)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是____ ,碱性最强的化合物的化学式是:_____ 。
(3)比较①与⑤的最高价氧化物对应的水化物,_____ 的酸性强(填化学式),能证明两者酸性强弱的离子反应方程式为______
(4)实验室制取②的氢化物的化学方程式________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(1)⑦元素的离子半径
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)比较①与⑤的最高价氧化物对应的水化物,
(4)实验室制取②的氢化物的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表为元素周期表的一 部分,请回答有关问题
(1)已知元素⑩ 的一种核素,中子数为45,用原子符号表示该核素为_________ ;
(2)元素⑦、⑧、⑨其离子半径由大到小的顺序是_________ (离子符号表示),元素⑨ 的最高价氧化物的水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为__________ 。
(3)下列事实不能说明元素⑧的非金属性比元素⑦的非金属性强的是_ ;
(4)由上表中的元素构成的A+、B+、 C-、D、E五种含有10个电子的粒子,已知他们有如下转化关系:反应一: A++C-  D+E↑:反应二 : B++C-=2D;写出B+的化学式
D+E↑:反应二 : B++C-=2D;写出B+的化学式__________ ,反应一的离子方程式为___________ 。
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ |
(2)元素⑦、⑧、⑨其离子半径由大到小的顺序是
(3)下列事实不能说明元素⑧的非金属性比元素⑦的非金属性强的是_ ;
| A.元素⑧的单质与⑦的氢化物的水溶液反应,溶液变浑浊 |
| B.元素⑧的单质能将Fe氧化成三价铁,而元素⑦的单质只能将铁氧化成二价铁 |
| C.⑦和⑧两元素的简单氢化物受热分解,后者的分解温度高 |
| D.元素⑧的氢化物的水溶液的酸性比元素⑦的氢化物水溶液的酸性强 |
 D+E↑:反应二 : B++C-=2D;写出B+的化学式
D+E↑:反应二 : B++C-=2D;写出B+的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,请回答有关问题:
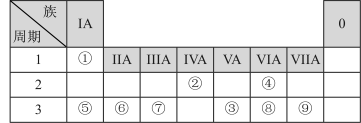
请按要求回答下列问题:
(1)元素⑦的原子结构示意图______________________ 。由②、④两种元素组成的化合物是___________ 化合物(填“共价”或“离子”)
(2)元素①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式__________________ ;一种离子化合物的化学式_________
(3)④⑤⑥三种元素的离子半径由大到小的顺序是____________ (填离子符号)。
(4)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较弱的是________ (填化学式)。
(5)元素③的气态氢化物和元素⑧的气态氢化物更稳定的是___________ (填化学式)。
(6)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应水化物反应,其离子方程式为_________________________________________

请按要求回答下列问题:
(1)元素⑦的原子结构示意图
(2)元素①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式
(3)④⑤⑥三种元素的离子半径由大到小的顺序是
(4)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较弱的是
(5)元素③的气态氢化物和元素⑧的气态氢化物更稳定的是
(6)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应水化物反应,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求填写
| 序号 | 要求 | 结果 |
| ① | 写出元素Ge价电子轨道式 | |
| ② | NH3NH H2OCO2键角由大到小排序 H2OCO2键角由大到小排序 | |
| ③ | C,N,O,F第一电离能从大到小排序 | |
| ④ | HFHClHBr稳定性由高到低排序 | |
| ⑤ | HFHClHBr沸点由高到低排序 | |
| ⑥ | MgOCaO晶格能大小比较,并解释原因 | |
| ⑦ | SO3中心原子杂化方式 | |
| ⑧ | 与NO 等电子体的阴离子(写一种) 等电子体的阴离子(写一种) | |
| ⑨ | 甲醇沸点高于甲醛的原因解释 | |
| ⑩ | O2-Na+Mg2+Al3+Cl-半径从大到小排序 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】C、N、O、Al、Si、Cu是常见的六种元素。
(1)Si位于元素周期表第_______ 周期第_______ 族,其基态原子的轨道表示式为_______ 。
(2)Cu的基态原子的电子排布式为_______ 。
(3)原子半径:Al_______ Si,电负性:N_______ O,第一电离能:C_______ N。(用“>”或“<”填空)
(4)Ge元素的最外层基态电子排布为4s24p2,Ge元素可能的性质或应用有_______。
(1)Si位于元素周期表第
(2)Cu的基态原子的电子排布式为
(3)原子半径:Al
(4)Ge元素的最外层基态电子排布为4s24p2,Ge元素可能的性质或应用有_______。
| A.是一种活泼的金属元素 | B.其电负性大于硅 |
| C.其单质可作为半导体材料 | D.其第一电离能小于硅 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I)下表为元素周期表的一部分,回答以下问题:
(1) 与
与 的原子半径大小关系是:
的原子半径大小关系是:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(2)F与 的非金属性强弱顺序是:F
的非金属性强弱顺序是:F___________  (填“>”或“<”),其简单氢化物的稳定性较强的是
(填“>”或“<”),其简单氢化物的稳定性较强的是___________ (填化学式)。
(3)P、S两种元素的最高价氧化物对应水化物的酸性较弱的是___________ (填化学式)。
(4)C位于元素周期表中的位置__________ 。
II)完成下列问题
(5)写出表示含有8个质子、10 个中子的原子的化学符号:_______ 。
(6)根据下列微粒回答问题: 、
、 、
、 、14C、 l4N、 16O、 35Cl2、 37Cl2。
、14C、 l4N、 16O、 35Cl2、 37Cl2。
①以上8种微粒共包含了_______ 种核素,共_______ 种元素。
②互为同位素的是_______ 。
③质量数相等的是_______ 和_______ ,中子数相等的是_______ 和_______ 。
(7)相同物质的量的14CO2与S18O2的质量之比为_______ ,电子数之比为c_______ 。
(8)物质的量相同的H2O和D2O与足量钠反应,放出的气体在标准状况下的体积之比为_______ 。
| C | N | F | ||||
 |  |  |  |  |  |
 与
与 的原子半径大小关系是:
的原子半径大小关系是:
 (填“>”或“<”)。
(填“>”或“<”)。(2)F与
 的非金属性强弱顺序是:F
的非金属性强弱顺序是:F (填“>”或“<”),其简单氢化物的稳定性较强的是
(填“>”或“<”),其简单氢化物的稳定性较强的是(3)P、S两种元素的最高价氧化物对应水化物的酸性较弱的是
(4)C位于元素周期表中的位置
II)完成下列问题
(5)写出表示含有8个质子、10 个中子的原子的化学符号:
(6)根据下列微粒回答问题:
 、
、 、
、 、14C、 l4N、 16O、 35Cl2、 37Cl2。
、14C、 l4N、 16O、 35Cl2、 37Cl2。①以上8种微粒共包含了
②互为同位素的是
③质量数相等的是
(7)相同物质的量的14CO2与S18O2的质量之比为
(8)物质的量相同的H2O和D2O与足量钠反应,放出的气体在标准状况下的体积之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】短周期元素N、Na、Al形成的物质在工农业生产、生活中应用广泛。
(1)Al在元素周期表中的位置为_______ ;其原子半径比Na_____ (填“大”或“小”)。
(2)Al单质在空气中不易腐蚀,原因是其表面形成了一种致密的且熔点高的化合物。该化合物的晶体类型为_________ ;该化合物遇酸碱易被腐蚀,请写出它与NaOH溶液反应的离子方程式______________ 。
(3)NH3的电子式为_______ ;NH3在同族元素形成的氢化物中具有较高的沸点,其原因是________ 。
(4)标准状况下22.4L NH3与0.5L 1mol/L 氮元素的最高价氧化物的水化物反应,所得溶液中离子浓度由大到小的顺序是____________________________________ 。
(5)NF3是一种新型电子材料,常温下为稳定气体,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和某种物质。请写出反应的化学方程式_______________________ 。
(1)Al在元素周期表中的位置为
(2)Al单质在空气中不易腐蚀,原因是其表面形成了一种致密的且熔点高的化合物。该化合物的晶体类型为
(3)NH3的电子式为
(4)标准状况下22.4L NH3与0.5L 1mol/L 氮元素的最高价氧化物的水化物反应,所得溶液中离子浓度由大到小的顺序是
(5)NF3是一种新型电子材料,常温下为稳定气体,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和某种物质。请写出反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
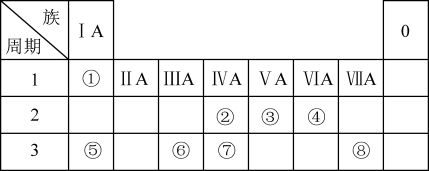
(1)地壳中含量居于第二位的元素在周期表中的位置是________________ 。
除稀有气体外,原子半径最大的元素是______ ,它的原子结构示意图是________ 。
(2)②的最高价氧化物的分子式为________ ;
⑦的最高价氧化物对应水化物的分子式为________ ;
最高价氧化物对应的水化物中酸性最强的是________ 。
(3)①④⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:________________________________ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是________ 。
A.最高正化合价为+6
B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱
D.单质在常温下可与氢气化合
(5)已知X为第ⅡA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,则Y的原子序数b与a所有可能的关系式为________________ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
除稀有气体外,原子半径最大的元素是
(2)②的最高价氧化物的分子式为
⑦的最高价氧化物对应水化物的分子式为
最高价氧化物对应的水化物中酸性最强的是
(3)①④⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是
A.最高正化合价为+6
B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱
D.单质在常温下可与氢气化合
(5)已知X为第ⅡA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,用化学用语回答下列问题:
(1)请画出元素⑨阴离子的结构示意图:___________ 。
(2)③⑤⑧的原子半径由小到大的顺序为___________ (填元素符号)。
(3)⑤和⑦的最高价氧化物对应水化物的碱性强弱为___________ >___________ (填化学式)。
(4)③⑤两种元素的原子按1∶1组成的常见化合物的电子式为___________ 。
(5)用电子式表示⑥和⑨形成的化合物的过程:______________________ 。

(1)请画出元素⑨阴离子的结构示意图:
(2)③⑤⑧的原子半径由小到大的顺序为
(3)⑤和⑦的最高价氧化物对应水化物的碱性强弱为
(4)③⑤两种元素的原子按1∶1组成的常见化合物的电子式为
(5)用电子式表示⑥和⑨形成的化合物的过程:
您最近一年使用:0次



