在中国古代,硫酸被炼丹术士称为“绿矾油”。这是因为生产硫酸最古老的方法是以绿矾为原料,在蒸馏釜中煅烧后,釜中逸出刺激性气味的气体,同时有油状液体流出,残留固体呈红棕色。

(1)请写出煅烧绿矾过程中发生反应的化学方程式:
①___________ ;
②___________ 。
(2)化学探究小组的同学用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去),其中b为干燥的试管。下列关于该反应说法正确的是___________。

(1)请写出煅烧绿矾过程中发生反应的化学方程式:
①
②
(2)化学探究小组的同学用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去),其中b为干燥的试管。下列关于该反应说法正确的是___________。
A.若将反应后的气体通入 溶液中,产生的沉淀为 溶液中,产生的沉淀为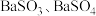 |
B.b中产物用紫色石蕊试液即可检验出其中 和 和 |
C.为检验反应的气态生成物是 ,试管c中应加入的试剂为NaOH溶液 ,试管c中应加入的试剂为NaOH溶液 |
| D.b中所得到的硫酸的质量分数为29.5% |
2024高一·全国·学业考试 查看更多[1]
更新时间:2024-04-04 05:44:16
|
相似题推荐
解答题-实验探究题
|
容易
(0.94)
名校
【推荐1】㵘同学根据Mg与 反应的原理推测Na也能在
反应的原理推测Na也能在 中燃烧,为了确定其产物,在春老师的指导下他设计了如图所示装置进行实验。已知
中燃烧,为了确定其产物,在春老师的指导下他设计了如图所示装置进行实验。已知 能被CO还原得到黑色的金属Pd。请回答下列问题:
能被CO还原得到黑色的金属Pd。请回答下列问题:
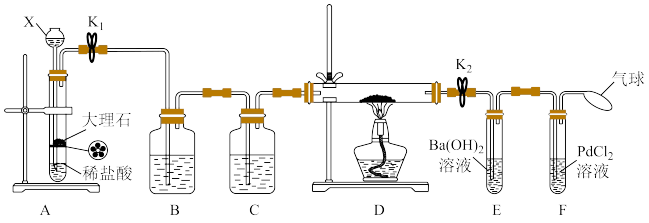
(1)仪器X的名称是___________ 。
(2)装置B中的试剂是___________ ,作用是___________ 。
(3)先称量硬质玻璃管的质量为 ,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是
,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是 。再按如下顺序进行实验操作。
。再按如下顺序进行实验操作。
①打开 和
和 ,通入
,通入 待E中出现
待E中出现___________ 时,再点燃酒,此操作的目的是___________ ;②熄灭酒精灯;③冷却到室温;④关闭 和
和 ;⑤称量硬质玻璃管。重复上述操作步骤,直至硬质玻璃管恒重,称得质量为
;⑤称量硬质玻璃管。重复上述操作步骤,直至硬质玻璃管恒重,称得质量为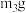 。
。
(4)加热D装置中硬质玻璃管一段时间,观察到以下现象:
①钠块表面变黑,熔融成金属小球;
②继续加热,钠燃烧产生黄色火焰,硬质玻璃管中有大量黑色和白色固体产生。
③F中试管内壁有黑色沉淀产生。
产生上述现象②中黑色固体的原因是___________ 。
(5)探究硬质玻璃管中固体产物中钠元素的存在形式:
假设一:白色固体是 ;假设二:白色固体是
;假设二:白色固体是 ;假设三:白色固体是
;假设三:白色固体是 和
和 的混合物。请完成下列实验设计,验证上述假设:
的混合物。请完成下列实验设计,验证上述假设:
步骤1:将硬质玻璃管中的固体产物溶于水后,过滤;
步骤2:往步骤1所得滤液中加入足量的___________ 溶液产生白色沉淀,过滤;
步骤3:往步骤2所得滤液中滴加几滴酚酞试液,滤液不变红色。
结论:假设一成立。
(6)根据上述实验现象及表格中的实验数据,写出Na与 反应的总化学方程式:
反应的总化学方程式:___________ 。
 反应的原理推测Na也能在
反应的原理推测Na也能在 中燃烧,为了确定其产物,在春老师的指导下他设计了如图所示装置进行实验。已知
中燃烧,为了确定其产物,在春老师的指导下他设计了如图所示装置进行实验。已知 能被CO还原得到黑色的金属Pd。请回答下列问题:
能被CO还原得到黑色的金属Pd。请回答下列问题:
(1)仪器X的名称是
(2)装置B中的试剂是
(3)先称量硬质玻璃管的质量为
 ,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是
,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是 。再按如下顺序进行实验操作。
。再按如下顺序进行实验操作。①打开
 和
和 ,通入
,通入 待E中出现
待E中出现 和
和 ;⑤称量硬质玻璃管。重复上述操作步骤,直至硬质玻璃管恒重,称得质量为
;⑤称量硬质玻璃管。重复上述操作步骤,直至硬质玻璃管恒重,称得质量为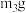 。
。(4)加热D装置中硬质玻璃管一段时间,观察到以下现象:
①钠块表面变黑,熔融成金属小球;
②继续加热,钠燃烧产生黄色火焰,硬质玻璃管中有大量黑色和白色固体产生。
③F中试管内壁有黑色沉淀产生。
产生上述现象②中黑色固体的原因是
(5)探究硬质玻璃管中固体产物中钠元素的存在形式:
假设一:白色固体是
 ;假设二:白色固体是
;假设二:白色固体是 ;假设三:白色固体是
;假设三:白色固体是 和
和 的混合物。请完成下列实验设计,验证上述假设:
的混合物。请完成下列实验设计,验证上述假设:步骤1:将硬质玻璃管中的固体产物溶于水后,过滤;
步骤2:往步骤1所得滤液中加入足量的
步骤3:往步骤2所得滤液中滴加几滴酚酞试液,滤液不变红色。
结论:假设一成立。
(6)根据上述实验现象及表格中的实验数据,写出Na与
 反应的总化学方程式:
反应的总化学方程式: |  |  |
| 66.70g | 69.00g | 72.15g |
您最近半年使用:0次
解答题-工业流程题
|
容易
(0.94)
解题方法
【推荐2】Fe/Fe3O4复合物是一种高密度磁记录材料,磁记录材料有记录和存储信息的功能。制备该材料的一种流程如下:
Ⅰ、相关反应原理:
①Fe2++2OH-=Fe(OH)2
②3Fe(OH)2=Fe+2Fe(OH)3
③Fe(OH)2+2Fe(OH)3=Fe3O4+4H2O
Ⅱ、25℃时Fe(OH)2的Ksp=8.0×10-16
1.用FeCl2溶液和KOH溶液制备Fe/Fe3O4反应的离子方程式为_____ 。该“反应”中通入氩气的原因_____ 。
2.取少量反应后溶液于试管中,选择试剂_____,可证明FeCl2溶液已反应完全。
3.已知参加反应的FeCl2溶液浓度为lmol·L−1。由题给信息分析,25℃时,当pH<2时,Fe/Fe3O4产率极低的原因_____ 。
下图1为回流时间与Fe/Fe3O4产率的关系图,图2为回流1h所得产品的X射线衍射图。_____ 。
通过Fe3O4和FeO的热化学循环可以利用太阳能,其转化关系如图所示。
6.从绿色化学角度评价该循环过程(说一点)。_____

Ⅰ、相关反应原理:
①Fe2++2OH-=Fe(OH)2
②3Fe(OH)2=Fe+2Fe(OH)3
③Fe(OH)2+2Fe(OH)3=Fe3O4+4H2O
Ⅱ、25℃时Fe(OH)2的Ksp=8.0×10-16
1.用FeCl2溶液和KOH溶液制备Fe/Fe3O4反应的离子方程式为
2.取少量反应后溶液于试管中,选择试剂_____,可证明FeCl2溶液已反应完全。
| A.SO2 | B.铁粉 |
| C.KSCN溶液 | D.KSCN溶液新制氯水 |
下图1为回流时间与Fe/Fe3O4产率的关系图,图2为回流1h所得产品的X射线衍射图。

通过Fe3O4和FeO的热化学循环可以利用太阳能,其转化关系如图所示。
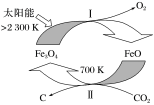
| A.反应物 | B.中间产物 | C.催化剂 | D.产物 |
您最近半年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐3】用如图所示实验装置可以完成中学化学实验中的一些实验。
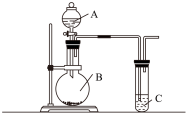
利用如图装置实验,证明二氧化硫气体具有漂白性。已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O。在装置A中加入70%的硫酸溶液,B中加入Na2SO3粉末。
(1)C中应加入溶液___ (填“品红”或“石蕊”)。打开分液漏斗活塞,一段时间后观察到C中现象是___ ,反应完全后,将C试管加热一段时间发生的现象是___ 。
(2)如果仅用如图装置进行此实验,可能造成环境污染,此污染属于___ (选填“白色污染”或“酸雨污染"),因此应该在C装置后加一个盛有___ 溶液的洗气瓶。
(3)将二氧化硫气体通入FeCl3溶液中反应一段时间后,滴加KSCN溶液,溶液未变红色,请写出所发生反应的离子方程式:___ 。

利用如图装置实验,证明二氧化硫气体具有漂白性。已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O。在装置A中加入70%的硫酸溶液,B中加入Na2SO3粉末。
(1)C中应加入溶液
(2)如果仅用如图装置进行此实验,可能造成环境污染,此污染属于
(3)将二氧化硫气体通入FeCl3溶液中反应一段时间后,滴加KSCN溶液,溶液未变红色,请写出所发生反应的离子方程式:
您最近半年使用:0次
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐1】 受热分解的化学方程式为2FeSO4
受热分解的化学方程式为2FeSO4 Fe2O3+SO3↑+SO2↑。
Fe2O3+SO3↑+SO2↑。
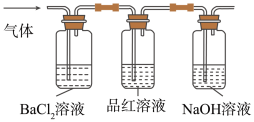
请回答:将 受热产生的气体按如图所示装置进行实验,证实含有
受热产生的气体按如图所示装置进行实验,证实含有 和
和 。能说明
。能说明 存在的实验现象是
存在的实验现象是____________ ;为测定 沉淀的质量,后续的操作步骤依次为
沉淀的质量,后续的操作步骤依次为__________ 、洗涤、干燥、称量。
 受热分解的化学方程式为2FeSO4
受热分解的化学方程式为2FeSO4 Fe2O3+SO3↑+SO2↑。
Fe2O3+SO3↑+SO2↑。请回答:将
 受热产生的气体按如图所示装置进行实验,证实含有
受热产生的气体按如图所示装置进行实验,证实含有 和
和 。能说明
。能说明 存在的实验现象是
存在的实验现象是 沉淀的质量,后续的操作步骤依次为
沉淀的质量,后续的操作步骤依次为
您最近半年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐1】某小组同学采用以下装置验证SO2的性质:

(夹持及加热装置略,试管1:紫色石蕊溶液,试管2: H2S 溶液,试管3:品红溶液,试管4:酸性KMnO4溶液,试管5: BaCl2溶液)。
(1)写出圆底烧瓶中发生反应的化学方程式_______ 。
(2)经过实验,观察到如下实验现象(填写字母):
①试管1中现象_______ 。
②试管2中现象_______ ,写出反应的化学方程式: _______ 。。
③试管3中现象_______ , 说明SO2具有漂白性,证明该漂白的可逆性的实验操作是_______ 。
A.溶液变为红色
B.溶液变为白色
C.溶液变为无色
D. 溶液先变为红色后变为无色
E.出现淡黄色沉淀
F.出现红褐色沉淀
(3)试管4中现象说明SO2还具有的性质是_______ ,反应离子方程式_______ 。

(夹持及加热装置略,试管1:紫色石蕊溶液,试管2: H2S 溶液,试管3:品红溶液,试管4:酸性KMnO4溶液,试管5: BaCl2溶液)。
(1)写出圆底烧瓶中发生反应的化学方程式
(2)经过实验,观察到如下实验现象(填写字母):
①试管1中现象
②试管2中现象
③试管3中现象
A.溶液变为红色
B.溶液变为白色
C.溶液变为无色
D. 溶液先变为红色后变为无色
E.出现淡黄色沉淀
F.出现红褐色沉淀
(3)试管4中现象说明SO2还具有的性质是
您最近半年使用:0次
解答题-无机推断题
|
容易
(0.94)
名校
解题方法
【推荐2】硫及其部分化合物的转化关系如图所示。

(1)硫单质俗称硫黄,通常状况下硫单质的颜色为___________ ;
(2)SO2可以使品红溶液褪色,说明SO2具有___________  填“漂白性”或“氧化性”
填“漂白性”或“氧化性” ;
;
(3)化合物A的化学式为___________ ;
(4)写出Cu与浓硫酸在加热条件下反应的化学反应方程式___________ 。

(1)硫单质俗称硫黄,通常状况下硫单质的颜色为
(2)SO2可以使品红溶液褪色,说明SO2具有
 填“漂白性”或“氧化性”
填“漂白性”或“氧化性” ;
;(3)化合物A的化学式为
(4)写出Cu与浓硫酸在加热条件下反应的化学反应方程式
您最近半年使用:0次
解答题-无机推断题
|
容易
(0.94)
解题方法
【推荐3】下图中每一字母表示一种反应物或生成物(反应时所需要的水或生成的水均已略去)。已知D是一种盐,焰色反应呈紫色,E在常温下是黄绿色气体,F是一种能使品红溶液褪色的无色气体。
请回答下列问题:
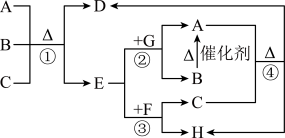
(1)写出D的化学式__________________ 。
(2)写出反应①的离子方程式____________________________________ ③的离子方程式___________________________________________
(3)在反应①中每生成1molE,转移电子数为_______________ mol。
请回答下列问题:

(1)写出D的化学式
(2)写出反应①的离子方程式
(3)在反应①中每生成1molE,转移电子数为
您最近半年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
解题方法
【推荐1】肼(N2H4)是氮和氢形成的一种化合物,易溶于水。工业上利用尿素法生产肼,同时得到副产品十水合碳酸钠,其工艺流程如图:
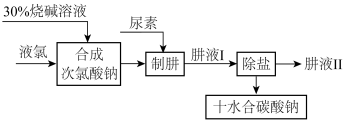
制肼过程的反应为:CO(NH2)2(尿素)+NaClO+2NaOH=N2H4+Na2CO3+NaCl+H2O
(1)实验室若配制30%烧碱溶液,所需的玻璃仪器除玻璃棒外,还有______ (填标号)。
A.漏斗 B.烧杯 C.烧瓶 D.量筒
(2)已知:Cl2+H2O=HCl+HClO,请推测C12与NaOH溶液发生反应的化学方程式:____ 。从后续反应过程来看,若要使原料不浪费,合成次氯酸钠时投入的液氯与烧碱的质量之比为71:_________ 。
(3)实验室中,欲从母液中分离出十水合碳酸钠晶体。可采用的操作依次为________ 。(填标号)
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
(4)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等。请写出肼除氧时发生反应的化学方程式:______________ 。

制肼过程的反应为:CO(NH2)2(尿素)+NaClO+2NaOH=N2H4+Na2CO3+NaCl+H2O
(1)实验室若配制30%烧碱溶液,所需的玻璃仪器除玻璃棒外,还有
A.漏斗 B.烧杯 C.烧瓶 D.量筒
(2)已知:Cl2+H2O=HCl+HClO,请推测C12与NaOH溶液发生反应的化学方程式:
(3)实验室中,欲从母液中分离出十水合碳酸钠晶体。可采用的操作依次为
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
(4)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等。请写出肼除氧时发生反应的化学方程式:
您最近半年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
【推荐2】“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为Na2CO3)吸收烟气中的 SO2,得到亚硫酸钠(Na2SO3)粗品。其流程如下:
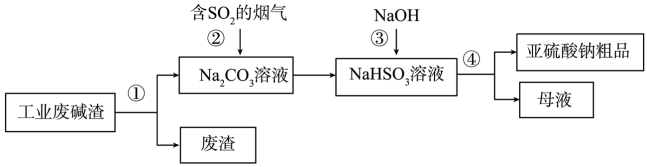
(1)为加快工业废碱渣中 Na2CO3的溶解,可采取的措施是_____ (写出一种即可)。
(2)上述流程中,加入NaOH 后,发生反应的化学方程式为_____ 。
(3)亚硫酸钠粗品中含有少量Na2SO4,原因是_____ 。
(4)设计实验证明亚硫酸钠粗品含有少量 Na2SO4的方案是:在一支试管中,加入少量 亚硫酸钠粗品,用适量蒸馏水溶解,_____ ,出现白色沉淀,则证明含有 Na2SO4。

(1)为加快工业废碱渣中 Na2CO3的溶解,可采取的措施是
(2)上述流程中,加入NaOH 后,发生反应的化学方程式为
(3)亚硫酸钠粗品中含有少量Na2SO4,原因是
(4)设计实验证明亚硫酸钠粗品含有少量 Na2SO4的方案是:在一支试管中,加入少量 亚硫酸钠粗品,用适量蒸馏水溶解,
您最近半年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐3】实验室常用Na2O2与H2O反应快速制取少量O2.用如图装置制取O2并演示Na在O2中的燃烧实验。
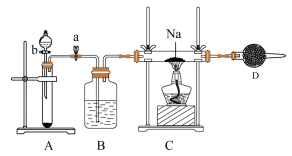
请回答下列问题:
(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管。试判断装置是否漏气_______ (填“漏气”“不漏气”或“无法确定”),判断理由是_______ 。
(2)B装置中的试剂是_______ ,其作用是_______ 。
(3)写出A装置中反应的化学方程式_______ 。
(4)C装置中观察到的现象是_______ 。
(5)D装置中盛放的试剂是_______ ,其作用是_______ 。

请回答下列问题:
(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管。试判断装置是否漏气
(2)B装置中的试剂是
(3)写出A装置中反应的化学方程式
(4)C装置中观察到的现象是
(5)D装置中盛放的试剂是
您最近半年使用:0次



