中国科学院化学研究所发表了 催化氢化机理。其机理中化合物
催化氢化机理。其机理中化合物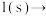 化合物
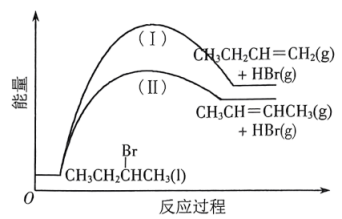
化合物 的过程和其相对能量变化如图所示。下列说法不正确的是
的过程和其相对能量变化如图所示。下列说法不正确的是

A.选择更优催化剂可以提升单位时间内 的转化率 的转化率 |
| B.该过程的总反应速率主要由过程①决定 |
C.化合物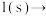 化合物 化合物 的过程包含两个基元反应 的过程包含两个基元反应 |
D.低温有利于化合物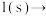 化合物 化合物 的反应自发进行 的反应自发进行 |
更新时间:2024-03-28 19:49:41
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法错误的是
| A.决定化学反应速率的主要因素是反应物本身的结构和性质 |
| B.活化分子之间发生的碰撞一定是有效碰撞 |
| C.所有活化分子的平均能量高于所有分子的平均能量 |
| D.升高温度能加快反应速率是因为反应物分子中活化分子的百分数增加 |
您最近半年使用:0次
【推荐2】信使分子NO对人体生命活动有重要意义,在一定温度时可以发生反应2NO+O2 2NO2,如图是在其他条件相同时,分别在有、无催化剂时反应过程的能量变化。下列说法正确的是
2NO2,如图是在其他条件相同时,分别在有、无催化剂时反应过程的能量变化。下列说法正确的是
 2NO2,如图是在其他条件相同时,分别在有、无催化剂时反应过程的能量变化。下列说法正确的是
2NO2,如图是在其他条件相同时,分别在有、无催化剂时反应过程的能量变化。下列说法正确的是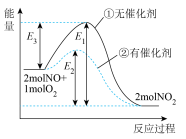
| A.该反应为吸热反应 |
| B.逆反应的活化能大于正反应的活化能 |
| C.加入催化剂可以改变反应的焓变 |
| D.该反应的焓变为E1—E2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】实现碳达峰、碳中和是党中央做出的重大战略决策。恒压、750°C时,CH4和CO2按物质的量之比1:3投料,反应经如下流程(主要产物已标出)可实现CO2高效转化。
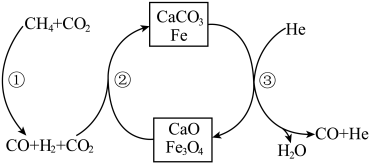
下列说法正确的是

下列说法正确的是
| A.过程①中,CO2的转化率为50% |
| B.过程②中CO2的吸收,不利于CO还原Fe3O4的平衡正向移动 |
| C.过程③中通入He的作用是催化剂,加快CaCO3分解 |
| D.过程①、②、③均涉及到了氧化还原反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关化学反应速率的说法正确的是
| A.100mL 2mol·L-1 的盐酸与锌反应时,加入适量的氯化钠溶液,反应速率不变 |
| B.SO2的催化氧化是一个放热反应,所以升高温度,反应速率减慢 |
| C.汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率减慢 |
| D.合成氨反应中,增加氨气浓度对反应速率无影响 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
A.由水电离产生的c(OH-)=10-11 mol·L-1的溶液中,Ba2+、CO 、Cl-、Na+定能大量共存 、Cl-、Na+定能大量共存 |
| B.等物质的量浓度的Na2SO4与NaHSO4溶液的pH相等 |
| C.对于反应N2H4(l)=N2(g)+2H2(g) △H=-50.6 kJ·mol-1,它只在高温下自发进行 |
| D.25℃时在醋酸钠溶液和盐酸混合后呈中性的溶液中:c(Na+)>c(Cl-)>c(H+) |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】关于反应进行方向的判断,以下说法错误的是
| A.高锰酸钾加热分解是一个熵增的过程 |
| B.能自发进行的化学反应不一定是ΔH<0、ΔS<0 |
| C.ΔH<0的化学反应均是自发反应,ΔS<0的化学反应均不能自发进行 |
| D.反应2Al2O3(s)+3C(s)=2Al(s)+3CO2(g)在常温下不能自发进行,说明该反应ΔH>0 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】哈伯法合成氨技术是德国诺贝尔化学奖获得者哈伯发明的。其合成原理为:N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H<0,
H<0, S<0。下列有关工业合成氨的说法正确的是
S<0。下列有关工业合成氨的说法正确的是
 2NH3(g)
2NH3(g)  H<0,
H<0, S<0。下列有关工业合成氨的说法正确的是
S<0。下列有关工业合成氨的说法正确的是A.因为 H<0,所以该反应一定能自发进行 H<0,所以该反应一定能自发进行 |
B.因为 S<0,所以该反应一定不能自发进行 S<0,所以该反应一定不能自发进行 |
| C.在低温下进行是为了提高反应物的转化率 |
| D.使用催化剂加快反应速率是因为催化剂降低了反应的活化能 |
您最近半年使用:0次

 或
或
 溶液中加入少量新制氯水,再加
溶液中加入少量新制氯水,再加 萃取
萃取 的还原性强于
的还原性强于

 溶液和4mL 1
溶液和4mL 1 ,分别记录溶液褪色所需的时间
,分别记录溶液褪色所需的时间 生成
生成

