常温下,用 溶液滴定
溶液滴定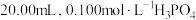 溶液的
溶液的 变化如图所示。下列说法正确的是
变化如图所示。下列说法正确的是
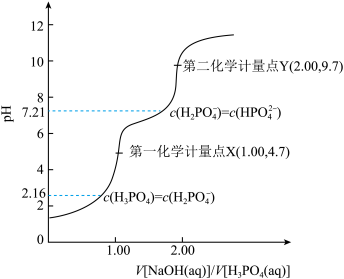
 溶液滴定
溶液滴定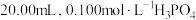 溶液的
溶液的 变化如图所示。下列说法正确的是
变化如图所示。下列说法正确的是
A.由X、Y点的 可得出 可得出 |
B.X点溶液中水电离出的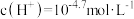 |
C.滴加 溶液至 溶液至 ,溶液中 ,溶液中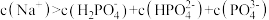 |
D.若向第三化学计量点溶液滴加同浓度 溶液,不会发生任何化学反应 溶液,不会发生任何化学反应 |
更新时间:2024-04-01 16:08:59
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】25℃时,用0.10mol·L-1的氨水滴定10.0mLamol·L-1的盐酸,溶液的pH与氨水体积(V)的关系如图所示,已知N点为恰好完全反应点。下列说法不正确的是


| A.a=0.10 |
| B.N、P两点溶液中水的电离程度:N<P |
C.M、N两点溶液中 的物质的量之比大于1∶2 的物质的量之比大于1∶2 |
D.Q点溶液中存在: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】银氨溶液配制过程中,自由移动离子浓度的变化可以用电导率传感器来表征。某实验人员向盛有100 mL0.01 mol/LAgNO3 溶液的检测仪中逐滴加入0.1 mol/L氨水,图是随氨水加入电导率变化示意图,下列说法解错误的是


| A.a约为10mL |
B.当氨水体积小于a时发生主要反应的离子方程式为: Ag++NH3·H2O=AgOH↓+ |
C.当氨水体积大于3a时导电离子主要是[Ag(NH3)2]+和 |
| D.整个实验检测仪中溶液碱性先减弱后增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下﹐用0.4mol•L-1HCl溶液滴定20mL0.4mol•L-1Na2CO3溶液,溶液的pH和体系的压强随滴加盐酸体积的变化关系如图所示。下列说法正确的是


| A.整个滴定过程中可以一直用酚酞溶液作指示剂 |
| B.a→f点对应的溶液中,水的电离程度一直增大 |
| C.常温下,Ka2(H2CO3)≈2.5×10-11 |
D.e点对应的溶液中存在:c(Na+)>2c(CO )+2c(HCO )+2c(HCO )+2c(H2CO3) )+2c(H2CO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,关于物质的量浓度均为0.1 mol·L-1的盐酸、硫酸、醋酸的说法不正确的是( )
| A.等体积的三种酸中加入等体积、等物质的量浓度的NaOH,反应后溶液的pH:醋酸>盐酸>硫酸 |
| B.与等物质的量的NaOH溶液反应,消耗三种酸的体积:硫酸>盐酸=醋酸 |
| C.等物质的量浓度的NaHCO3溶液与三种酸反应,产生气体的起始速率:硫酸>盐酸>醋酸 |
| D.三种溶液的pH:醋酸>盐酸>硫酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知 是二元弱酸,常温下,向
是二元弱酸,常温下,向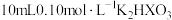 溶液中滴加
溶液中滴加 的盐酸,溶液的pH与所加盐酸体积的关系如图所示,下列说法正确的是
的盐酸,溶液的pH与所加盐酸体积的关系如图所示,下列说法正确的是
 是二元弱酸,常温下,向
是二元弱酸,常温下,向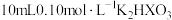 溶液中滴加
溶液中滴加 的盐酸,溶液的pH与所加盐酸体积的关系如图所示,下列说法正确的是
的盐酸,溶液的pH与所加盐酸体积的关系如图所示,下列说法正确的是
A.b点溶液中存在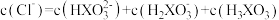 |
B.常温下, 的一级电离常数数量级是 的一级电离常数数量级是 |
C. 与足量的 与足量的 溶液反应的离子方程式为 溶液反应的离子方程式为 |
| D.水的电离程度:c>b>a |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】高铁酸盐在水溶液中有四种含铁型体,25°C时,它们的物质的量分数随pH的变化如图所示。下列叙述错误的是( )
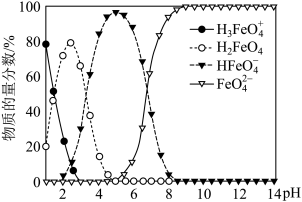

A.已知H3FeO4+的电离平衡常数分别为K1=2.5×10-2,K2=4.8×10-4,K3=5.0×10-8,当pH=4时,溶液中 =1.2 =1.2 |
| B.为获得尽可能纯净的高铁酸盐,应控制pH≥9 |
C.向pH=5的高铁酸盐溶液中加入KOH溶液,发生反应的离子方程式为HFeO +OH-=FeO +OH-=FeO +H2O +H2O |
D.pH=2时,溶液中主要含铁型体浓度的大小关系为c(H2FeO4 )>c(H3FeO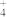 )>c(HFeO )>c(HFeO ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关电解质溶液的说法正确的是
| A.向盐酸中加入氨水至中性,溶液中c(NH4+)/c(Cl-)<1 |
| B.在蒸馏水中滴加浓H2SO4,Kw不变 |
| C.向0.1mol/L CH3COOH溶液中加入少量水,溶液中c(H+)/c(CH3COOH)增大 |
| D.将CH3COONa溶液从20℃升温至30℃,溶液中c(CH3COO-)/c(CH3COOH).c(OH-)增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在25℃,草酸(HOOCCOOH)电离常数:Ka1=5.9×10-2,,Ka2=6.4×10-5。下列说法正确的是
| A.0.1mol•L-1HOOCCOOH溶液的pH<1 |
B.将Na2C2O4溶液加水稀释时, 将增大 将增大 |
C.0.1mol•L-1NaHC2O4溶液中:c(HC2O )>c(H2C2O4)>c(C2O )>c(H2C2O4)>c(C2O ) ) |
| D.向草酸溶液加入Na2CO3粉末,有CO2放出,说明草酸为弱酸 |
您最近一年使用:0次

 在溶液中存在多种微粒形态,向溶液中逐滴加入
在溶液中存在多种微粒形态,向溶液中逐滴加入 、
、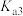 分别表示
分别表示 的第二步、第三步电离平衡常数。下列有关说法错误的是
的第二步、第三步电离平衡常数。下列有关说法错误的是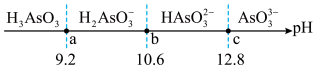
 点对应的溶液中,
点对应的溶液中,
 的第一步水解平衡常数的数量级为
的第一步水解平衡常数的数量级为
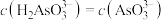 时,
时,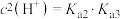
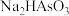 为酸式盐
为酸式盐

