在一定条件下,用草酸-草酸铵浸出废渣中的Fe2O3,平衡时浸出体系中含草酸根粒子及含Fe(Ⅲ)粒子的形态分布随pH变化如下图所示。下列说法正确的是
已知:①Fe3+和ox2−(代表草酸根)可以生成Fe(ox)+、Fe(ox) 和Fe(ox)
和Fe(ox) 三种配离子。
三种配离子。
②体系中草酸根的总浓度[ox2−]TOT = 4.54 mol/L(按折合成ox2−计)
体系中Fe(Ⅲ)的总浓度[Fe3+]TOT = 1.08 mol/L(按折合成Fe3+计)
已知:①Fe3+和ox2−(代表草酸根)可以生成Fe(ox)+、Fe(ox)
 和Fe(ox)
和Fe(ox) 三种配离子。
三种配离子。②体系中草酸根的总浓度[ox2−]TOT = 4.54 mol/L(按折合成ox2−计)
体系中Fe(Ⅲ)的总浓度[Fe3+]TOT = 1.08 mol/L(按折合成Fe3+计)
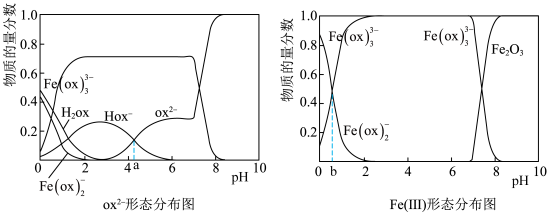
A.该条件下,酸性增强Fe(ox) 的物质的量分数增大 的物质的量分数增大 |
B.改变体系中草酸-草酸铵和Fe2O3的量,使[ox2-]TOT / [Fe3+]TOT = 3,体系中Fe(Ⅲ)全部以Fe(ox) 形态存在 形态存在 |
C.Hox− H+ + ox2− Ka2 = 10−a;Fe(ox) H+ + ox2− Ka2 = 10−a;Fe(ox) + ox2− + ox2−  Fe(ox) Fe(ox) K = 10−b K = 10−b |
| D.pH = 4时,c(Hox−) + c(ox2−) ≈ 1.3 mol/L |
更新时间:2024-04-01 19:16:01
|
【知识点】 化学平衡的有关计算
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】温度为T℃,向初始体积均为1L的两个密闭容器甲(恒容)、乙(恒压)中分别加入3molA和3molB发生反应:A(g)+B(g) xC(g),实验测得甲、乙两容器中A的转化率随时间变化如图所示。下列说法正确的是
xC(g),实验测得甲、乙两容器中A的转化率随时间变化如图所示。下列说法正确的是
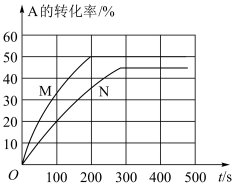
 xC(g),实验测得甲、乙两容器中A的转化率随时间变化如图所示。下列说法正确的是
xC(g),实验测得甲、乙两容器中A的转化率随时间变化如图所示。下列说法正确的是
| A.N为容器乙 |
| B.x等于或大于3 |
| C.平衡时,容器乙中C的浓度为2mol/L |
| D.N的平衡常数等于0.25 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】在一定温度下,将等量的气体分别通入起始体积相同的密闭容器Ⅰ和Ⅱ中,使其发生反应,t0时容器Ⅰ中达到化学平衡,X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是( )

①该反应的化学方程式为:3X+2Y 2Z
2Z
②若两容器中均达到平衡时,两容器的体积V(Ⅰ)<V(Ⅱ),则容器Ⅱ达到平衡所需时间大于t0
③若两容器中均达到平衡时,两容器中Z的物质的量分数相同,则Y为固态或液态
④若达平衡后,对容器Ⅱ升高温度时其体积增大,说明Z发生的反应为吸热反应

①该反应的化学方程式为:3X+2Y
 2Z
2Z②若两容器中均达到平衡时,两容器的体积V(Ⅰ)<V(Ⅱ),则容器Ⅱ达到平衡所需时间大于t0
③若两容器中均达到平衡时,两容器中Z的物质的量分数相同,则Y为固态或液态
④若达平衡后,对容器Ⅱ升高温度时其体积增大,说明Z发生的反应为吸热反应
| A.①②③④ | B.②③ | C.③④ | D.①②④ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】固体氨基甲酸铵H2NCOONH4可用于医药制药、(NH4)2CO3可用于做化肥,两者受热均发生分解反应。某一温度T℃下反应I: 的
的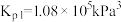 。该温度下单独发生反应II:
。该温度下单独发生反应II: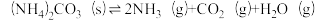 ,平衡后的总压为160kPa.该温度下、刚性容器中放入H2NCOONH4和(NH4)2CO3两种固体,平衡后两种固体均大量存在,下列关于两种固体共存并达到化学平衡态的说法正确的是
,平衡后的总压为160kPa.该温度下、刚性容器中放入H2NCOONH4和(NH4)2CO3两种固体,平衡后两种固体均大量存在,下列关于两种固体共存并达到化学平衡态的说法正确的是
 的
的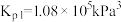 。该温度下单独发生反应II:
。该温度下单独发生反应II: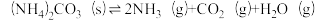 ,平衡后的总压为160kPa.该温度下、刚性容器中放入H2NCOONH4和(NH4)2CO3两种固体,平衡后两种固体均大量存在,下列关于两种固体共存并达到化学平衡态的说法正确的是
,平衡后的总压为160kPa.该温度下、刚性容器中放入H2NCOONH4和(NH4)2CO3两种固体,平衡后两种固体均大量存在,下列关于两种固体共存并达到化学平衡态的说法正确的是| A.NH3和CO2的比值不变说明反应I和II达到了化学平衡 |
| B.气态水的分压p(H2O)=70kPa |
| C.气体的总压约为184.8kPa |
D.反应II的平衡常数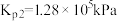 |
您最近一年使用:0次



