 具有易液化、含氢密度高、应用广泛等优点,
具有易液化、含氢密度高、应用广泛等优点, 的合成及应用是科学研究的重要课题。
的合成及应用是科学研究的重要课题。(1)以
 、
、 合成
合成 ,Fe是常用的催化剂。
,Fe是常用的催化剂。①
 分子空间构型为
分子空间构型为 极易溶于水的原因
极易溶于水的原因②实际生产中采用铁的氧化物
 、FeO,使用前用
、FeO,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
ⅰ.两种晶胞所含铁原子个数比为
ⅱ.图1晶胞的棱长为apm(
 ),则其密度
),则其密度
 (写出化简的表达式)。
(写出化简的表达式)。③我国科学家开发出Fe-LiH双中心催化剂,在合成
 中显示出高催化活性。第一电离能
中显示出高催化活性。第一电离能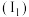 :
: ,从原子结构角度解释原因
,从原子结构角度解释原因(2)
 、
、 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。①
 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为②
 存在配位键,提供空轨道的是
存在配位键,提供空轨道的是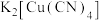 的配离子是
的配离子是 的配体是
的配体是(3)常温下
 是橙黄色液体,其分子结构如图所示。
是橙黄色液体,其分子结构如图所示。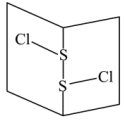
少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液。
 分子中含有
分子中含有(4)已知N、P、As为同一主族元素,则写出三种元素最简单氢化物沸点由高到低的顺序为(用化学式表示)
更新时间:2024/04/09 19:34:33
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】铜是重要的过渡金属元素,铜被广泛应用于电子工业和航天领域中。回答下列问题:
(1)基态铜原子的简化电子排布式为___________ ,同周期与铜原子未成对电子数相同的p区元素原子为___________ (填元素符号)。
(2)向CuSO4溶液中滴加氨水可以得到1∶1型离子化合物,其阳离子结构如图所示,阴离子为正四面体结构。

①该阳离子中存在的化学键类型为___________ (填序号)。
A.离子键 B.极性键 C.非极性键 D.σ键 E.π键 F.配位键 G.氢键
②该化合物加热时首先失去的组分是H2O,原因是___________ 。
③在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,最后溶解形成深蓝色溶液。写出此蓝色沉淀溶解的离子方程式:___________ ;
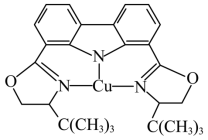
(3)我国科学家制取了一种铜的配合物如下图所示,该配合物中sp2杂化的碳原子与sp3杂化的碳原子个数比为___________ 。
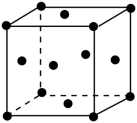
(4)金属铜是面心立方晶体,在上图的铜晶胞中,原子的空间利用率为___________ (用含有π的代数式表示)。
(1)基态铜原子的简化电子排布式为
(2)向CuSO4溶液中滴加氨水可以得到1∶1型离子化合物,其阳离子结构如图所示,阴离子为正四面体结构。

①该阳离子中存在的化学键类型为
A.离子键 B.极性键 C.非极性键 D.σ键 E.π键 F.配位键 G.氢键
②该化合物加热时首先失去的组分是H2O,原因是
③在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,最后溶解形成深蓝色溶液。写出此蓝色沉淀溶解的离子方程式:
(3)我国科学家制取了一种铜的配合物如下图所示,该配合物中sp2杂化的碳原子与sp3杂化的碳原子个数比为


(4)金属铜是面心立方晶体,在上图的铜晶胞中,原子的空间利用率为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某课题小组用比色法估测无色污水样品中苯酚的浓度。
已知:
①比色法是通过与标准色阶比对颜色确定有色物质浓度的方法。
②苯酚是一种水体污染物,在溶液中与氯化铁发生显色反应:

③当苯酚溶液pH=5.5时,其与氯化铁显色效果最佳。
(1)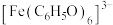 中,提供孤电子对用以形成配位键的原子是
中,提供孤电子对用以形成配位键的原子是_______ 。
(2)根据苯酚与氯化铁的显色原理,推测溶液的pH会影响显色效果,设计如下实验。
解释实验Ⅱ中产生相关现象的原因:_______ 。
(3)缓冲溶液可用于调节并维持待测污水样品pH在一定范围内。将0.2 某一元弱酸HA(
某一元弱酸HA(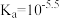 ),与0.1
),与0.1 的NaOH溶液等体积混合,配制成缓冲溶液。解释该缓冲溶液pH约为5.5的原因:
的NaOH溶液等体积混合,配制成缓冲溶液。解释该缓冲溶液pH约为5.5的原因:_______ 。
(4)取a 的标准苯酚溶液40mL,加入10mL缓冲溶液(不干扰显色反应),再加入0.1
的标准苯酚溶液40mL,加入10mL缓冲溶液(不干扰显色反应),再加入0.1
 溶液10mL,混合均匀,定容至100mL,得到溶液X。等差改变标准苯酚溶液的浓度,重复实验,得到标准色阶。
溶液10mL,混合均匀,定容至100mL,得到溶液X。等差改变标准苯酚溶液的浓度,重复实验,得到标准色阶。
①用比色法估测污水中苯酚浓度的操作是:取40mL污水样品,_______ 。
②下列说法不正确的是_______ (填字母序号)。
a.若苯酚溶液pH=6,加入缓冲溶液将促进苯酚的电离
b.溶液X颜色对应的苯酚浓度应标记为0.4a
c.溶液X中,有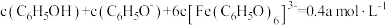
d.若将污水样品、缓冲溶液和 溶液用量均减为原来的1/10,其他操作相同,对比色阶,读取的苯酚浓度不变
溶液用量均减为原来的1/10,其他操作相同,对比色阶,读取的苯酚浓度不变
③为操作方便,用有效成分为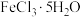 的药片代替上述
的药片代替上述 溶液。若每次检测投入一粒药片,为保证标准色阶准确有效,每片应含
溶液。若每次检测投入一粒药片,为保证标准色阶准确有效,每片应含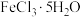
_______ g(保留到小数点后四位)。
(5)小组进一步探究发现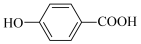 不能与
不能与 形成配合物,原因是
形成配合物,原因是_______ 。
(6)分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为 )。一种观点认为,苯酚羟基中的O原子是
)。一种观点认为,苯酚羟基中的O原子是 杂化则苯酚中的大π键可表示为
杂化则苯酚中的大π键可表示为_______ ,一定在同一平面上的原子有_______ 个。
已知:
①比色法是通过与标准色阶比对颜色确定有色物质浓度的方法。
②苯酚是一种水体污染物,在溶液中与氯化铁发生显色反应:

③当苯酚溶液pH=5.5时,其与氯化铁显色效果最佳。
(1)
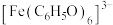 中,提供孤电子对用以形成配位键的原子是
中,提供孤电子对用以形成配位键的原子是(2)根据苯酚与氯化铁的显色原理,推测溶液的pH会影响显色效果,设计如下实验。
| 实验 | 操作 | 现象 |
| Ⅰ | 向2mL苯酚溶液(调节pH=9)滴加0.1  溶液 溶液 | 生成红褐色沉淀 |
| Ⅱ | 向实验Ⅰ所得悬浊液中逐滴加入0.1 盐酸 盐酸 | 沉淀逐渐溶解,溶液变为紫色;继续滴加盐酸,溶液由紫色变为浅黄色 |
(3)缓冲溶液可用于调节并维持待测污水样品pH在一定范围内。将0.2
 某一元弱酸HA(
某一元弱酸HA(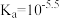 ),与0.1
),与0.1 的NaOH溶液等体积混合,配制成缓冲溶液。解释该缓冲溶液pH约为5.5的原因:
的NaOH溶液等体积混合,配制成缓冲溶液。解释该缓冲溶液pH约为5.5的原因:(4)取a
 的标准苯酚溶液40mL,加入10mL缓冲溶液(不干扰显色反应),再加入0.1
的标准苯酚溶液40mL,加入10mL缓冲溶液(不干扰显色反应),再加入0.1
 溶液10mL,混合均匀,定容至100mL,得到溶液X。等差改变标准苯酚溶液的浓度,重复实验,得到标准色阶。
溶液10mL,混合均匀,定容至100mL,得到溶液X。等差改变标准苯酚溶液的浓度,重复实验,得到标准色阶。①用比色法估测污水中苯酚浓度的操作是:取40mL污水样品,
②下列说法不正确的是
a.若苯酚溶液pH=6,加入缓冲溶液将促进苯酚的电离
b.溶液X颜色对应的苯酚浓度应标记为0.4a

c.溶液X中,有
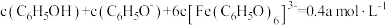
d.若将污水样品、缓冲溶液和
 溶液用量均减为原来的1/10,其他操作相同,对比色阶,读取的苯酚浓度不变
溶液用量均减为原来的1/10,其他操作相同,对比色阶,读取的苯酚浓度不变③为操作方便,用有效成分为
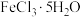 的药片代替上述
的药片代替上述 溶液。若每次检测投入一粒药片,为保证标准色阶准确有效,每片应含
溶液。若每次检测投入一粒药片,为保证标准色阶准确有效,每片应含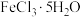
(5)小组进一步探究发现
 不能与
不能与 形成配合物,原因是
形成配合物,原因是(6)分子中的大π键可用符号
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为 )。一种观点认为,苯酚羟基中的O原子是
)。一种观点认为,苯酚羟基中的O原子是 杂化则苯酚中的大π键可表示为
杂化则苯酚中的大π键可表示为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】(1)三价铬离子能形成多种配位化合物。[Cr(NH3)3(H2O)2 Cl]2+中提供电子对形成配位键的原子是___________ ,中心离子的配位数为___________ 。
(2) [Cr(NH3)3(H2O)2 Cl]2+中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示。
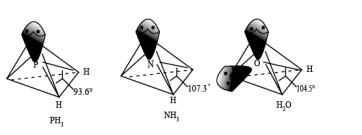
PH3中P的杂化类型是___________ 。NH3的沸点比PH3的___________ ,原因是___________ ,H2O的键角小于NH3的,分析原因___________ 。
(2) [Cr(NH3)3(H2O)2 Cl]2+中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示。

PH3中P的杂化类型是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铜是人类广泛使用的一种金属,钼是一种难熔的稀有金属。两种物质在生产生活中都有着重要的应用。回答下列问题:
(1)基态Cu原子价层电子排布式为___________ ,在周期表中,Cu元素属于___________ 区,Cu能与拟卤素(SCN)2反应。拟卤素(SCN)2对应的酸有两种,理论上异硫氰酸(H-N=C=S)的沸点高于硫氰酸(H-S-CN),其原因为___________ ,写出一种与SCN-互为等电子体分子的化学式___________ 。
(2)将氨水逐滴加入硫酸铜溶液中,先生成蓝色沉淀,继续滴加氨水,沉淀溶解并得到深蓝色溶液,写出沉淀溶解反应的离子方程式:___________ 。
(3)向深蓝色溶液中继续加入乙醇,会析出深蓝色的晶体[Cu(NH3)4]SO4·H2O。在该晶体中1mol[Cu(NH3)4]2+含有σ键的数目为___________ 。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子的原因是___________ 。
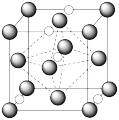
(4)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的八面体空隙中,晶胞结构如图所示。氮化钼的化学式为___________ ,氮化钼晶胞边长为anm,晶体的密度ρ=___________ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)基态Cu原子价层电子排布式为
(2)将氨水逐滴加入硫酸铜溶液中,先生成蓝色沉淀,继续滴加氨水,沉淀溶解并得到深蓝色溶液,写出沉淀溶解反应的离子方程式:
(3)向深蓝色溶液中继续加入乙醇,会析出深蓝色的晶体[Cu(NH3)4]SO4·H2O。在该晶体中1mol[Cu(NH3)4]2+含有σ键的数目为
(4)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的八面体空隙中,晶胞结构如图所示。氮化钼的化学式为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】科学家开发一种氮掺杂氢化镥(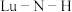 )材料,在1 GPa压强下,该材料表现出室温超导特性。回答下列问题:
)材料,在1 GPa压强下,该材料表现出室温超导特性。回答下列问题:
(1)已知基态Lu(镥)原子的价层电子排布式为
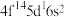 ,它位于元素周期表第
,它位于元素周期表第___________ 周期___________ 族,有___________ 个未成对电子。
(2)与氮同主族元素的最简单氢化物的稳定性、沸点随着原子序数递增而变化的规律如图所示。
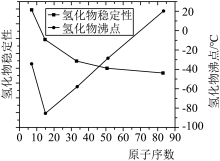
①氮族元素的最简单氢化物中,沸点最低的是___________ (填化学式,下同),最稳定的是___________ 。
② 的沸点高于
的沸点高于 ,其主要原因是
,其主要原因是___________ 。
(3)某药品活性成分的结构简式如图所示。
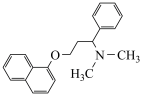
该分子中N原子的杂化类型是___________ ,1个该分子含___________ 个手性碳原子。
(4)含N的分子或离子是常见的配体。例如,雷氏盐的化学式为
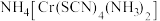 ,常作分析试剂。
,常作分析试剂。
①雷氏盐中 的空间结构为
的空间结构为___________ , 中的N
中的N___________ (填“是”或“不是”)配位原子。
②预测:雷氏盐中阴离子的空间结构最可能是___________ (填标号)。
A.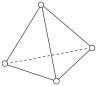 B.
B.  C.
C.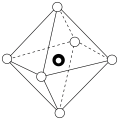 D.
D.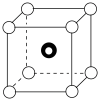
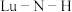 )材料,在1 GPa压强下,该材料表现出室温超导特性。回答下列问题:
)材料,在1 GPa压强下,该材料表现出室温超导特性。回答下列问题:(1)已知基态Lu(镥)原子的价层电子排布式为
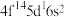 ,它位于元素周期表第
,它位于元素周期表第(2)与氮同主族元素的最简单氢化物的稳定性、沸点随着原子序数递增而变化的规律如图所示。

①氮族元素的最简单氢化物中,沸点最低的是
②
 的沸点高于
的沸点高于 ,其主要原因是
,其主要原因是(3)某药品活性成分的结构简式如图所示。

该分子中N原子的杂化类型是
(4)含N的分子或离子是常见的配体。例如,雷氏盐的化学式为
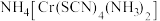 ,常作分析试剂。
,常作分析试剂。①雷氏盐中
 的空间结构为
的空间结构为 中的N
中的N②预测:雷氏盐中阴离子的空间结构最可能是
A.
 B.
B.  C.
C. D.
D.
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】回答下列问题
(1)基态铜原子核外有___________ 种不同空间运动状态的电子;C、N、F、Cu四种元素第一电离能从小至大的顺序为___________ 。
(2)化合物 、
、 常温下均为气体,沸点较高的是
常温下均为气体,沸点较高的是___________ ; 中氮原子的杂化方式是
中氮原子的杂化方式是___________ 。
(3)将无水硫酸铜溶解在一定量的水中,再加入过量氨水,溶液变为深蓝色,该深蓝色离子。 内存在的化学键有
内存在的化学键有___________ 。
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
(4)基态Co的价电子排布图为___________ ,Co和Fe的逐级电离能(kJ/mol)如表,Fe的 大于Co的
大于Co的 原因是
原因是___________ 。
(1)基态铜原子核外有
(2)化合物
 、
、 常温下均为气体,沸点较高的是
常温下均为气体,沸点较高的是 中氮原子的杂化方式是
中氮原子的杂化方式是(3)将无水硫酸铜溶解在一定量的水中,再加入过量氨水,溶液变为深蓝色,该深蓝色离子。
 内存在的化学键有
内存在的化学键有A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
(4)基态Co的价电子排布图为
 大于Co的
大于Co的 原因是
原因是| 元素 |  |  |  |  |  | … |
| Fe | 462.5 | 1561.9 | 2957 | 5290 | 7240 | |
| Co | 760.4 | 1648 | 3232 | 4950 | 7670 |
您最近半年使用:0次
【推荐1】硫及其化合物有许多用途。请回答下列问题。
(1)基态硫离子价层电子的轨道表达式为___________ ,其电子填充的最高能级的轨道数为___________ 。
(2)常见含硫的物质有单质硫(S8)、SO2、Na2S、K2S等,四种物质的熔点由高到低的顺序依次为___________ ,原因是___________ 。
(3)方铅矿(即硫化铅)是一种比较常见的矿物,酸溶反应为:PbS+4HCl(浓)=H2[PbCl4]+H2S↑,则H2[PbCl4]中配位原子是_________ ,第一电离能I1(Cl)___________ I1(S)(填“>”、“<”或¨=”),H2S中硫的杂化方式为_______ ,下列分子空间的构型与H2S相同的有___________ 。
A.H2O B.SO3 C.O3 D.CH4
(4)方铅矿的立方晶胞如图所示,硫离子采取面心立方堆积,铅离子填在由硫离子形成的___________ 空隙中。已知晶体密度为ρg·cm-3,阿伏伽德罗常数的值为NA,则晶胞中硫离子与铅离子最近的距离为___________ nm。

(1)基态硫离子价层电子的轨道表达式为
(2)常见含硫的物质有单质硫(S8)、SO2、Na2S、K2S等,四种物质的熔点由高到低的顺序依次为
(3)方铅矿(即硫化铅)是一种比较常见的矿物,酸溶反应为:PbS+4HCl(浓)=H2[PbCl4]+H2S↑,则H2[PbCl4]中配位原子是
A.H2O B.SO3 C.O3 D.CH4
(4)方铅矿的立方晶胞如图所示,硫离子采取面心立方堆积,铅离子填在由硫离子形成的

您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、F六种元素,它们的相关信息如下:①原子序数依次增大,②A和C的L能层中都有两个未成对的电子,③C、D同主族且位于相邻周期,④E和F的原子序数相差3,F原子除最外能层只有1个电子外,其余各能层均全充满。根据以上信息填空(涉及的具体物质用元素符号或化学式回答):
(2)基态D原子中,具有______ 种不同能量的电子,E2+的价层电子轨道表达式是______ 。
(2)六种元素中电负性最强的元素是______ 。
(3)A元素的最高价氧化物中心原子采取的轨道杂化方式为______ ,D元素的最简单氢化物的VSEPR模型为______ 。
(4)与化合物AC2互为等电子体的分子的分子式为______ (任写一种,下同),与化合物AC2互为等电子体且含有的元素只能是上述六种元素中的一价阴离子为______ 。
(5)某种化合物由D、E、F三种元素组成,其晶胞结构如图所示,则其化学式为______ ,该晶胞上下底面为正方形,侧面与底面垂直,根据图中所示的数据列式计算该晶体的密度:ρ=______ g·cm-3(只要求列出计算式)。

(2)基态D原子中,具有
(2)六种元素中电负性最强的元素是
(3)A元素的最高价氧化物中心原子采取的轨道杂化方式为
(4)与化合物AC2互为等电子体的分子的分子式为
(5)某种化合物由D、E、F三种元素组成,其晶胞结构如图所示,则其化学式为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】结构化学的世界异彩纷呈,美不胜收。
Ⅰ.芦笋中的天冬酰胺结构如图所示,具有提高身体免疫力的功效。

(1)天冬酰胺所含元素中,___________ 元素的基态原子核外未成对电子数最多。
(2)天冬酰胺中碳原子的杂化轨道类型有___________ 种。
Ⅱ. 和
和 的参数对比见下表。
的参数对比见下表。
(3) 的空间构型为
的空间构型为___________ 。
(4) 的沸点低于
的沸点低于 的原因是
的原因是___________ 。
Ⅲ.铜、铁、锌是常见的过渡金属元素,可以形成多种化合物。
(5)已知 与
与 形成的配合物可表示成
形成的配合物可表示成 ,在该配合物中,
,在该配合物中, 的4s轨道及4p轨道通过sp杂化接受
的4s轨道及4p轨道通过sp杂化接受 提供的孤电子对。则
提供的孤电子对。则 中
中 与n个氮原子的空间结构呈
与n个氮原子的空间结构呈___________ 形,n=___________ 。
(6)Fe能与N形成一种磁性材料,其晶胞结构如图所示。
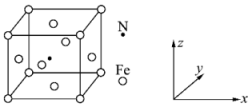
①该磁性材料的化学式为___________ 。
②Fe原子的坐标参数为 、
、 、
、 、(0,0,0),则N原子的坐标参数为
、(0,0,0),则N原子的坐标参数为___________ 。
(7) 与
与 形成的一种晶胞结构如图所示(黑球表示
形成的一种晶胞结构如图所示(黑球表示 ,白球表示
,白球表示 )。
)。
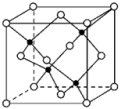
则 的配位数为
的配位数为___________ 。晶胞边长为anm,设ZnS的相对分子质量为M,阿伏加德罗常数的值为 ,其晶体密度的计算表达式为
,其晶体密度的计算表达式为___________  (列出表达式,不必化简)。
(列出表达式,不必化简)。
Ⅰ.芦笋中的天冬酰胺结构如图所示,具有提高身体免疫力的功效。

(1)天冬酰胺所含元素中,
(2)天冬酰胺中碳原子的杂化轨道类型有
Ⅱ.
 和
和 的参数对比见下表。
的参数对比见下表。| 化学式 | 键长/nm | 沸点℃ |
 | 1.34 | -60.75 |
 | 1.47 | -41.50 |
 的空间构型为
的空间构型为(4)
 的沸点低于
的沸点低于 的原因是
的原因是Ⅲ.铜、铁、锌是常见的过渡金属元素,可以形成多种化合物。
(5)已知
 与
与 形成的配合物可表示成
形成的配合物可表示成 ,在该配合物中,
,在该配合物中, 的4s轨道及4p轨道通过sp杂化接受
的4s轨道及4p轨道通过sp杂化接受 提供的孤电子对。则
提供的孤电子对。则 中
中 与n个氮原子的空间结构呈
与n个氮原子的空间结构呈(6)Fe能与N形成一种磁性材料,其晶胞结构如图所示。

①该磁性材料的化学式为
②Fe原子的坐标参数为
 、
、 、
、 、(0,0,0),则N原子的坐标参数为
、(0,0,0),则N原子的坐标参数为(7)
 与
与 形成的一种晶胞结构如图所示(黑球表示
形成的一种晶胞结构如图所示(黑球表示 ,白球表示
,白球表示 )。
)。
则
 的配位数为
的配位数为 ,其晶体密度的计算表达式为
,其晶体密度的计算表达式为 (列出表达式,不必化简)。
(列出表达式,不必化简)。
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】钛被称为继铁、铝之后的第三金属,请回答下列问题:
(1)金红石(TiO2)是钛的主要矿物之一,基态Ti原子价层电子的排布图为__ ,基态O原子电子占据最高能级的电子云轮廓图为__ 形。
(2)以TiO2为原料可制得TiCl4,TiCl4的熔、沸点分别为205K、409K,均高于结构与其相似的CCl4,主要原因是__ 。
(3)TiCl4可溶于浓盐酸得H2[TiCl6],向溶液中加入NH4Cl浓溶液可析出黄色的(NH4)2[TiCl6]晶体。该晶体中微观粒子之间的作用力有__ 。
A.离子键 B.共价键 C.分子间作用力 D.氢键 E.范德华力
(4)TiCl4可与CH3CH2OH、HCHO、CH3OCH3等有机小分子形成加合物。上述三种小分子中C原子的VSEPR模型不同于其他分子的是__ ,该分子中C的轨道杂化类型为__ 。
(5)TiO2与BaCO3一起熔融可制得钛酸钡。
①BaCO3中阴离子的立体构型为__ 。
②经X射线分析鉴定,钛酸钡的晶胞结构如图所示(Ti4+、Ba2+均与O2-相接触),则钛酸钡的化学式为___ 。

(1)金红石(TiO2)是钛的主要矿物之一,基态Ti原子价层电子的排布图为
(2)以TiO2为原料可制得TiCl4,TiCl4的熔、沸点分别为205K、409K,均高于结构与其相似的CCl4,主要原因是
(3)TiCl4可溶于浓盐酸得H2[TiCl6],向溶液中加入NH4Cl浓溶液可析出黄色的(NH4)2[TiCl6]晶体。该晶体中微观粒子之间的作用力有
A.离子键 B.共价键 C.分子间作用力 D.氢键 E.范德华力
(4)TiCl4可与CH3CH2OH、HCHO、CH3OCH3等有机小分子形成加合物。上述三种小分子中C原子的VSEPR模型不同于其他分子的是
(5)TiO2与BaCO3一起熔融可制得钛酸钡。
①BaCO3中阴离子的立体构型为
②经X射线分析鉴定,钛酸钡的晶胞结构如图所示(Ti4+、Ba2+均与O2-相接触),则钛酸钡的化学式为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】联氨(N2H4)可以用于处理高压锅炉水中的氧,防止锅炉被腐蚀,其中一种可能的反应机理如图所示。回答下列问题:
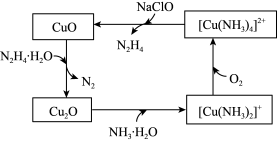
(1)Cu2+基态核外电子排布式为___ 。
(2)1molN2H4•H2O含σ键的数目为___ 。
(3)Cu2O与NH3•H2O反应能形成较稳定的Cu(NH3)2+的原因是__ 。
(4)N2H4的晶体类型是___ 。N2H4与O2的相对分子质量相近,但N2H4的熔点(2℃),沸点(114℃)分别远远高于O2的熔点(218℃),沸点(183℃),原因是___ 。
(5)NaClO发生水解可生成HClO,HClO的空间构型是__ ,中心原子的杂化类型是__ 。
(6)已知Cu2O晶胞的结构如图所示:

①在该晶胞中,Cu+的配位数是___ 。
②已知该晶体密度为dg/cm3,NA表示阿伏加 德罗常数的数值,则晶胞参数α为___ nm(用含d和NA的代数式表示)。

(1)Cu2+基态核外电子排布式为
(2)1molN2H4•H2O含σ键的数目为
(3)Cu2O与NH3•H2O反应能形成较稳定的Cu(NH3)2+的原因是
(4)N2H4的晶体类型是
(5)NaClO发生水解可生成HClO,HClO的空间构型是
(6)已知Cu2O晶胞的结构如图所示:

①在该晶胞中,Cu+的配位数是
②已知该晶体密度为dg/cm3,NA表示阿伏加 德罗常数的数值,则晶胞参数α为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】有色金属行业发展蕴藏着巨大潜力。目前,全世界消费量排在前五位为铜、铝、铅、锌、镍。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于___ 晶体;基态Ni原子的价电子电子排布式为____ 。
(2)铜原子的电子占有____ 种能量不同的原子轨道。
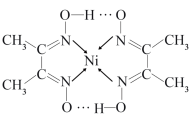
(3)配合物分子内(如图)的作用力有_____ (填编号)。
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
(4)很多不饱和有机物在Ni催化下可以与H2发生加成反应。如 ①CH2=CH2、②CH≡CH、③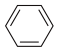 、④HCHO等,其中分子中C原子为SP2杂化的有
、④HCHO等,其中分子中C原子为SP2杂化的有____ (填物质序号),预测HCHO分子的立体结构为_____ 形。
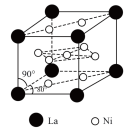
(5)氢气是新型清洁能源,镧(La)和镍(Ni)的合金可做储氢材料。该合金的晶胞如右图所示,晶胞中心有一个镍原子,其他镍原子都在晶胞面上,镧原子都在晶胞顶点上。该晶体的化学式为______ 。
(6)邻羟基苯甲醛的沸点____ (填大于,小于或等于)对羟基苯甲醛的沸点。

(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于
(2)铜原子的电子占有
(3)配合物分子内(如图)的作用力有

A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
(4)很多不饱和有机物在Ni催化下可以与H2发生加成反应。如 ①CH2=CH2、②CH≡CH、③
 、④HCHO等,其中分子中C原子为SP2杂化的有
、④HCHO等,其中分子中C原子为SP2杂化的有(5)氢气是新型清洁能源,镧(La)和镍(Ni)的合金可做储氢材料。该合金的晶胞如右图所示,晶胞中心有一个镍原子,其他镍原子都在晶胞面上,镧原子都在晶胞顶点上。该晶体的化学式为
(6)邻羟基苯甲醛的沸点
您最近半年使用:0次



