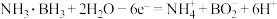鲍林提出杂化轨道理论能解释分子的空间结构,下列关于粒子的描述正确的是
选项 | 粒子 | 空间结构 | 解释 |
A |
| V形 | S原子采取 |
B |
| 直线形 | C原子采取 |
C |
| 平面形 | C原子采取 |
D |
| 四面体形 | Cl原子采取 |
| A.A | B.B | C.C | D.D |
更新时间:2024-04-11 11:34:55
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关比较正确的是
| A.熔点:CH4>SiH4>GeH4>SnH4 |
| B.键角: H2Se>H2S>H2O |
| C.键的极性:N-H键>O-H键>F-H键 |
| D.热稳定性:HF>H2O>NH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列化学用语表示正确的是
A.H2S分子的球棍模型: | B.AlCl3的价层电子对互斥模型: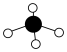 |
C.KI的电子式: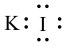 | D. 基态原子的轨道表示式为 基态原子的轨道表示式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列分子的键角为109°28′的是
| A.CCl4 | B.NH3 | C.H2O | D.P4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关化学用语表示正确的是
A. 的空间填充模型: 的空间填充模型: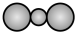 | B.N,N-二甲基甲酰胺的结构简式: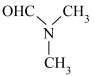 |
C. 分子的球棍模型: 分子的球棍模型: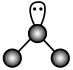 | D. 的电子式: 的电子式: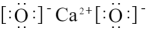 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在水溶液中甲醛能与 发生反应:
发生反应: 。下列说法错误的是
。下列说法错误的是
 发生反应:
发生反应: 。下列说法错误的是
。下列说法错误的是| A.K2[Zn(CN)4]中所含的化学键有离子键、共价键和配位键 |
| B.HCHO和BF3中心原子的价层电子对数相同,H-C-H键角大于F-B-F键角 |
C. 和H2O与Zn2+的配位能力: 和H2O与Zn2+的配位能力: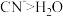 |
D. 中,σ键和π键数目之比为1∶1 中,σ键和π键数目之比为1∶1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】硒(Se)是第ⅥA族元素,则SeS3的分子立体构型是
| A.正四面体形 | B.V形 | C.三角锥形 | D.平面三角形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
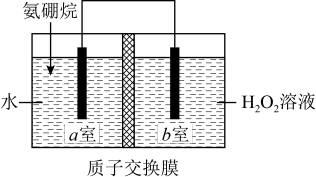
【推荐3】SO2、氮氧化物(NOx)等均是空气污染物。研究表明,NOx(x=1或2)、SO2与雾霾的形成有关,过程如图所示:
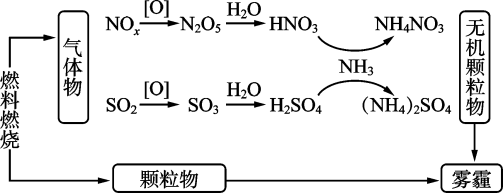
SO2、氮氧化物需处理后才能排放,可用NaOH溶液、氨水吸收处理,主要反应为:
NO+NO2+2OH-= 2NO +H2O
+H2O
2NO2+2OH-= NO +NO
+NO +H2O
+H2O
SO2+2NH3·H2O = 2NH +SO
+SO +H2O等
+H2O等
下列有关含氮、含硫微粒的说法正确的是

SO2、氮氧化物需处理后才能排放,可用NaOH溶液、氨水吸收处理,主要反应为:
NO+NO2+2OH-= 2NO
 +H2O
+H2O2NO2+2OH-= NO
 +NO
+NO +H2O
+H2OSO2+2NH3·H2O = 2NH
 +SO
+SO +H2O等
+H2O等下列有关含氮、含硫微粒的说法正确的是
| A.SO2转化为SO3时,分子的键角变小 |
B.NO 和NO 和NO 中N原子轨道的杂化类型均为sp3杂化 中N原子轨道的杂化类型均为sp3杂化 |
C.NH 和SO 和SO 的空间构型都是正四面体形 的空间构型都是正四面体形 |
| D.SO2、SO3和NO2均为酸性氧化物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】干冰(固态二氧化碳)在﹣78℃时可直接升华为气体,其晶胞结构如下图所示。下列说法不正确的是


| A.干冰升华时需克服分子间作用力 |
| B.每个晶胞中含有4个CO2分子 |
| C.每个CO2分子周围有12个紧邻CO2分子 |
| D.CO2中有C=O键,中心原子C是sp2杂化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】硼单质及其化合物有重要的应用。硼晶体熔点为2076℃,可形成多种卤化物, 可与
可与 反应生成
反应生成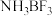 ,
, 可与
可与 反应生成乙硼烷
反应生成乙硼烷 (标准燃烧热为
(标准燃烧热为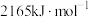 ),其分子中一个硼与周围的四个氢形成正四面体,结构式为
),其分子中一个硼与周围的四个氢形成正四面体,结构式为 ,具有还原性。乙硼烷也可与NaH反应生成
,具有还原性。乙硼烷也可与NaH反应生成 ,−1价的氢有较强的还原性,是一种常用的还原剂。下列说法正确的是
,−1价的氢有较强的还原性,是一种常用的还原剂。下列说法正确的是
 可与
可与 反应生成
反应生成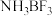 ,
, 可与
可与 反应生成乙硼烷
反应生成乙硼烷 (标准燃烧热为
(标准燃烧热为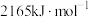 ),其分子中一个硼与周围的四个氢形成正四面体,结构式为
),其分子中一个硼与周围的四个氢形成正四面体,结构式为 ,具有还原性。乙硼烷也可与NaH反应生成
,具有还原性。乙硼烷也可与NaH反应生成 ,−1价的氢有较强的还原性,是一种常用的还原剂。下列说法正确的是
,−1价的氢有较强的还原性,是一种常用的还原剂。下列说法正确的是| A.硼晶体为分子晶体 | B.基态硼原子的核外电子排布式为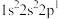 |
C. 与 与 中心原子均为 中心原子均为 杂化 杂化 | D. 晶体中存在离子键、共价键、氢键 晶体中存在离子键、共价键、氢键 |
您最近一年使用:0次



 杂化
杂化
 和
和 的中心原子均为
的中心原子均为 中有每个原子均满足最外层8电子稳定结构
中有每个原子均满足最外层8电子稳定结构 分子的立体构型为V形
分子的立体构型为V形 和雌黄(
和雌黄( ,其结构如图所示)是提取砷的主要矿物原料,二者在自然界中共生,
,其结构如图所示)是提取砷的主要矿物原料,二者在自然界中共生, 有如下反应:
有如下反应: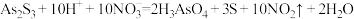 。下列说法
。下列说法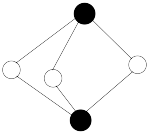
 的VSEPR模型为正四面体形
的VSEPR模型为正四面体形 应该在正极附近逸出
应该在正极附近逸出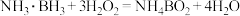 。下列说法正确的是
。下列说法正确的是