饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为N2,反应的离子方程式为
还原为N2,反应的离子方程式为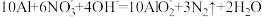 。设
。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为N2,反应的离子方程式为
还原为N2,反应的离子方程式为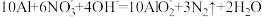 。设
。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.消耗lmolAl,反应转移的电子数为 | B. 的空间构型是正四面体形 的空间构型是正四面体形 |
C.标准状况下,11.2LN2中含π键数目为 | D.2mol液态水中含有的氢键数目少于 |
更新时间:2024-04-13 21:34:03
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.0.1molI2与lmolH2反应,生成HI分子数为0.2NA |
B.25℃时,1L0.2mol/LCH3COONH4溶液(pH=7)中, 数为0.2NA 数为0.2NA |
| C.标准状况下,11.2L苯中,含有0.5NA个苯分子 |
D.20g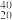 Ca2+含有的电子数为9NA Ca2+含有的电子数为9NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】设 代表阿伏加德罗常数的值。臭氧能氧化
代表阿伏加德罗常数的值。臭氧能氧化 ,通常用于处理电镀工业含氰废水,其化学原理为
,通常用于处理电镀工业含氰废水,其化学原理为 。下列叙述正确的是
。下列叙述正确的是
 代表阿伏加德罗常数的值。臭氧能氧化
代表阿伏加德罗常数的值。臭氧能氧化 ,通常用于处理电镀工业含氰废水,其化学原理为
,通常用于处理电镀工业含氰废水,其化学原理为 。下列叙述正确的是
。下列叙述正确的是A.处理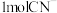 时生成还原产物 时生成还原产物 的分子数为 的分子数为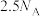 |
B.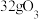 和 和 的混合气体中含氧原子数为 的混合气体中含氧原子数为 |
C.每生成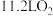 的同时生成 的同时生成 数为 数为 |
D.由离子方程式知每生成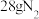 时转移电子数为 时转移电子数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏加 德罗常数的值,下列说法正确的是
| A.25 ℃时,pH=11的Na2CO3溶液中水电离出的OH-的数目为0.001NA |
| B.0.1mol甲基中所含电子数目为NA |
| C.28g乙烯、乙烷混合气体中所含原子数大于6NA |
| D.5.6g铁与硝酸完全反应时转移的电子数目为0.3NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用NA表示阿伏加 德罗常数的值。下列说法中正确的是
| A.25℃时,pH=13的NaOH溶液中含有OH-的数目为0.1 NA |
| B.60 g二氧化硅中Si—O键个数为4NA个 |
| C.标准状况下,22.4 L SO2与0.5 mol O2混合反应,生成NA个SO3分子 |
| D.1mol甲烷与1 mol乙炔中的σ键均为3NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用NA表示阿伏加德罗常数,下列说法正确的是
A.常温常压下, 乙烯共用电子对数为4 NA 乙烯共用电子对数为4 NA |
B. 乙醛与足量新制 乙醛与足量新制 悬浊液反应,转移电子数目为NA 悬浊液反应,转移电子数目为NA |
C.标准状况下, 戊烷充分燃烧后生成气态产物的分子数为 戊烷充分燃烧后生成气态产物的分子数为 |
D. 乙烯和乙醇的混合物完全燃烧所消耗的氧气分子数一定为0.3 NA 乙烯和乙醇的混合物完全燃烧所消耗的氧气分子数一定为0.3 NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】设NA为阿伏加 德罗常数的值。下列说法正确的是
| A.标准状况下,2.24L SO3中所含原子数为0.4NA |
| B.l0mL 12mol/L盐酸与足量MnO2加热反应,制得Cl2的分子数为0. 03NA |
| C.0. 1mol CH4与0.4mol Cl2在光照下充分反应,生成CCl4的分子数为0.1NA |
| D.常温常压下,6g乙酸中含有C-H键的数目为0.3NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】亚硝酰氟(FNO)是一种工业稳定剂,可通过反应N2O4 +CsF=FNO+CsNO3制得。下列说法正确的是
A.氧原子基态价电子轨道表达式为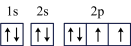 |
B.CsF的电子式为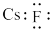 |
| C.FNO的空间构型为直线形 |
| D.CsNO3中含有离子键与共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知:硫代硫酸根( )可看作是
)可看作是 中的一个O原子被S原子取代的产物,
中的一个O原子被S原子取代的产物, 作为配体可提供孤电子对与
作为配体可提供孤电子对与 形成
形成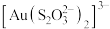 。下列有关说法正确的是
。下列有关说法正确的是
 )可看作是
)可看作是 中的一个O原子被S原子取代的产物,
中的一个O原子被S原子取代的产物, 作为配体可提供孤电子对与
作为配体可提供孤电子对与 形成
形成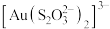 。下列有关说法正确的是
。下列有关说法正确的是A.SO3与 的键角相等 的键角相等 |
B. 与 与 的空间构型相同 的空间构型相同 |
| C. SO3是极性分子,故SO3易溶于水 |
D. 作为配体时,两种硫原子中只有端基硫原子能提供孤电子对 作为配体时,两种硫原子中只有端基硫原子能提供孤电子对 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列化学用语或图示正确的是
A.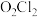 的球棍模型: 的球棍模型: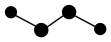 |
B.虚线表示邻羟基苯甲醛的分子内氢键: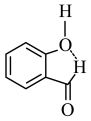 |
C.在氨水中, 与 与 分子间的氢键主要形式可表示为: 分子间的氢键主要形式可表示为: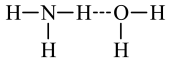 |
D.某种壬烷的键线式: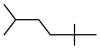 |
您最近一年使用:0次
【推荐2】尿黑酸症是由酪氨酸在人体内非正常代谢而产生的一种疾病。其转化过程如图所示,下列说法正确的是
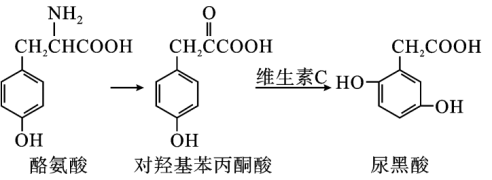

| A.尿黑酸和对羟基苯丙酮酸均不能形成分子内氢键 |
| B.酪氨酸和对羟基苯丙酮酸所含的含氧官能团相同 |
| C.尿黑酸能与Fe3+反应制备特种墨水 |
| D.1 mol对羟基苯丙酮酸分别可以和2 mol NaHCO3和4 mol H2完全反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列叙述正确的个数是
①稀有气体原子与同周期ⅠA、ⅡA族元素的简单阳离子具有相同的核外电子排布
②第n主族元素其最高价氧化物分子式为R2On,氢化物分子式为RHn (n≥4)
③若R2﹣和M+的电子层结构相同,则原子序数:R>M
④含有共价键的化合物一定是共价化合物
⑤共价化合物中不可能含有离子键
⑥键角大小SO3>SO2>SO >SO
>SO
⑦由于非金属性:F>Cl>Br>I,所以酸性:HF>HCl>HBr>HI
⑧HF分子很稳定是由于HF分子之间能形成氢键
⑨分子极性HF>HCl>HBr>HI
⑩熔沸点HF<HCl<HBr<HI
①稀有气体原子与同周期ⅠA、ⅡA族元素的简单阳离子具有相同的核外电子排布
②第n主族元素其最高价氧化物分子式为R2On,氢化物分子式为RHn (n≥4)
③若R2﹣和M+的电子层结构相同,则原子序数:R>M
④含有共价键的化合物一定是共价化合物
⑤共价化合物中不可能含有离子键
⑥键角大小SO3>SO2>SO
 >SO
>SO
⑦由于非金属性:F>Cl>Br>I,所以酸性:HF>HCl>HBr>HI
⑧HF分子很稳定是由于HF分子之间能形成氢键
⑨分子极性HF>HCl>HBr>HI
⑩熔沸点HF<HCl<HBr<HI
| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次

 、
、 、
、 、
、 、三聚的
、三聚的 等,三聚的
等,三聚的
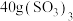 分子中含有
分子中含有 键
键 杂化
杂化

