某中学研究性学习小组的以黄铁矿 (杂质为石英)为原料,设计了如下工艺流程:
(杂质为石英)为原料,设计了如下工艺流程:
(1)在空气中焙烧黄铁矿的化学方程式为:__________________________ 。
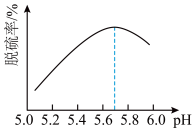
(2)研究发现,pH和温度对石灰石浆液的脱硫效率有一定影响。当烟气通入速度一定时,石灰石浆液的脱硫率与浆液pH的关系如图所示( )。
)。__________ 。
a.烟气通入石灰石浆液时的温度越高,吸收越快,吸收率越高
b.反应时需鼓入足量的空气以保证 被充分氧化生成
被充分氧化生成
c.将脱硫后的气体通入 溶液,可粗略判断烟气脱硫效率
溶液,可粗略判断烟气脱硫效率
d.石灰石浆液pH>5.7烟气脱硫效果降低,是因为石灰石的溶解程度增大
(3)写出反应Ⅱ的化学反应方程式_____________________ 。检验反应Ⅱ所得的滤液中所含阴离子的方法是____________________________ 。
(4)向红渣酸浸得到的滤液中加入适量铁粉还原,再由还原后的滤液制得 的操作为:
的操作为:__________ 、__________ 、过滤、洗涤、干燥。
(5)反应①反应方程式是______________ 。从反应①至④制取高纯多晶硅的过程中可以循环利用的物质有____________________ 。
 (杂质为石英)为原料,设计了如下工艺流程:
(杂质为石英)为原料,设计了如下工艺流程: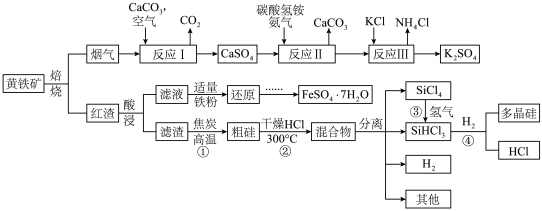
(1)在空气中焙烧黄铁矿的化学方程式为:
(2)研究发现,pH和温度对石灰石浆液的脱硫效率有一定影响。当烟气通入速度一定时,石灰石浆液的脱硫率与浆液pH的关系如图所示(
 )。
)。
a.烟气通入石灰石浆液时的温度越高,吸收越快,吸收率越高
b.反应时需鼓入足量的空气以保证
 被充分氧化生成
被充分氧化生成
c.将脱硫后的气体通入
 溶液,可粗略判断烟气脱硫效率
溶液,可粗略判断烟气脱硫效率d.石灰石浆液pH>5.7烟气脱硫效果降低,是因为石灰石的溶解程度增大
(3)写出反应Ⅱ的化学反应方程式
(4)向红渣酸浸得到的滤液中加入适量铁粉还原,再由还原后的滤液制得
 的操作为:
的操作为:(5)反应①反应方程式是
更新时间:2024-04-20 23:00:40
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
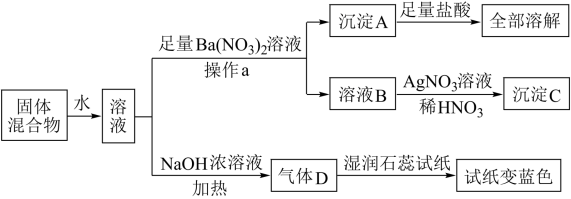
【推荐1】现有五种物质A、B、C、D、E,其中有一种是碱,四种是盐(含正盐和酸式盐),A、B、C溶于水后电离可以产生大量下表中的离子:
为鉴别它们,分别完成以下实验,其结果如下:
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果,填空:
(1)气体X为_______ ,沉淀E为_______ ,沉淀D为_______ 。
(2)B在水溶液中的电离方程式为_______ 。
(3)X与C生成E的离子方程式_______ 。
| 阳离子 |  |
| 阴离子 | 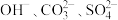 |
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果,填空:
(1)气体X为
(2)B在水溶液中的电离方程式为
(3)X与C生成E的离子方程式
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某无色澄清溶液中可能含有 、
、 、
、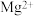 、
、 、
、 、
、 、
、 、
、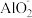 、
、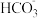 中的几种,且每种离子的物质的量浓度均相等,依次进行如下实验:
中的几种,且每种离子的物质的量浓度均相等,依次进行如下实验:
①向溶液中滴加 滴紫色石蕊溶液,溶液变红;
滴紫色石蕊溶液,溶液变红;
②向溶液中滴加 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
③将②中所得沉淀过滤,向滤液中加入 溶液和稀硝酸,有白色沉淀生成。
溶液和稀硝酸,有白色沉淀生成。
回答下列问题:
(1)由①可判断该溶液中一定没有的离子是___________ ,由①和②可判断该溶液中一定有的离子是 ___________ 。
(2)该溶液中 和
和 能否同时存在
能否同时存在 ___________ (填“能”或“不能”)。
(3)该溶液中所含离子有___________ 或 ___________ 。
 、
、 、
、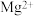 、
、 、
、 、
、 、
、 、
、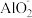 、
、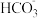 中的几种,且每种离子的物质的量浓度均相等,依次进行如下实验:
中的几种,且每种离子的物质的量浓度均相等,依次进行如下实验:①向溶液中滴加
 滴紫色石蕊溶液,溶液变红;
滴紫色石蕊溶液,溶液变红;②向溶液中滴加
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;③将②中所得沉淀过滤,向滤液中加入
 溶液和稀硝酸,有白色沉淀生成。
溶液和稀硝酸,有白色沉淀生成。回答下列问题:
(1)由①可判断该溶液中一定没有的离子是
(2)该溶液中
 和
和 能否同时存在
能否同时存在 (3)该溶液中所含离子有
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】一种利用湿法炼锌净化渣回收钴并制备碱式碳酸锌的工艺如下图所示,已知净化渣含有较多的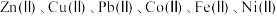 的硫酸盐及氢氧化物(“Ⅱ”指相应元素的化合价为
的硫酸盐及氢氧化物(“Ⅱ”指相应元素的化合价为 价)。
价)。 。
。
(1)浸出渣主要成分为_______ 。
(2)大多数金属硫化物都难溶于水,选择 除铜的原因是
除铜的原因是_______ ,若加入 后溶液中
后溶液中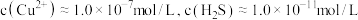 ,则溶液的
,则溶液的 约为
约为_______ 。
(3)研究加入 后温度和时间对金属脱除率的影响,所得曲线如下图所示。
后温度和时间对金属脱除率的影响,所得曲线如下图所示。_______ , 滤渣中还含有
滤渣中还含有_______ 。
(4)在适宜的条件下,加入 并调节溶液
并调节溶液 至
至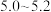 ,反应生成
,反应生成 的离子方程式为
的离子方程式为_______ 。以 湿法炼锌净化渣(
湿法炼锌净化渣( 的质量分数为
的质量分数为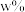 )为原料提取出
)为原料提取出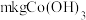 ,在提取过程中钴的损失率为
,在提取过程中钴的损失率为_______  (填含
(填含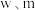 的表达式)。
的表达式)。
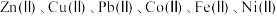 的硫酸盐及氢氧化物(“Ⅱ”指相应元素的化合价为
的硫酸盐及氢氧化物(“Ⅱ”指相应元素的化合价为 价)。
价)。
 。
。(1)浸出渣主要成分为
(2)大多数金属硫化物都难溶于水,选择
 除铜的原因是
除铜的原因是 后溶液中
后溶液中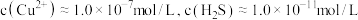 ,则溶液的
,则溶液的 约为
约为(3)研究加入
 后温度和时间对金属脱除率的影响,所得曲线如下图所示。
后温度和时间对金属脱除率的影响,所得曲线如下图所示。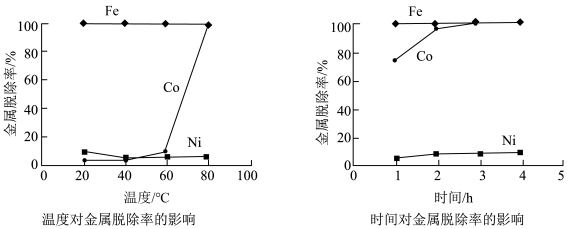
 滤渣中还含有
滤渣中还含有(4)在适宜的条件下,加入
 并调节溶液
并调节溶液 至
至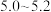 ,反应生成
,反应生成 的离子方程式为
的离子方程式为 湿法炼锌净化渣(
湿法炼锌净化渣( 的质量分数为
的质量分数为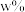 )为原料提取出
)为原料提取出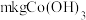 ,在提取过程中钴的损失率为
,在提取过程中钴的损失率为 (填含
(填含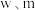 的表达式)。
的表达式)。
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某废旧金属材料中主要含Fe、Cu、Al、FeO、CuO、Al2O3和可燃性有机物(其余成分与酸碱都不反应),为节约和充分利用资源,通过如下工艺流程回收Al、Cu、绿矾(FeSO4·7H2O)等。

回答下列问题:
(1)“焙烧”的目的是_____ 。 中所含化学键的类型是
中所含化学键的类型是_____ 。
(2)提高“碱浸”速率的措施有_____ (任写两条合理措施)。“碱浸”时发生反应的化学方程式为_____ 。
(3)在实验室中进行操作Ⅱ时,用到的玻璃仪器有_____ 种。滤渣2在酸浸时可形成原电池,写出负极反应式:_____ 。
(4)滤液2中可能含有因氧气的作用而产生的少量杂质离子,该反应的离子方程式为_____ 。
(5)由滤液2制取绿矾晶体需先加入少量稀硫酸再经过_____ 、过滤、洗涤、干燥得到绿矾晶体。

回答下列问题:
(1)“焙烧”的目的是
 中所含化学键的类型是
中所含化学键的类型是(2)提高“碱浸”速率的措施有
(3)在实验室中进行操作Ⅱ时,用到的玻璃仪器有
(4)滤液2中可能含有因氧气的作用而产生的少量杂质离子,该反应的离子方程式为
(5)由滤液2制取绿矾晶体需先加入少量稀硫酸再经过
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】LFP是一种常见的锂离子电池正极材料,其中含有LiFePO4、炭黑、铝箔。利用废弃LFP正极材料回收金属、选择性提锂的工艺流程如下图所示。
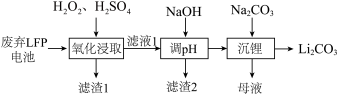
回答下列问题:
(1)Fe位于元素周期表的第___________ 周期___________ 族。
(2)若“滤渣1”中含有炭黑和FePO4,则“氧化浸取”中生成FePO4的离子方程式为___________ 。
(3)“滤渣2”的主要成分是___________ 。
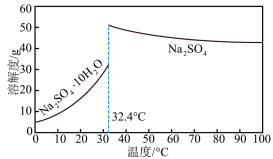
(4) 和Na2SO4的溶解度曲线如下图所示,从母液中获Na2SO4的操作是加热浓缩至有大量晶体析出、
和Na2SO4的溶解度曲线如下图所示,从母液中获Na2SO4的操作是加热浓缩至有大量晶体析出、___________ 、干燥。
(5)利用FePO4和Li2CO3与葡萄糖在氮气氛围中加热能制备LiFePO4和CO,则发生的化学方程式为___________ 。
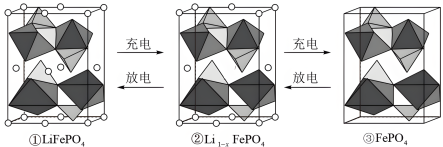
(6)LiFePO4的晶胞结构如图①所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。电池充电时,LiFeO4脱出部分 ,转化为
,转化为 (图②),最终变成FePO4(图③,晶胞参数为a pm、b pm、c pm),则FePO4的晶胞密度为
(图②),最终变成FePO4(图③,晶胞参数为a pm、b pm、c pm),则FePO4的晶胞密度为___________ g/cm3,LiFeO4转化 的电极反应式为
的电极反应式为___________ 。

回答下列问题:
(1)Fe位于元素周期表的第
(2)若“滤渣1”中含有炭黑和FePO4,则“氧化浸取”中生成FePO4的离子方程式为
(3)“滤渣2”的主要成分是
(4)
 和Na2SO4的溶解度曲线如下图所示,从母液中获Na2SO4的操作是加热浓缩至有大量晶体析出、
和Na2SO4的溶解度曲线如下图所示,从母液中获Na2SO4的操作是加热浓缩至有大量晶体析出、
(5)利用FePO4和Li2CO3与葡萄糖在氮气氛围中加热能制备LiFePO4和CO,则发生的化学方程式为
(6)LiFePO4的晶胞结构如图①所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。电池充电时,LiFeO4脱出部分
 ,转化为
,转化为 (图②),最终变成FePO4(图③,晶胞参数为a pm、b pm、c pm),则FePO4的晶胞密度为
(图②),最终变成FePO4(图③,晶胞参数为a pm、b pm、c pm),则FePO4的晶胞密度为 的电极反应式为
的电极反应式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
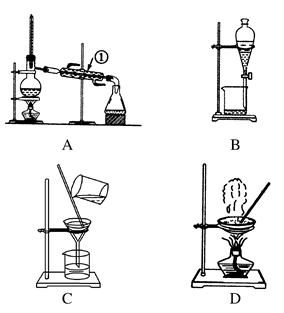
(1)从氯化钾溶液中得到氯化钾固体,选择装置________ (填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置________ 。
(2)从碘水中分离出I2,选择装置______ ,该分离方法的名称为________ 、 ________ 。
(3)装置A中①的名称是________ ,进水的方向是从________ 口进水。装置B在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是:__________ 。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:

 ―→
―→
粗盐中含Ca2+、Mg2+、Fe3+、SO 等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④用适量盐酸调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发
正确的操作顺序是________ (填选项字母)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦
c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
(5)粗盐的提纯实验中每步所加试剂均需过量,如何判断除杂过程中所加BaCl2溶液是否过量?_________________________________________________________ 。

(1)从氯化钾溶液中得到氯化钾固体,选择装置
(2)从碘水中分离出I2,选择装置
(3)装置A中①的名称是
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:

 ―→
―→
粗盐中含Ca2+、Mg2+、Fe3+、SO
 等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④用适量盐酸调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发
正确的操作顺序是
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦
c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
(5)粗盐的提纯实验中每步所加试剂均需过量,如何判断除杂过程中所加BaCl2溶液是否过量?
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】 与
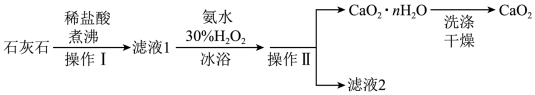
与 都属于过氧化物。过氧化钙(CaO2)是一种难溶于水、可与水缓慢反应、能溶于酸的白色固体,广泛用于果蔬保鲜、空气净化、污水处理等方面。如图是一种制备过氧化钙的实验方法。
都属于过氧化物。过氧化钙(CaO2)是一种难溶于水、可与水缓慢反应、能溶于酸的白色固体,广泛用于果蔬保鲜、空气净化、污水处理等方面。如图是一种制备过氧化钙的实验方法。
已知: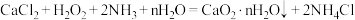
回答下列问题:
(1) 中氧元素化合价
中氧元素化合价___________ ,阴阳离子数之比___________ 。
(2)操作Ⅰ、Ⅱ均为___________ 。
(3)过氧化钙可用于长途运输鱼苗,与此用途无关的性质是___________ 。
A.能缓慢供氧 B.能潮解 C.能抑菌
(4)检验“洗涤”是否完全的方法是:___________ 。
(5)流程中使用“冰浴”的目的是:___________ ;___________ 。
 与
与 都属于过氧化物。过氧化钙(CaO2)是一种难溶于水、可与水缓慢反应、能溶于酸的白色固体,广泛用于果蔬保鲜、空气净化、污水处理等方面。如图是一种制备过氧化钙的实验方法。
都属于过氧化物。过氧化钙(CaO2)是一种难溶于水、可与水缓慢反应、能溶于酸的白色固体,广泛用于果蔬保鲜、空气净化、污水处理等方面。如图是一种制备过氧化钙的实验方法。
已知:
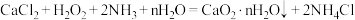
回答下列问题:
(1)
 中氧元素化合价
中氧元素化合价(2)操作Ⅰ、Ⅱ均为
(3)过氧化钙可用于长途运输鱼苗,与此用途无关的性质是
A.能缓慢供氧 B.能潮解 C.能抑菌
(4)检验“洗涤”是否完全的方法是:
(5)流程中使用“冰浴”的目的是:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】HDS催化剂广泛用于石油炼制和化学工业生产中,通常利用加碱焙烧——水浸取法从HDS废催化剂(主要成分为MoS、NiS、V2O5、Al2O3)中提取贵重金属钒和钼,其工艺流程如图所示。
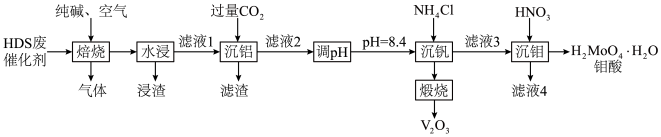
已知:I.MoO3、V2O5、Al2O3均可与纯碱反应生成对应的钠盐,而NiO不行。
II.高温下,NH4VO3易分解产生N2和一种含氮元素的气体。
III.Ksp(CuS)=6×10-36;K1(H2S)=1×10-7、K2(H2S)=6×10-15。
回答下列问题:
(1)“浸渣”的成分为_______ (填化学式);“滤液2”中的成分除了Na2MoO4外,还含有_______ (填化学式)。
(2)请写出“焙烧”过程中MoS及Al2O3分别与纯碱反应的化学方程式:_______ ,_______ 。
(3)“沉钒”时提钒率随初始钒的浓度及氯化铵的加入量的关系如图所示,则选择的初始钒的浓度和NH4Cl的加入量分别为_______ 、_______ 。
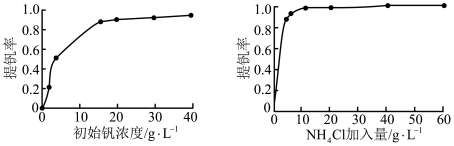
(4)“沉钒”时生成NH4VO3沉淀,请写出“煅烧”后生成氧化产物和还原产物的物质的量之比_______ 。
(5)在实际的工业生产中,“沉钼”前要加入NH4HS进行“除杂”,除掉溶液中微量的Cu2+,则反应Cu2++HS-=CuS↓+H+的K=_______ 。

已知:I.MoO3、V2O5、Al2O3均可与纯碱反应生成对应的钠盐,而NiO不行。
II.高温下,NH4VO3易分解产生N2和一种含氮元素的气体。
III.Ksp(CuS)=6×10-36;K1(H2S)=1×10-7、K2(H2S)=6×10-15。
回答下列问题:
(1)“浸渣”的成分为
(2)请写出“焙烧”过程中MoS及Al2O3分别与纯碱反应的化学方程式:
(3)“沉钒”时提钒率随初始钒的浓度及氯化铵的加入量的关系如图所示,则选择的初始钒的浓度和NH4Cl的加入量分别为

(4)“沉钒”时生成NH4VO3沉淀,请写出“煅烧”后生成氧化产物和还原产物的物质的量之比
(5)在实际的工业生产中,“沉钼”前要加入NH4HS进行“除杂”,除掉溶液中微量的Cu2+,则反应Cu2++HS-=CuS↓+H+的K=
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组以含铜废料(Cu、CuO、Fe、Ag)制备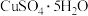 ,实验流程如下所示:
,实验流程如下所示:

(1)“酸浸”时将一定量粉碎后的含铜废料加入到如图的装置中,后通过分液漏斗向废料中滴加混酸(稀硫酸+稀硝酸),在滴加混酸的间隙鼓入氧气,待含铜废料完全溶解后向装置中加入NaCl固体。
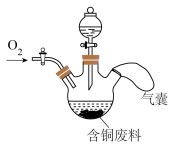
①Cu与混酸发生反应的离子方程式为_______ 。
②鼓入氧气的目的是_______ 。鼓入氧气时可观察到的实验现象为_______ 。
③加入NaCl固体的目的是_______ 。
(2)“调节pH=a”的步骤中,a的值必须满足的条件是_______ 。
(3)请补充完成利用“调节pH”后的滤液制备较纯净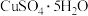 的实验方案:
的实验方案:_______ ,过滤、洗涤、干燥。实验中须选用试剂:3 NaOH溶液、3
NaOH溶液、3 H2SO4溶液、0.01
H2SO4溶液、0.01 AgNO3溶液。
AgNO3溶液。
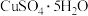 ,实验流程如下所示:
,实验流程如下所示:
(1)“酸浸”时将一定量粉碎后的含铜废料加入到如图的装置中,后通过分液漏斗向废料中滴加混酸(稀硫酸+稀硝酸),在滴加混酸的间隙鼓入氧气,待含铜废料完全溶解后向装置中加入NaCl固体。

①Cu与混酸发生反应的离子方程式为
②鼓入氧气的目的是
③加入NaCl固体的目的是
(2)“调节pH=a”的步骤中,a的值必须满足的条件是
(3)请补充完成利用“调节pH”后的滤液制备较纯净
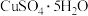 的实验方案:
的实验方案: NaOH溶液、3
NaOH溶液、3 H2SO4溶液、0.01
H2SO4溶液、0.01 AgNO3溶液。
AgNO3溶液。
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某实验小组利用废硫酸液制备 K2SO4 晶体,流程如图所示。回答下列问题:
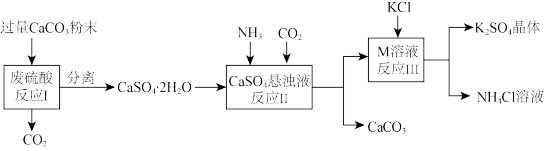
(1)将 CaCO3研成粉末的目的是___________ 。
(2)上述流程中可循环使用的物质有 CO2和___________ (填化学式)。
(3)反应Ⅲ中相关物质的溶解度如下表。
反应Ⅲ的化学方程式为___________ ,该反应在常温下能实现的原因是___________
(4)不用水而用饱和 K2SO4溶液洗涤反应Ⅲ所得晶体的目的是___________ ,为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入___________ (填标号,下同), 振荡、静置,使 SO 完全沉淀,再向上层清液中滴加
完全沉淀,再向上层清液中滴加___________ ,观察现象即可判断。
a.AgNO3溶液
b.过量的BaCl2溶液
c.过量的Ba(NO3)2溶液

(1)将 CaCO3研成粉末的目的是
(2)上述流程中可循环使用的物质有 CO2和
(3)反应Ⅲ中相关物质的溶解度如下表。
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(4)不用水而用饱和 K2SO4溶液洗涤反应Ⅲ所得晶体的目的是
 完全沉淀,再向上层清液中滴加
完全沉淀,再向上层清液中滴加a.AgNO3溶液
b.过量的BaCl2溶液
c.过量的Ba(NO3)2溶液
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】LiCoO2是锂离子电池常用的电极材料。利用原钴矿Co2O3(含Cr2O3、NiS等杂质)制备LiCoO2的工艺流程如下。
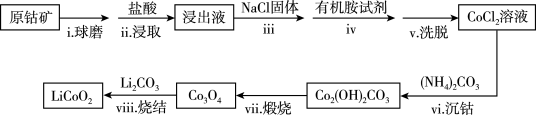
已知:①在含一定量Cl-的溶液中,钻离子以CoCl 形式存在:Co2++4Cl-
形式存在:Co2++4Cl- CoCl
CoCl ;
;
②CoCl 溶于有机胺试剂,有机胺不溶于水;
溶于有机胺试剂,有机胺不溶于水;
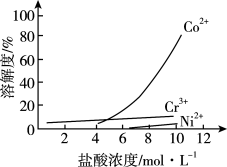
③盐酸溶液中,有机胺试剂对金属离子的溶解率随盐酸浓度变化如图所示:
(1)基态钴原子的价层电子排布式为___________ ,其核外有___________ 种能量不同的电子。
(2)步骤ⅰ的目的是___________ 。
(3)步骤ⅱ中出现了淡黄色沉淀,写出发生该反应的离子方程式___________ 。
(4)从平衡移动角度解释步骤ⅲ中加入NaCl固体的目的___________ 。
(5)步骤ⅳ的操作是___________ 。步骤ⅵ用(NH4)2CO3作沉淀剂,在一定条件下得到碱式碳酸钻Co2(OH)2CO3]。已知碱式碳酸钻在339℃以上开始分解,实验测得在一段时间内加入等量(NH4)2CO3所得沉淀质量随反应温度的变化如图所示。分析曲线下降的原因___________ 。

(6)步骤ⅷ中Co3O4和Li2CO3混合后,鼓入空气,经高温烧结得到LiCoO2。该反应的化学方程式是___________ 。
(7)多次实验测定该原钴矿中钴元素的质量分数为1.18%,假设原钻矿中含钻元素的物质只有Co2O3,则原钴矿中Co2O3的质量分数为___________ %。

已知:①在含一定量Cl-的溶液中,钻离子以CoCl
 形式存在:Co2++4Cl-
形式存在:Co2++4Cl- CoCl
CoCl ;
;②CoCl
 溶于有机胺试剂,有机胺不溶于水;
溶于有机胺试剂,有机胺不溶于水;③盐酸溶液中,有机胺试剂对金属离子的溶解率随盐酸浓度变化如图所示:

(1)基态钴原子的价层电子排布式为
(2)步骤ⅰ的目的是
(3)步骤ⅱ中出现了淡黄色沉淀,写出发生该反应的离子方程式
(4)从平衡移动角度解释步骤ⅲ中加入NaCl固体的目的
(5)步骤ⅳ的操作是

(6)步骤ⅷ中Co3O4和Li2CO3混合后,鼓入空气,经高温烧结得到LiCoO2。该反应的化学方程式是
(7)多次实验测定该原钴矿中钴元素的质量分数为1.18%,假设原钻矿中含钻元素的物质只有Co2O3,则原钴矿中Co2O3的质量分数为
您最近半年使用:0次

 、Cl-、SO
、Cl-、SO 等离子,溶于水配成溶液,取两份该固体的溶液进行如图的实验:
等离子,溶于水配成溶液,取两份该固体的溶液进行如图的实验: