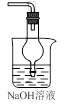
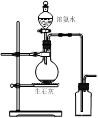
是一种用途广泛的磁性材料,以
是一种用途广泛的磁性材料,以 为原料制备
为原料制备 并获得副产物
并获得副产物 水合物的工艺流程如图所示。
水合物的工艺流程如图所示。
| A.反应釜1需在隔绝空气条件下进行 |
| B.适当升温和搅拌,可提高反应釜中的反应速率 |
C.进入反应釜1和2的 的物质的量之比宜为2∶1 的物质的量之比宜为2∶1 |
D.实验室进行“滤液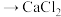 水合物”的操作为加热浓缩、冷却结晶、过滤等 水合物”的操作为加热浓缩、冷却结晶、过滤等 |
2024·海南·三模 查看更多[1]
更新时间:2024-04-30 17:34:47
|
相似题推荐
单选题
|
适中
(0.65)
名校
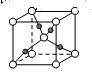
【推荐1】氧化亚铜(Cu2O)主要用于制造杀虫剂、分析试剂和红色玻璃等。在潮湿的空气中会逐渐氧化为黑色的氧化铜。以肼(N2H4)为原料与醋酸铜反应制取Cu2O的反应为: 4 Cu (CH3COO)2+N2H4+2H2O=2Cu2O↓+N2+8CH3COOH。生成的沉淀需用水洗涤后,用乙醇洗涤。下列说法不正确 的是

| A.N2H4能与水分子形成分子间氢键 |
| B.如图所示Cu2O的晶胞中,Cu+的配位数是4 |
| C.每生成标准状况下2.24 L N2,反应转移电子数为0.4×6.02×1023 |
| D.沉淀用水洗后,再用乙醇洗可以除去Cu2O表面的水,防止被氧气氧化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】亚氯酸钠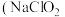 )在溶液中会生成
)在溶液中会生成 、
、 、
、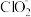 、
、 等,其中
等,其中 和
和 都是具有漂白作用。已知
都是具有漂白作用。已知 ,经测定
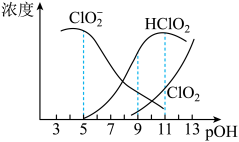
,经测定 时各组分含量随
时各组分含量随 变化情况如图所示(
变化情况如图所示( 浓度没有画出),此温度下,下列分析正确的是
浓度没有画出),此温度下,下列分析正确的是
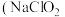 )在溶液中会生成
)在溶液中会生成 、
、 、
、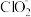 、
、 等,其中
等,其中 和
和 都是具有漂白作用。已知
都是具有漂白作用。已知 ,经测定
,经测定 时各组分含量随
时各组分含量随 变化情况如图所示(
变化情况如图所示( 浓度没有画出),此温度下,下列分析正确的是
浓度没有画出),此温度下,下列分析正确的是
A. 的电离平衡常数的数值 的电离平衡常数的数值 |
B. 时, 时,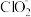 部分转化成 部分转化成 和 和 离子的方程式为: 离子的方程式为: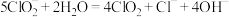 |
C. 时,溶液中含氯微粒的浓度大小为: 时,溶液中含氯微粒的浓度大小为: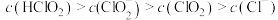 |
D.同浓度 溶液和 溶液和 溶液等体积混合,则混合溶液中有: 溶液等体积混合,则混合溶液中有: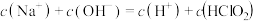 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】SO2直接排放会造成环境污染,可用浓溴水等物质进行回收再利用。单质Se是半导体材料,Se可通过SO2还原H2SeO3获得。K2O2和KO2常用于潜水时的供氧剂。下列化学反应表示正确的是
| A.SO2与溴水反应:SO2+Br2+2H2O=H2SO3+HBr+HBrO |
| B.SO2还原H2SeO3:H2O+2SO2+H2SeO3=Se+2H2SO4 |
| C.KO2与水的反应:KO2+H2O=KOH+O2 |
| D.酸性KMnO4溶液与H218O2反应:2KMnO4+H2l8O2+3H2SO4=K2SO4+MnSO4+318O2↑+4H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】用铁泥(主要成分为Fe2O3、FeO和少量Fe)制备超顺磁性(平均直径25nm)纳米Fe3O4的流程示意图如下:
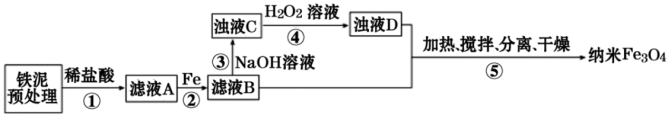
下列叙述不正确 的是

下列叙述
| A.滤液A中含有Fe3+和Fe2+ |
| B.步骤②中,主要反应的离子方程式是Fe3++Fe=2Fe2+ |
| C.步骤④中,反应完成后剩余的H2O2可以通过加热的方式除去 |
| D.步骤⑤中,可将产品均匀分散在水中,利用丁达尔效应验证得到的固体是超顺磁性的Fe3O4粒子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用废旧镀锌铁皮制备 胶体粒子的流程图如下:
胶体粒子的流程图如下:
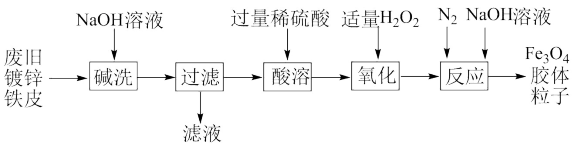
已知:镀锌铁皮就是铁皮表面镀上一层锌; 溶于强碱时生成
溶于强碱时生成 。下列有关说法正确的是
。下列有关说法正确的是
 胶体粒子的流程图如下:
胶体粒子的流程图如下:
已知:镀锌铁皮就是铁皮表面镀上一层锌;
 溶于强碱时生成
溶于强碱时生成 。下列有关说法正确的是
。下列有关说法正确的是| A.用氢氧化钠溶液处理废旧镀锌铁皮,主要目的是为了处理铁皮表面的油污 |
B.“酸溶”的离子方程式为 |
C.“氧化”后溶液中所存在的离子有: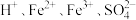 |
D.最后一步“反应”中 的作用是将部分 的作用是将部分 还原成 还原成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】用下列实验方案或装置能很好地达到相应实验目的的是
| 选项 | A | B | C | D |
| 实验方案 | 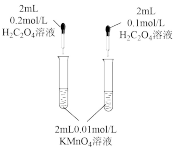 | 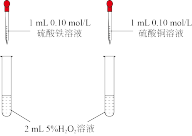 | 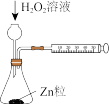 | 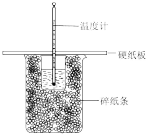 |
| 实验目的 | 探究反应物浓度对化学反应速率的影响 | 探究催化剂对化学反应速率的影响 | 测定化学反应速率 | 测量中和反应的反应热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】探究2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+10CO2↑+8H2O反应速率的影响因素,有关实验数据如下表所示:下列说法不正确的是( )
| 实验编号 | 温度 | 催化剂用量(g) | 酸性KMnO4溶液 | H2C2O4溶液 | KMnO4溶液褪色平均时间 min | ||
| 体积(mL) | 浓度mol·L-1 | 体积(mL) | 浓度 mol·L-1 | ||||
| 1 | 25 | 0.5 | 4 | 0.1 | 8 | 0.2 | 12.7 |
| 2 | 80 | 0.5 | 4 | 0.1 | 8 | 0.2 | a |
| 3 | 25 | 0.5 | 4 | 0.01 | 8 | 0.2 | 6.7 |
| 4 | 25 | 0 | 4 | 0.01 | 8 | 0.2 | b |
| A.a<12.7,b>6.7 |
| B.用KMnO4表示该反应速率,v(实验3)<v(实验1) |
| C.用H2C2O4表示该反应速率,v(实验1)约为7.87×10-5 mol·L-1·min-1 |
| D.可通过比较收集相同体积CO2所消耗的时间来判断反应速率快慢 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法中正确的是
①熵增加且放热的反应一定是自发反应
②凡是放热反应都是自发的,吸热反应都是非自发的
③增大反应物浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多
④有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大
⑤也能用固体或纯液体的变化量来表示反应快慢
⑥催化剂能增大活化分子百分数,从而增大化学反应速率
①熵增加且放热的反应一定是自发反应
②凡是放热反应都是自发的,吸热反应都是非自发的
③增大反应物浓度,可增大单位体积内活化分子数,从而使有效碰撞次数增多
④有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大
⑤也能用固体或纯液体的变化量来表示反应快慢
⑥催化剂能增大活化分子百分数,从而增大化学反应速率
| A.①②③ | B.①③⑥ | C.①④⑤ | D.③⑤⑥ |
您最近一年使用:0次
【推荐1】为提纯下列物质(括号内的物质为杂质),所用除杂试剂和分离方法都正确的是
| A | B | C | D | |
| 物质 | 乙醇(水) | 苯(甲苯) | 乙烷(乙烯) | 溴苯(液溴) |
| 除杂试剂 | 生石灰 | 酸性 溶液 溶液 | 酸性 溶液 溶液 | 苯 |
| 分离方法 | 蒸馏 | 分液 | 洗气 | 分液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】除杂和配制试剂是中学化学中常见的实验。对实验方法描述正确的是
| A.用蒸发结晶法除去KNO3中少量的NaCl |
| B.用加入NaOH(aq)并蒸馏的方法除去乙醛中少量的乙酸 |
| C.准确称取14.800g Ca(OH)2,配制100mL 2.0 mol/L的Ca(OH)2溶液 |
| D.在2mL10%的CuSO4(aq)中滴入3滴 2%的NaOH(aq),配制检验醛基的试剂 |
您最近一年使用:0次

 、
、 、
、 ,不考虑其他杂质)制备七水合硫酸亚铁(
,不考虑其他杂质)制备七水合硫酸亚铁( ),设计了如下流程:
),设计了如下流程: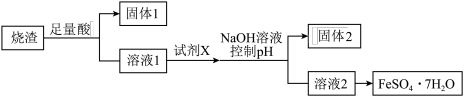
 溶液反应生成偏铝酸钠溶液。
溶液反应生成偏铝酸钠溶液。
 选用铁粉
选用铁粉 中一定有
中一定有 是为了使
是为了使 转化为
转化为 进入固体
进入固体